й«ҳдёҖеҢ–еӯҰдёӢеӯҰжңҹдёӢеҶҢиҜ•йўҳ
дёӢеҲ—е®һйӘҢзҺ°иұЎжҸҸиҝ°дёҚжӯЈзЎ®зҡ„жҳҜ(В В В В В )
| йҖүйЎ№ | е®һйӘҢ | зҺ°иұЎ |
| A | еҠ зғӯж”ҫеңЁеқ©еҹҡдёӯзҡ„е°Ҹеқ—й’ | й’ е…ҲзҶ”еҢ–жҲҗе…үдә®зҡ„е°ҸзҗғпјҢзҮғзғ§ж—¶пјҢзҒ«з„°дёәй»„иүІпјҢзҮғзғ§еҗҺпјҢз”ҹжҲҗж·Ўй»„иүІеӣәдҪ“ |
| B | еңЁй…’зІҫзҒҜдёҠеҠ зғӯй“қз®” | й“қз®”зҶ”еҢ–пјҢеӨұеҺ»е…үжіҪпјҢзҶ”еҢ–зҡ„й“қ并дёҚж»ҙиҗҪпјҢ еҘҪеғҸжңүдёҖеұӮиҶңе…ңзқҖ |
| C | зӮ№зҮғзҡ„й•ҒжқЎдјёе…ҘзӣӣжңүO2зҡ„йӣҶ气瓶пјҲеә•йғЁй“әжңүе°‘йҮҸз»Ҷз Ӯпјүдёӯ | й•ҒжқЎз»§з»ӯзҮғзғ§пјҢеҸ‘еҮәиҖҖзңјзҷҪе…үж”ҫеҮәеӨ§йҮҸзғӯйҮҸпјҢ з”ҹжҲҗзҷҪиүІеӣәдҪ“ |
| D | еңЁз©әж°”дёӯд№…зҪ®зҡ„й“қжқЎж”ҫе…ҘNaOHжә¶ж¶Ідёӯ | з«ӢеҲ»дә§з”ҹеӨ§йҮҸж— иүІж°”жіЎпјҢй“қжқЎйҖҗжёҗеҸҳз»ҶпјҢ й“қжқЎйҖҗжёҗеҸ‘зғӯ |
дёӢеҲ—еҸҷиҝ°дёӯжӯЈзЎ®зҡ„жҳҜпјҲВ В пјү
В AгҖҒеҗ«жңүзҰ»еӯҗй”®зҡ„еҢ–еҗҲзү©дёҖе®ҡжҳҜзҰ»еӯҗеҢ–еҗҲзү©
В BгҖҒеҗ«жңүе…ұд»·й”®зҡ„еҢ–еҗҲзү©дёҖе®ҡжҳҜе…ұд»·еҢ–еҗҲзү©
В CгҖҒзҰ»еӯҗеҢ–еҗҲзү©дёӯдёҚеҸҜиғҪеҗ«жңүе…ұд»·й”®
В DгҖҒе…ұд»·еҢ–![]() еҗҲзү©дёӯеҸҜиғҪеҗ«жңүзҰ»еӯҗй”®
еҗҲзү©дёӯеҸҜиғҪеҗ«жңүзҰ»еӯҗй”®
.дёӢиЎЁдёӯaгҖҒbгҖҒcиЎЁзӨәзӣёеә”д»ӘеҷЁдёӯеҠ е…Ҙзҡ„иҜ•еүӮпјҢеҸҜз”ЁеҰӮеӣҫиЈ…зҪ®еҲ¶еҸ–гҖҒеҮҖеҢ–гҖҒ收йӣҶзҡ„ж°”дҪ“жҳҜпјҡ
| йҖүйЎ№ | ж°”дҪ“ | a | b | c |
|
| A | NH3 | жө“ж°Ёж°ҙ | з”ҹзҹізҒ° | зўұзҹізҒ° | |
| B | CO2 | зӣҗй…ё | зўій…ёй’ҷ | йҘұе’ҢNaHCO3жә¶ж¶І | |
| C | NO | зЁҖзЎқй…ё | й“ңеұ‘ | H2O | |
| D | Cl2 | жө“зӣҗй…ё | дәҢж°§еҢ–й”° | йҘұе’ҢNaClжә¶ж¶І |
пјҺеӮ¬еҢ–ж°§еҢ–зҡ„дә§зү©жҳҜ В зҡ„йҶҮжҳҜпјҲВ В пјү
В зҡ„йҶҮжҳҜпјҲВ В пјү
A. ![]() В В В В В В В В В В В В В В В В В B.
В В В В В В В В В В В В В В В В В B. ![]()
C. ![]() В В В В В В В В В В В В В В В В D.
В В В В В В В В В В В В В В В В D. ![]()
иғҪе®һзҺ°дёӢеҲ—зү©иҙЁй—ҙзӣҙжҺҘиҪ¬еҢ–зҡ„е…ғзҙ жҳҜ(гҖҖгҖҖ)
еҚ•иҙЁ![]() ж°§еҢ–зү©
ж°§еҢ–зү©![]() й…ёжҲ–зўұ
й…ёжҲ–зўұ![]() зӣҗ
зӣҗ
AпјҺй•ҒВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В BпјҺзЎ«
CпјҺй“ңВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В DпјҺй“Ғ
е·ІзҹҘдёӢеҲ—дёӨдёӘзғӯеҢ–еӯҰж–№зЁӢејҸпјҡ
H2(g) + 1/2 O2(g) ![]() H2O(l) в–іH=пјҚ300KJВ·molпјҚ1
H2O(l) в–іH=пјҚ300KJВ·molпјҚ1
C3H8(g) + 5O2(g) ![]() 3CO2(g) + 4H2O(l) в–іH =пјҚ2000.0 KJВ·molпјҚ1
3CO2(g) + 4H2O(l) в–іH =пјҚ2000.0 KJВ·molпјҚ1
е®һйӘҢжөӢеҫ—ж°ўж°”зҡ„дёҷзғ·зҡ„ж··еҗҲж°”дҪ“е…ұ5molпјҢе®Ңе…ЁзҮғзғ§ж—¶ж”ҫзғӯ5000KJпјҢеҲҷж··еҗҲж°”дҪ“дёӯж°ўж°”е’Ңдёҷзғ·зҡ„дҪ“з§ҜжҜ”зәҰдёәпјҲВ В В пјү
A. 7:10В В В B. 3:1В В В C. 10:7В В В D. 1:3
дёӢеҲ—иҜҙжі•дёӯжӯЈзЎ®зҡ„жҳҜ пјҲВ В В пјүВ В В В В В В В В В В В В В В
В пјЎпјҺв… AгҖҒв…ЎAж—Ҹе…ғзҙ зҡ„еҺҹеӯҗпјҢе…¶еҚҠеҫ„и¶ҠеӨ§пјҢи¶ҠйҡҫеӨұеҺ»з”өеӯҗ
В пјўпјҺе…ғзҙ е‘ЁжңҹиЎЁдёӯд»Һв…ўBж—ҸеҲ°в…ЎBж—Ҹ10дёӘзәөиЎҢзҡ„е…ғзҙ йғҪжҳҜйҮ‘еұһе…ғзҙ
В пјЈпјҺеҺҹеӯҗеҸҠе…¶зҰ»еӯҗзҡ„ж ёеӨ–з”өеӯҗеұӮж•°зӯүдәҺиҜҘе…ғзҙ жүҖеңЁзҡ„е‘Ёжңҹж•°
В пјӨпјҺжүҖжңүдё»ж—Ҹе…ғзҙ зҡ„еҺҹеӯҗпјҢйғҪиғҪеҪўжҲҗеҚ•еҺҹеӯҗзҰ»еӯҗ
ж №жҚ®дёӢеҲ—еҸҳеҢ–е…ізі»пјҢиҜ·еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ(AпҪһEеқҮеҲҶеҲ«д»ЈиЎЁдёҖз§Қзү©иҙЁпјҢжЎҶеӣҫдёӯзҡ„йғЁеҲҶдә§зү©е·Із•ҘеҺ»пјҢеҰӮAз”ҹжҲҗDзҡ„еҗҢж—¶иҝҳжңүCO2з”ҹжҲҗ)

(1)еҶҷеҮәAзү©иҙЁзҡ„еҗҚз§°гҖҖгҖҖгҖҖгҖҖгҖӮеҠ Bжә¶ж¶Ізҡ„дҪңз”ЁдёәгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖгҖӮВ
(2)еҶҷеҮәDзҡ„з»“жһ„з®ҖејҸВ В В В В В В В В В В В В В В В гҖӮ
(3)еҶҷеҮәдёӢеҲ—еҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸ:
в‘ўгҖҖВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В гҖӮВ
в‘ЈгҖҖВ В В В В В В В В В В В В В В ![]() В В В В В В В В В В В В В В В В В гҖӮВ
В В В В В В В В В В В В В В В В В гҖӮВ
в‘ҘгҖҖВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В гҖӮВ
(4)еҸҚеә”в‘Ҙзҡ„еҸҚеә”зұ»еһӢжҳҜгҖҖгҖҖгҖҖгҖҖгҖҖгҖӮВ
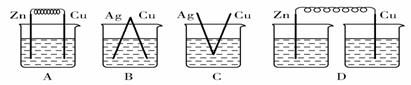
жңүе…ідёӢеҲ—еӣӣдёӘеёёз”Ёз”өеҢ–еӯҰиЈ…зҪ®зҡ„еҸҷиҝ°дёӯпјҢжӯЈзЎ®зҡ„жҳҜпјҲВ В пјү
|
|
|
|
|
| еӣҫв… зўұжҖ§й”Ңй”°з”өжұ | еӣҫв…Ўй“…-зЎ«й…ёи“„з”өжұ | еӣҫв…ўз”өи§ЈзІҫзӮјй“ң | еӣҫⅣ银й”ҢзәҪжүЈз”өжұ |
AпјҺеӣҫв… жүҖзӨәз”өжұ дёӯпјҢMnO2зҡ„дҪңз”ЁжҳҜеӮ¬еҢ–![]() еүӮ
еүӮ
BпјҺеӣҫв…ЎжүҖзӨәз”өжұ ж”ҫз”өиҝҮзЁӢдёӯпјҢзЎ«й…ёжө“еәҰдёҚж–ӯеўһеӨ§
CпјҺеӣҫв…ўжүҖзӨәиЈ…зҪ®е·ҘдҪңиҝҮзЁӢдёӯпјҢз”өи§ЈиҙЁжә¶ж¶ІдёӯCu2+жө“еәҰе§Ӣз»ҲдёҚеҸҳ
DпјҺеӣҫв…ЈжүҖзӨәз”өжұ дёӯпјҢAg2OжҳҜж°§еҢ–еүӮпјҢз”өжұ е·ҘдҪңиҝҮзЁӢдёӯиў«иҝҳеҺҹдёәAg
дёӢеҲ—е…ідәҺиӢҜзҡ„еҸҷиҝ°жӯЈзЎ®зҡ„жҳҜ(В В В В )

A. еҸҚеә”в‘ дёәеҸ–д»ЈеҸҚеә”пјҢжңүжңәдә§зү©зҡ„еҜҶеәҰжҜ”ж°ҙе°Ҹ
B. еҸҚеә”в‘Ўдёәж°§еҢ–еҸҚеә”пјҢеҸҚеә”зҺ°иұЎжҳҜзҒ«з„°жҳҺдә®е№¶еёҰжңүиҫғеӨҡзҡ„й»‘зғҹ
C. еҸҚеә”в‘ўдёәеҸ–д»ЈеҸҚеә”пјҢжңүжңәдә§зү©жҳҜдёҖз§Қзғғ
D. еҸҚеә”в‘Ј1molиӢҜжңҖеӨҡдёҺ3molH2еҸ‘з”ҹеҠ жҲҗеҸҚеә”пјҢжҳҜеӣ дёәиӢҜеҲҶеӯҗеҗ«жңүдёүдёӘзўій…ёеҸҢй”®
дёӢеҲ—е®һйӘҢдёӯпјҢдёҚиғҪи§ӮеҜҹеҲ°жҳҺжҳҫеҸҳеҢ–зҡ„жҳҜпјҲВ В В пјү
A. жҠҠдёҖж®өжү“зЈЁиҝҮзҡ„й•ҒеёҰж”ҫе…Ҙе°‘йҮҸеҶ·ж°ҙдёӯ
B. жҠҠCl2йҖҡе…ҘFeCl2жә¶ж¶Ідёӯ
C. жҠҠз»ҝиұҶеӨ§зҡ„й’ҫжҠ•е…Ҙж°ҙдёӯ
D. жҠҠжәҙж°ҙж»ҙеҠ еҲ°KIж·ҖзІүжә¶ж¶Ідёӯ
дёӢеҲ—еҢ–еӯҰз”ЁиҜӯдёӯпјҢжӯЈзЎ®зҡ„жҳҜпјҲпјү
A. ж¬Ўж°Ҝй…ёзҡ„з»“жһ„ејҸпјҡHвҖ”OвҖ”Cl
B. ж°®ж°”зҡ„з”өеӯҗејҸпјҡвҲ¶NвҲ¶вҲ¶вҲ¶NвҲ¶
C. CO2еҲҶеӯҗзҡ„зҗғжЈҚжЁЎеһӢпјҡ![]()
D. з”Ёз”өеӯҗејҸиЎЁзӨәж°ҜеҢ–ж°ўеҲҶеӯҗзҡ„еҪўжҲҗиҝҮзЁӢпјҡ![]()
жө·жҙӢдёӯжңүеӨ§йҮҸзҡ„е®қиҙөиө„жәҗгҖӮдёӢйқўжҳҜе·ҘдёҡдёҠеҲ©з”Ёжө·ж°ҙжҸҗеҸ–жәҙе’Ңй•Ғзҡ„жөҒзЁӢеӣҫгҖӮ
в‘Ў в‘
В
В 
пјҲ1пјүжҸҗеҸ–жәҙзҡ„иҝҮзЁӢдёӯпјҢеңЁз¬¬2ж¬ЎBrпјҚвҶ’Br2 зҡ„иҪ¬еҢ–дёӯпјҢжҜҸдә§з”ҹ1molжәҙж¶ҲиҖ—ж ҮеҶөдёӢж°Ҝж°”______LгҖӮ
пјҲ2пјүеңЁеҗёж”¶еЎ”дёӯпјҢд»ҺзҗҶи®әдёҠиҖғиҷ‘дёӢеҲ—зү©иҙЁд№ҹиғҪеҗёж”¶Br2зҡ„жҳҜ________гҖӮ
AпјҺKBrВ В В В В В BпјҺNa2SO4В В В В В В В CпјҺFeCl3В В В В В В DпјҺH2S
пјҲ3пјүеңЁеҗёж”¶еЎ”дёӯеҸ‘з”ҹеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸжҳҜ___________________________гҖӮ
пјҲ4пјүеҶҷеҮәж°ўж°§еҢ–й•Ғеҫ—еҲ°й•Ғзҡ„жөҒзЁӢдёӯж¶үеҸҠеҲ°зҡ„еҸҚеә”ж–№зЁӢејҸв‘ ___________________________гҖҒв‘Ў___________________________гҖӮ
д»ҘдёӢеӣӣз§Қж ҮзӯҫпјҢйҖӮеҗҲиҙҙеңЁж— ж°ҙд№ҷйҶҮиҜ•еүӮ瓶дёҠзҡ„жҳҜ(гҖҖгҖҖ)

дёӢеҲ—зғ§жқҜдёӯзӣӣж”ҫзҡ„йғҪжҳҜзЁҖзЎ«й…ёпјҢеңЁй“ңз”өжһҒдёҠиғҪдә§з”ҹеӨ§йҮҸж°”жіЎзҡ„жҳҜ(гҖҖгҖҖ)
дёӢеҲ—еҗ„зү©иҙЁеҗҢеҲҶејӮжһ„дҪ“жңҖеӨҡзҡ„жҳҜ(В В В )
AпјҺжҲҠзғ·В В В BпјҺC3H6Cl2В В В CпјҺйӮ»дәҢз”ІиӢҜВ В В DпјҺ2 вҖ”дёҒзғҜ
гҖҖ
еҜ№дәҺеҸҜйҖҶеҸҚеә”4 NH3(g)пјӢ5O2(g)![]() 4NO(g)пјӢ6 H2O(g),дёӢеҲ—еҸҷиҝ°жӯЈзЎ®зҡ„жҳҜ
4NO(g)пјӢ6 H2O(g),дёӢеҲ—еҸҷиҝ°жӯЈзЎ®зҡ„жҳҜ
A. NH3е’Ң![]() H2OеҢ–еӯҰеҸҚеә”йҖҹзҺҮе…ізі»жҳҜ2vжӯЈпјҲNH3пјү= 3vжӯЈпјҲH2Oпјү
H2OеҢ–еӯҰеҸҚеә”йҖҹзҺҮе…ізі»жҳҜ2vжӯЈпјҲNH3пјү= 3vжӯЈпјҲH2Oпјү
B. иҫҫеҲ°еҢ–еӯҰе№іиЎЎж—¶пјҢ4vжӯЈпјҲO2пјү= 5vйҖҶпјҲNO пјү
C. иҫҫеҲ°еҢ–еӯҰе№іиЎЎж—¶пјҢиӢҘеўһеҠ е®№еҷЁдҪ“з§ҜпјҢеҲҷжӯЈеҸҚеә”йҖҹзҺҮеҮҸе°‘пјҢйҖҶеҸҚеә”йҖҹзҺҮеўһеӨ§
D. иӢҘеҚ•дҪҚж—¶й—ҙеҶ…з”ҹжҲҗx mol NOзҡ„еҗҢж—¶пјҢж¶ҲиҖ—x mol NH3 пјҢеҲҷеҸҚеә”иҫҫеҲ°е№іиЎЎзҠ¶жҖҒ
еҸҜйҖҶеҸҚеә”пјҡ![]() еңЁжҒ’жё©жҒ’е®№еҜҶй—ӯе®№еҷЁдёӯеҸҚеә”пјҢиҫҫеҲ°е№іиЎЎзҠ¶жҖҒзҡ„ж Үеҝ—жҳҜ
еңЁжҒ’жё©жҒ’е®№еҜҶй—ӯе®№еҷЁдёӯеҸҚеә”пјҢиҫҫеҲ°е№іиЎЎзҠ¶жҖҒзҡ„ж Үеҝ—жҳҜ
![]() еҚ•дҪҚж—¶й—ҙеҶ…з”ҹжҲҗnВ
еҚ•дҪҚж—¶й—ҙеҶ…з”ҹжҲҗnВ ![]() зҡ„еҗҢж—¶ж¶ҲиҖ—2nВ
зҡ„еҗҢж—¶ж¶ҲиҖ—2nВ ![]() пјӣ
пјӣ
![]() еҚ•дҪҚж—¶й—ҙеҶ…з”ҹжҲҗnВ
еҚ•дҪҚж—¶й—ҙеҶ…з”ҹжҲҗnВ ![]() В зҡ„еҗҢж—¶ж¶ҲиҖ—2nВ molВ NOпјӣ
В зҡ„еҗҢж—¶ж¶ҲиҖ—2nВ molВ NOпјӣ
![]() ж··еҗҲж°”дҪ“зҡ„йўңиүІдёҚеҶҚж”№еҸҳзҡ„зҠ¶жҖҒпјӣ
ж··еҗҲж°”дҪ“зҡ„йўңиүІдёҚеҶҚж”№еҸҳзҡ„зҠ¶жҖҒпјӣ
![]() ж··еҗҲж°”дҪ“дёӯ
ж··еҗҲж°”дҪ“дёӯ![]() дёҚеҸҳпјӣ
дёҚеҸҳпјӣ
![]() зҡ„ж¶ҲиҖ—йҖҹзҺҮдёҺNOзҡ„з”ҹжҲҗйҖҹзҺҮзӣёзӯүпјӣ
зҡ„ж¶ҲиҖ—йҖҹзҺҮдёҺNOзҡ„з”ҹжҲҗйҖҹзҺҮзӣёзӯүпјӣ
![]() е®№еҷЁеҶ…еҺӢејәдёҚйҡҸж—¶й—ҙеҸҳеҢ–иҖҢеҸҳеҢ–гҖӮ
е®№еҷЁеҶ…еҺӢејәдёҚйҡҸж—¶й—ҙеҸҳеҢ–иҖҢеҸҳеҢ–гҖӮ
A. ![]() В В В В В В В В В В В В B.
В В В В В В В В В В В В B. ![]() В В В В В В В В В C.
В В В В В В В В В C. ![]() В В В В В В В В В В В В D.
В В В В В В В В В В В В D. ![]()
зҷҪзЈ·ж”ҫе…Ҙзғӯзҡ„ CuSO4 жә¶ж¶ІдёӯеҸ‘з”ҹеҰӮдёӢеҸҚеә”:
11P+15CuSO4+24H2O ==5Cu3P+6H3PO4+15H2SO4пјҢеҲҷ 160g CuSO4 жүҖж°§еҢ–зҡ„зЈ·зҡ„зү©иҙЁзҡ„
йҮҸдёә
A.0.2molВ В В В В В В В В В В В В В В В В В В В В В B.0.3molВ В В В В В В В В В В В В В C.0.4mol В В В В В В В В В В В В В В В D.0.5mol
В
дёӢеҲ—еҸҚеә”дә§з”ҹзҡ„ж°”дҪ“пјҢйҖҡе…ҘNa2S03жә¶ж¶ІдёҚеҸҚеә”зҡ„жҳҜ
в‘ Na202е’ҢC02 в‘ЎA1е’ҢNaOHжә¶ж¶І в‘ўMn02е’Ңжө“зӣҗй…ёе…ұзғӯ в‘Јжө“зЎқй…ёе’Ңй“ңзүҮв‘Өй“ңзүҮе’Ңжө“зЎ«й…ёе…ұзғӯ
A. в‘ в‘ЎВ В В B. еҸӘжңүв‘ЎВ В В C. в‘ в‘Ўв‘ӨВ В В D. в‘Ўв‘Јв‘Ө








