高一化学下学期下册试题
.下列有关化学键和化合物的说法不正确的是
A.离子键就是阴阳离子间强烈的静电作用
B.H和Cl形成的分子中存在的是极性共价键
C.氯化铵中没有金属元素,所以不是离子化合物
D.11号与9号元素能够形成离子化合物,该化合物中存在离子键
下列叙述错误的是( )
A.油脂、淀粉、蔗糖和蛋白质在一定条件都能发生水解反应
B.甲烷和苯都不能与溴水、酸性高锰酸钾溶液发生反应,但苯不属于饱和烃
C.将红热的铜丝迅速插入乙醇中,可观察到铜丝表面变红,并能闻到刺激性气味
D.煤中含有苯![]() 、甲苯,可用先干馏后分馏的方法将它们分离出来
、甲苯,可用先干馏后分馏的方法将它们分离出来
将下列溶液置于敞口容器中,溶液质量会增加的是( )
A.浓硫酸 B.稀硫酸 C.浓盐酸 D.浓硝酸
A、B、C、D为原子序数依次增大的短周期元素。已知A的某种单质是自然界中硬度最大的物质,C元素是短周期主族元素中原子半径最大的元素,a为A的最高价氧化物,b、c、d分别为B、C、D的最高价氧化物对应的水化物。化和物a~g的转化关系如图所示(部分产物己略去)。下列说法正确的是( )
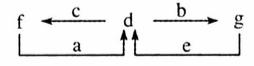
A. 简单离子半径的大小:C>D>B
B. a中只含非极性共价键,属于共价化合物
C. B的氢化物的稳定性和沸点均大于A的氢化物
D. 工业上通过电解其![]() 氯化物的方法制取D的单质
氯化物的方法制取D的单质
已知A、B、C、D、E、F是前四周期中的元素(不包括稀有气体元素)有关性质和相关信息如下表:
| 元素 | 相 关 信 息 |
| A | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| B | 最高价氧化物对应的水化物能1:1电离出电子数相等的阴阳离子 |
| C | 所在主族序数与所在周期序数之差为4,非金属性在同周期元素中最强 |
| D | 其单质为淡黄色气体 |
| E | 它是日常生活中接触最多的过渡金属元素,密度7.8g/m3 |
| F | D元素的单质在F元素的单质中燃烧,发出明亮的蓝紫色火焰 |
(1)F在元素周期表中的位置为 。B和F形成的含有共价键的化合物的电子式为 。
(2)C、D的最高价氧化物对应的水化物中,酸性强的化学式是: 。
(3)用一个化学方程式证明非金属性F>D: 。
(4)1molA的某种氢化物甲中含18mol电子,写出甲的结构式: 。
(5)用亚硝酸氧化化合物甲,可生成A的另一种氢化物乙,乙的相对分子质量为43,其中A原子的质量分数为97.7%,则乙的分子式为 。
(6)在碱性条件下,C的单质可与EF2-反应制备一种可用于净水的盐EF42-,该反应的离子方程式为 。
某阴离子X2﹣有m个电子,其质量数![]() a,则核内中子数为( )
a,则核内中子数为( )
A. m+2 B. m+5 C. a﹣m+2 D. a﹣m﹣2
在恒温、恒容的容器中进行反应:N2(g)+3H2(g)![]() 2NH3(g),若氮气浓度由0.1 mol/L降到0.06 mol/L需2 s,那么由0.06 mol/L降到0.024 mol/L需要的反应时间为
2NH3(g),若氮气浓度由0.1 mol/L降到0.06 mol/L需2 s,那么由0.06 mol/L降到0.024 mol/L需要的反应时间为![]() ( )
( )
A.等于1.8 s B.等于1.2 s C.大于1.8 s D.小于1.8 s
根据①~⑩元素的编号所在周期表中的位置,用化.学.用.语.回答有关问题:

(1)最难形成简单离子的元素是____,元素⑧的最高价氧化物的水化物的化学式为_____;
(2)①与⑤能形成 9 电子微粒,其名称为____;①与⑦可组成原子个数比为 1:1的化合物甲,将⑨的单质通入甲的水溶液中,生成一种强酸且有气体放出,该反应的化学方程式为____;
(3)元素⑥、⑧形成的简单氢化物中,沸点较高的是_____,原因是____;
(4)③与⑦的单质加热条件下可发生反应,产物的化学式为____;
(5)元素④与铝性质相似,其最高价氧化物的水化物能与⑩的氢氧化物反应,离子方程 式为___。
下列说法正确的是
A. 实验室鉴别丙烯和苯,可以用酸性高锰酸钾溶液
B. 甲烷、乙烯和苯都可以与溴水发生反应
C. 乙醇被氧化只能生成乙醛
D. 乙醇和乙酸生成乙酸乙酯的反应不属于取代反应
铋(Bi)的化合物在医药方面用于治疗皮肤损伤和肠胃病。下列关于![]() Bi和
Bi和![]() Bi的说法正确的是
Bi的说法正确的是
A.![]() Bi和
Bi和![]() Bi互为同素异形体 B.
Bi互为同素异形体 B.![]() Bi和
Bi和![]() Bi互为同位素
Bi互为同位素
C.![]() Bi和
Bi和![]() Bi的核外电子数不同 D.
Bi的核外电子数不同 D.![]() Bi和
Bi和![]() Bi分别含有126和127个质子
Bi分别含有126和127个质子
下列有关化学![]() 用语表述正确的是( )
用语表述正确的是( )
![]() A.甲烷的结构式:H
A.甲烷的结构式:H![]() H B.质量数为37的氯原子:
H B.质量数为37的氯原子:![]()
![]() Cl
Cl
C.乙烯的结构简式:CH2CH2 D.S2-的结构示意图:

如右图所示,将相同条件下的m体积NO和n体积O2同时通入倒立于水槽中且盛满水的试管内,充分反应后,试管内残留![]() 体积的气体,该气体与空气接触后立即变为红棕色。则n与m的比值为 ( )
体积的气体,该气体与空气接触后立即变为红棕色。则n与m的比值为 ( )
A.3∶2 B.2∶3
C.8∶3 D.3∶8
下列关于能量转化的说法中正确的是( )
A.给手机充电时:化学能转化为电能
B.铅蓄电池的放电过程:电能转化为化学能
C.氢气在氧气中燃烧:化学能转化为热能和光能
D.植物的光合作用:生物质能(化学能)转化为光能(太阳能)
下列各组给定原子序数的元素,不能形成原子数之比为1∶1稳定化合物的是
A. 3和17 B. 1和8 C. 1和9 D. 17和12
下列各组物质反应产生的气体分别通入Na2SO3溶液中,与Na2SO3不发生反应的是( )①Na2O2和CO2 ②Al和NaOH溶液 ③MnO2和浓盐酸共热
④浓硝酸和铜片 ⑤铜片和浓硫酸共热
A.只有② B.只有①② C.只有①②⑤ D.只有②④⑤
下列各种混合物,能用分液漏斗分离的是( )
A.水和苯 B.水和乙醇 C.碘和酒精 D.乙酸和乙醇
下列关于金属铝的叙述中,说法不正确的是( )
A.Al是地壳中含量最多![]() 的元素
的元素
B.Al是比较活泼的金属,在化学反应中容易失去电子,表现还原性
C.铝箔在空气中受热可以熔化。
D.铝箔在空气中受热可![]() 以熔化,由于氧化膜的存在,熔化的铝并不滴落
以熔化,由于氧化膜的存在,熔化的铝并不滴落
下列说法正确的是( )
A. 含有共价键的化合物一定是共价化合物
B. KI和HI中化学键类型完全相同
C. Na2O2中既含有离子键又含有非极性共价键
D. KOH中只含有共价键
下列操作不能达到实验目的是 ( )
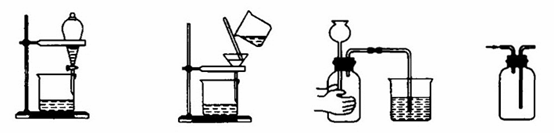
A.分离汽油与水B.除去Na2SO4溶液中的BaSO4 C.检验装置气密性 D.收集H2
X、Y、Z、W均为短周期元素,在周期表中位置如图,Y原子的最外层电子数是其次外层电子数的3倍。下列说法正确的是( )
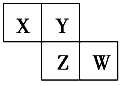
A. X、Y、Z的原子半径大小:X>Y>Z
B. Y、Z的气态氢化物中,前者更稳定
C. Z、W的最高价氧化物对应水化物的酸性,前者更强
D. X、W的气态氢化物相互反应,生成物中只含离子键不含共价键



