2020年九年级化学上学期会考真题免费检测试卷
| 1. 选择题 | 详细信息 |
|
“绿色消费”理念强调节约资源,保护生态环境,下列做法不符合这一理念的是 A.开发燃煤新技术使其充分燃烧 B.推广太阳能、风能可缓解温室效应 C.大量使用化肥、农药提高农作物产量 D.淘汰尾气排放不合格车辆,减少汽车尾气污染 |
|
| 2. 选择题 | 详细信息 |
|
下列物质属于纯净物的是 A.水银 B.牛奶 C.生铁 D.大理石 |
|
| 3. 选择题 | 详细信息 |
|
下列实验操作正确的是( ) A. 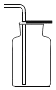 收集氧气 B. 收集氧气 B. 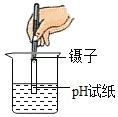 测定溶液的pH 测定溶液的pHC. 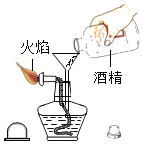 添加酒精 D. 添加酒精 D. 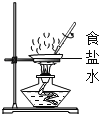 蒸发食盐水 蒸发食盐水 |
|
| 4. 选择题 | 详细信息 |
|
下列化学用语所表达的意义正确的是( ) A.2K﹣﹣2个钾元素 B.Fe2+﹣﹣1个铁离子 C.K2MnO4﹣﹣高锰酸钾 D.2N2﹣﹣2个氮分子 |
|
| 5. 选择题 | 详细信息 |
|
下列物质的用途主要利用其化学性质的是 A.酒精作燃料 B.用石墨制铅笔芯 C.用铜丝作导线 D.液氮冷冻治疗皮肤病 |
|
| 6. 选择题 | 详细信息 |
中国对大深度载人潜水器“蛟龙号”的研制取得了世界嘱目的成绩,实现了我国挺进深蓝的宏伟目标,乘蛟龙号下潜的科研人员,他们的呼吸环境必须注意调节的是( ) A. O2和H2O的含量 B. O2和N2的含量 C. O2和H2的含量 D. O2和CO2的含量 |
|
| 7. 选择题 | 详细信息 |
下列标志属于中国节能标志的是  A. A B. B C. C D. D |
|
| 8. 选择题 | 详细信息 |
|
“垃圾分类新时尚”,下列垃圾分类不合理的是 A.可回收物:易拉罐 B.其他垃圾:废报纸 C.有害垃圾:废旧电池 D.厨余垃圾:剩余饭菜 |
|
| 9. 选择题 | 详细信息 |
|
材料是人类发展中的重要物质,很多学校使用的电子白板是纳米陶瓷材质,纳米陶瓷属于 A.合成材料 B.复合材料 C.金属材料 D.无机非金属材料 |
|
| 10. 选择题 | 详细信息 |
钪(Kc)是一种“工业的维生素”。下图为钪在元素周期表中的相关信息及其原子的结构示意图。下列说法正确的是( )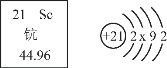 A. 钪属于非金属元素 B. 钪的相对原子质量是 21 C. 原子结构示意图中 X = 10 D. 钪原子核外有四个电子层 |
|
| 11. 选择题 | 详细信息 |
|
下列关于化学与健康的说法正确的是 A.油脂和维生素不属于食物中的营养成分 B.误食重金属盐,可喝些牛奶或蛋清应急解毒 C.缺铁会使儿童发育停滞、智力低下,严重时会得侏儒症 D.纤维素不能被人体吸收,所以食物中的纤维素对人体毫无意义 |
|
| 12. 选择题 | 详细信息 | ||||||||||
某化学实验室有四个药品橱,分别存放了以下药品
|
|||||||||||
| 13. 选择题 | 详细信息 |
|
(2018 达州改编)误差分析是定量实验的一个重要内容,下列分析正确的是( ) A.用量筒量取10毫升水,仰视读数,会导致水的实际体积偏小 B.测定溶液的pH,先用水将pH试纸润湿,会导致测出的pH偏大 C.测定空气中氧气的体积分数,红磷的量不足,会导致测出氧气的体积分数偏小 D.配制6%的氯化钠溶液,氯化钠中含有杂质,会导致氯化钠的质量分数偏大 |
|
| 14. 选择题 | 详细信息 |
|
根据你的化学知识和生活经验判断,下列说法正确的是 A.生铁和钢的性能不同,因为生铁的含碳量比钢少 B.燃料电池是一种将化学能直接转化成电能的装置 C.纸篓着火用水浇灭,因为水能降低可燃物的着火点 D.铁桶不能盛放波尔多液,因为铁能和氢氧化铜发生反应 |
|
| 15. 选择题 | 详细信息 |
|
尿素是一种重要的化肥,它的化学式为(CO(NH2)2),下列关于尿素的说法正确的是 A.尿素属于有机氮肥 B.尿素的相对分子质量是60g C.尿素不能与碱性物质混合使用 D.尿素由一氧化碳分子、氮原子和氢原子构成 |
|
| 16. 选择题 | 详细信息 |
|
金属和溶液在生活中有着广泛的用途,下列有关说法正确的是 A.油可以用洗洁精洗去是因为油能溶解在洗洁精中 B.铁粉是“暖宝宝”的原料之一,因为铁能与氧气和水反应放热 C.蔗糖、氢氧化钠的水溶液都能导电,因为溶液中都有自由移动的离子 D.武德合金(铋、铅、锡、镉等金属合金)用于电路保险丝,熔点比锡高 |
|
| 17. 选择题 | 详细信息 |
|
建立模型是学习化学的重要方法。下列有关模型正确的是 A. 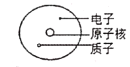 原子结构模型 B. 原子结构模型 B.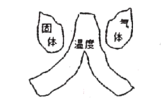 燃烧条件模型 燃烧条件模型C. 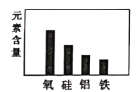 地壳中元素含量 D. 地壳中元素含量 D. 空气组成模型 空气组成模型 |
|
| 18. 选择题 | 详细信息 |
|
下列变化,遵循质量守恒定律的是 A.用催化剂将水变成汽油 B.石墨制成金刚石 C.2g氢气完全燃烧生成36g水 D.20g酒精和20g水混合后得到40g酒精溶液 |
|
| 19. 选择题 | 详细信息 |
工业上使用一种国产低温催化剂生产氢气的反应过程如下图所示: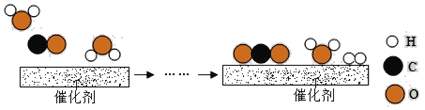 下列说法正确的为 A.该微观反应过程中出现了二种氧化物 B.参加反应的水与一氧化碳分子个数之比为1:1 C.该反应中水起了催化作用 D.此反应中有单质生成的同时还生成了二种氧化物 |
|
| 20. 选择题 | 详细信息 |
|
下列物质间的转化不能一步实现的是 A.H2O2→H2 B.CO2→O2 C.Fe→Fe3O4 D.CaO→CaCl2 |
|
| 21. 选择题 | 详细信息 |
|
现有50g溶质的质量分数为10%的硝酸钠溶液.要使其溶质的质量分数增大1倍,可采用的方法是 A.增加5g硝酸钠 B.倒掉一半溶液 C.蒸发掉25g水 D.增加50g同种溶液 |
|
| 22. 选择题 | 详细信息 |
|
下列各组离子在溶液中能大量共存的是 A.K+、 C. |
|
| 23. 选择题 | 详细信息 |
|
在一定溶质质量分数的稀盐酸中加入下列物质,充分反应后,溶液的pH没有明显变化的是 A.锌粉 B.硝酸银粉末 C.碳酸钙粉末 D.氢氧化钡粉末 |
|
| 24. 选择题 | 详细信息 | |||||||||||||||
下列实验方案不能达到实验目的是
|
||||||||||||||||
| 25. 选择题 | 详细信息 |
|
在CO和CO2的混合气体中,含氧元素64 %,将5g该混合气体通过足量灼热的氧化铁,完全反应后,气体再通入足量的澄清石灰水中,得到的白色沉淀质量是 A.5 g B.10g C.15g D.20g |
|
| 26. 填空题 | 详细信息 |
|
化学源于生活,生活中蕴含着许多化学知识。 (1)生理盐水中的溶质是________; (2)可用于急救病人的气体是________; (3)生活用水多是硬水,生活中常用____的方法降低水的硬度; (4)家用净水器中一般都会用到活性炭,是因为其具有___作用; (5)“端午节”有吃粽子的习俗,粽子中糯米为人体提供主要的营养成分是__________; (6)“84”消毒液有效成分为次氯酸钠(NaClO),次氯酸钠中氯元素的化合价是______。 |
|
| 27. 填空题 | 详细信息 |
金属的用途与性质密切相关。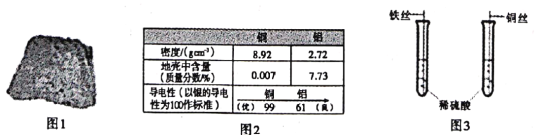 (1)图1所示赤铁矿的主要成分是_______(填化学式)。 (2)沿江铁路的建成,使常熟市民的出行更为方便。铁路建设需要大量的钢铁,在炼铁高炉中将赤铁矿还原为铁的主要化学方程式是___________。 (3)家用电线常用铜制,但在高压远距离输电中,常用铝代替铜,请根据图2的信息分析,其原因是__________。 (4)在空气中,铝具有很好的抗腐蚀性,其原因用化学方程式表示为_______。 (5)新能源汽车越来越受到人们的青睐,华晨宝马530Le新能源汽车定位系统微电脑控制器应用了一种新型材料氮化铝( AlN)。工业上在氮气流中由氧化铝与焦炭在高温条件下制得氮化铝,并生成一种可燃性气体,该反应的化学方程式为____。 (6)为探究铁、铜的金属活动性,分别将铁丝、铜丝插入稀硫酸中(图3所示),说明铁比铜的金属活动性更强的实验现象是______,反应的化学方程式是____。 |
|
| 28. | 详细信息 |
阅读下列短文后回答问题:新冠疫情期间,复旦大学华山医院张文宏教授在不同场合说:“早餐要吃鸡蛋牛奶”。鸡蛋营养价值很高,一个重约50 g的鸡蛋,约含7g蛋白质。蛋黄中富含卵磷脂,卵磷脂可以阻止胆固醇和脂肪在血管壁上沉积。一般人群每天吃1~2个鸡蛋不会造成血管硬化,但多吃会增加肝、肾负担。市售鸡蛋常采用三种涂膜保鲜技术,分别是:A—聚乙烯醇溶液涂膜、B—聚乙烯醇和双乙酸钠溶液涂膜、C—聚乙烯醇和氢氧化钙溶液涂膜。三种涂膜剂涂抹于鸡蛋表面 后,在温度为20 ℃、相对湿度为70%的贮藏柜中贮藏30天,测得哈夫单位和蛋黄指数 的变化趋势如下图所示,其中CK是对照组,哈夫单位和蛋黄指数的数值越小,鸡蛋越不新鲜。鸡蛋买回家后,在-1℃、相时湿度80%的条件下储存,最长可以保鲜6个月。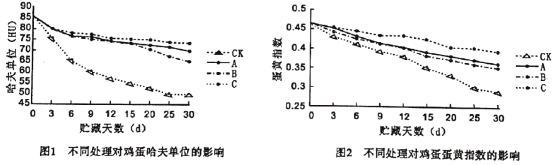 (1)每100 g鸡蛋,约含蛋白质_______g。 (2)用C涂膜保鲜鸡蛋的过程中,发生反应的化学方程式为______。 (3)三种涂膜保鲜技术中,保鲜效果最好的是__________。 (4)在进行涂膜保鲜效果的研究中使用了________实验方法。 |
|
| 29. 填空题 | 详细信息 | |||||||||||||||||||||||||||||
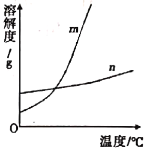
KNO3和KCl在不同温度时的溶解度如下表所示。请回答下列问题:
|
||||||||||||||||||||||||||||||
| 30. 实验探究题 | 详细信息 |
通过对实验室制取气体学习,请结合下图回答问题: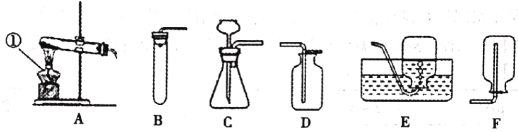 (1)写出标有数字的仪器名称:①___________。 (2)同学们想用高锰酸钾制取一瓶较纯净的氧气,他应选择上述装置中的A和_______(填装置序号)进行组装,而小明认为A装置中还缺少______________;该反应的化学方程式为__________。 (3)同学们在制取CO2实验时,选择发生装置_____(填装置序号)可随时添加液体,用排空气法收集CO2验满的方法是将______的木条放在瓶口。 (4)①如图1是同学们设计的甲、乙、丙一组“吹气球”的实验,请回答:甲装置中,向a中加入一定量水后会看到气球胀大,一段时间内观察到______,说明该装置气密性良好。乙装置中,若锥形瓶中装有水,向锥形瓶加入分液漏斗中的浓硫酸,则气球胀大的主要原因是_______。丙装置中,若锥形瓶中盛满CO2,欲使气球明显胀大,加入分液漏斗中的液体最好是______。 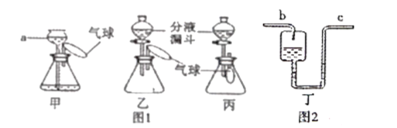 ②如图2装置丁是同学们利用医用输液观察滴液快慢的滴壶,用它作微型洗气装置,请回答:气体应从____(填“b”或“c”)进入,其中所装洗气的液体不能装满的原因是________。 |
|
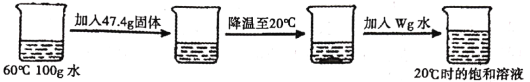
| 31. 流程题 | 详细信息 |
实验室利用反应所得硫酸铜、稀硫酸混合液制备CuSO4·5H2O,其主要流程如图。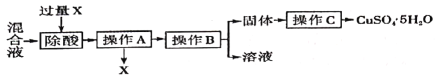 已知:20 ℃时,硫酸铜的溶解度为20.7g 。 (1)试剂X应选用__(填序号)。 a Cu b CuO c Fe (2)操作A为______,操作中所用玻璃仪器有___、玻璃棒、烧杯。 (3)操作B为_____、降温到20℃结晶、过滤。过滤后溶液的溶质质量分数为___。 (结果精确到0.1%) (4)操作C为冰水洗涤、低温干燥,用冰水洗涤的目的; Ⅰ是_________;Ⅱ是__________。 |
|
| 32. 科学探究题 | 详细信息 | ||||||||||||||||||||||||
|
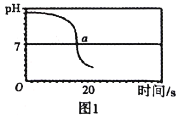
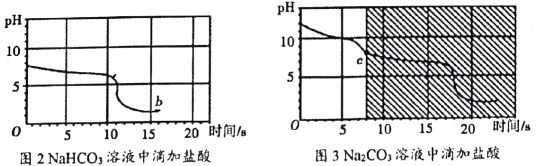
某小组同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行探究。 (提出问题)①三种溶液的酸碱性?②它们与酸反应时溶液的pH如何变化?
|
|||||||||||||||||||||||||