甘肃2019年高二后半期化学期末考试在线免费考试
| 1. 选择题 | 详细信息 | ||||||||||||||||||||
下表所列物质晶体的类型全部正确的一组是
|
|||||||||||||||||||||
| 2. 选择题 | 详细信息 |
|
日常生活中遇到的很多问题都涉及到化学知识,下列有关做法在日常生活中可行的是 A.医用酒精和工业酒精的主要成分相同,都可用于伤口消毒 B.可利用米汤检验含碘盐的真假 C.低血糖症状出现时,吃馒头要比喝葡萄糖水见效快 D.人体对食物中蛋白质的消化其实就是使蛋白质发生了水解 |
|
| 3. 选择题 | 详细信息 |
|
只用一种试剂便可将苯、苯酚、四氯化碳、乙醛4种无色液体进行鉴别,这种试剂是 ①银氨溶液 ②新制的Cu(OH)2悬浊液 ③NaOH溶液 ④溴水 A. 仅①④ B. 仅②③ C. ①②③④ D. 仅①②④ |
|
| 4. 选择题 | 详细信息 |
|
BF3是典型的平面三角形分子,它溶于氢氟酸或NaF溶液中都形成BF4-离子,则BF3和BF4-中的B原子的杂化轨道类型分别是 A. sp2、sp2 B. sp3、sp3 C. sp2、sp3 D. sp、sp2 |
|
| 5. 选择题 | 详细信息 |
|
下列叙述正确的是 A. NH3是极性分子,分子中N原子处在3个H原子所组成的三角形的中心 B. CCl4是非极性分子,分子中C原子处在4个Cl原子所组成的正方形的中心 C. H2O是极性分子,分子中O原子不在2个H原子所连直线的中点处 D. CO2是非极性分子,分子中C原子不在2个O原子所连直线的中点处 |
|
| 6. 选择题 | 详细信息 |
|
以下有关元素性质的说法不正确的是 A. 具有下列电子排布式的原子中:①1s22s22p63s23p2,②1s22s22p3,③1s22s22p2,④1s22s22p63s23p4,原子半径最大的是① B. 具有下列价电子排布式的原子中:①3s23p1,②3s23p2,③3s23p3,④3s23p4,第一电离能最大的是③ C. ①Na、K、Rb,②N、P、As,③O、S、Se,④Na、P、Cl,元素的电负性随原子序数增大而递增的是④ D. 某元素气态基态离子的逐级电离能分别为738、1 451、7 733、10 540、13 630、17 995、21 703,当它与氯气反应时可能生成的阳离子是X3+ |
|
| 7. 选择题 | 详细信息 |
|
关于晶体的下列说法正确的是( ) A. 在晶体中只要有阴离子就一定有阳离子 B. 在晶体中只要有阳离子就一定有阴离子 C. 原子晶体的熔点一定比金属晶体的高 D. 分子晶体的熔点一定比金属晶体的低 |
|
| 8. 选择题 | 详细信息 |
|
下列鉴别方法不可行的是 A. 用水鉴别乙醇、甲苯和溴苯 B. 用燃烧法鉴别乙醇、苯和四氯化碳 C. 用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 D. 用酸性高锰酸钾溶液鉴别苯、环已烯和环已烷 |
|
| 9. 选择题 | 详细信息 |
|
下列说法不正确的是 A. HF、HCl、HBr、HI的热稳定性依次减弱 B. Si、SiC、金刚石的熔点依次降低 C. F2、Cl2、Br2、I2的沸点依次升高 D. HCl的熔、沸点低于HF的熔、沸点 |
|
| 10. 选择题 | 详细信息 |
|
某有机物的分子式为C11H14O2,结构简式中含有一个苯环且苯环上只有一个取代基,与NaHCO3反应有气体生成,则该有机物的结构共有(不含立体异构) A. 9种 B. 10种 C. 11种 D. 12种 |
|
| 11. 选择题 | 详细信息 |
|
下列有关说法中不正确的是 A. 分离硝基苯和苯的混合物通常采用分液法 B. 分子式为C5H10O2且遇小苏打能产生气体的有机物有4种(不考虑立体异构) C. 乙烯和苯的同系物使酸性高锰酸钾溶液褪色的原理均为氧化反应 D. ClCH2CH(CH3)CH2Cl不能通过烯烃与氯气发生加成反应得到 |
|
| 12. 选择题 | 详细信息 |
|
某优质甜樱桃中含有一种羟基酸(用M表示),M的碳链结构无支链,分子式为C4H6O5;1.34 g M与足量的碳酸氢钠溶液反应,生成标准状况下的气体0.448 L。M在一定条件下可发生如下转化:M A. M的结构简式为HOOC—CHOH—CH2—COOH B. B的分子式为C4H4O4Br2 C. 与M的官能团种类、数量完全相同的同分异构体还有2种 D. C物质不可能溶于水 |
|
| 13. 填空题 | 详细信息 |
氯吡苯脲是一种西瓜膨大剂(植物生长调节剂),其组成结构和物理性质见下表。 回答下列问题: (1)氯吡苯脲晶体中,氮原子的杂化轨道类型为________。 (2)氯吡苯脲晶体中,微粒间的作用力类型有________。 A.离子键 B.金属键 C.极性键 D.非极性键 E.配位键 F.氢键 (3)查文献可知,可用2-氯-4-氨吡啶与异氰酸苯酯反应,生成氯吡脲。 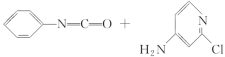  反应过程中,每生成1 mol氯吡苯脲,断裂________个σ键、断裂________个π键。 |
|
| 14. 填空题 | 详细信息 |
|
A+、B+、C-、D、E五种粒子(分子或离子)中,每个粒子均有10个电子,已知: ①A++C- 请回答: (1)C-离子的电子式是________________。 (2)A+离子中的键角为______________。 (3)分别写出A+和D反应、B+和E反应的离子方程式____________、____________。 (4)除D、E外,请再写出两种含10个电子的分子的分子式____________。 (5)除A+、B+外,请再写出两种含10个电子的阳离子________。 |
|
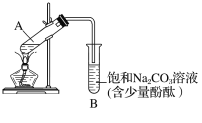
| 15. 实验题 | 详细信息 | ||||||||||||||||||||
已知下列数据:
|
|||||||||||||||||||||
| 16. 综合题 | 详细信息 | ||||||
|
钠、铝是两种重要的金属,其单质及化合物在人们的日常生活、生产及科学研究中具有广泛的用途。回答下列问题: (1)基态铝原子的电子排布图是____________________。 (2)与Al3+具有相同的电子层结构的简单阴离子有__________(填离子符号),其中形成这些阴离子的元素中,电负性最强的是__________(填元素符号,下同),第一电离能最小的是__________。 (3)Al、Cl的电负性如下表:
|
|||||||
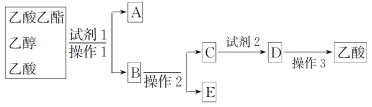
| 17. 推断题 | 详细信息 |
化合物F是一种重要的有机物,可通过以下方法合成: (1)B中含有的官能团名称为_________________。 (2)A→B的化学方程式为_________________。 (3)B→C的反应类型为_________________。 (4)E的分子式为C10H10O4N2,写出E的结构简式:______________________。 (5)写出同时满足下列条件的C的一种同分异构体的结构简式:_______________________。 ①能发生银镜反应;②能发生水解反应,其水解产物之一能与FeCl3溶液发生显色反应; ③分子中只有4种不同化学环境的氢。 (6)已知:CH3CHO+CH3CHO 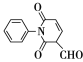 ,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)__________________。 ,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)__________________。 |
|