贵州2019年高三化学上册期末考试网上在线做题
| 1. 选择题 | 详细信息 |
|
下列说法正确的是: A. 煤经过气化和液化等物理变化可转化为清洁燃料 B. 天然植物油常温下一般呈液态,有恒定的熔点、沸点 C. 燃煤中加入CaO可以减少酸雨的形成及温室气体的排放 D. 氯化钠是生活中常见的调味品和防腐剂 |
|
| 2. 选择题 | 详细信息 |
|
NA为阿伏伽德罗常数,下列说法正确的是: A. 标准状况下,11.2LH2O所含分子数大于0.5NA B. 1mol淀粉水解后产生的葡萄糖分子数为NA C. 1LpH=12的氢氧化钡溶液中OH-的数目为0.02NA D. 15gCH3+(碳正离子)中含有电子数为10NA |
|
| 3. 选择题 | 详细信息 |
|
下列叙述不正确的是 A. 蔗糖水解生成的两种有机物互为同分异构体 B. 含有5个碳原子的饱和链烃,其一氯代物有3种 C. 乙烷与氯气在光照下发生反应的产物可能有10种 D. 金刚烷的结构为 |
|
| 4. 选择题 | 详细信息 | |||||||||||||||
下列实验操作、实验现象及日的均正确的是:
|
||||||||||||||||
| 5. 选择题 | 详细信息 |
|
短周期主族元素W、X、Y、Z的原子序数依次增大,Wˉ与X+电子层结构相同,Y所在周期数与族序数相同,Z的最高价氧化物的水化物为强酸。下列说法正确的是: A. 简单离子半径:X>Y>Z>W B. W、Z对应氢化物的沸点:W>Z C. 周期表中Z的氧化物对应水化物的酸性最强 D. 工业上用电解XZ的水溶液制备X单质 |
|
| 6. 选择题 | 详细信息 |
有一种节能的氯碱工业新工艺,将电解池与燃料电池相组合,相关流程如下图所示(电极未标出),下列说法错误的是: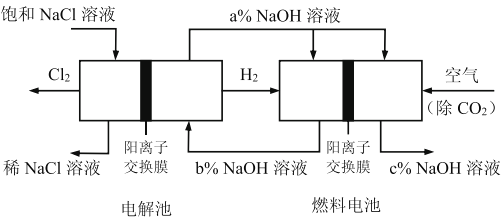 A. 电解池的阴极反应式2H2O+2e-=H2+2OH- B. 相同条件下,当电解池生成2LCl2,理论上燃料电池应消耗1LO2 C. 电解池中阳离子移动流向阴极池 D. 溶液a、b、c的pH大小顺序为:a>b>c |
|
| 7. 选择题 | 详细信息 |
化学上常用AG表示溶液中的酸碱度,AG= A. 点C时溶液存在c(Na+)=c(CH3COO-)>c(OH-)=c(H+) B. 点B时溶液存在2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) C. 25℃时,醋酸的水解常数Kh=10-4.5 D. 点D溶液的pH=11.25 |
|
| 8. 实验题 | 详细信息 | ||||||||||||
|
印刷电路板是由有机复合材料和铜箔复合构成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,研究其制备及性质是一个重要的课题。 (1)氯化铁晶体的制备(夹持及加热装置省略) 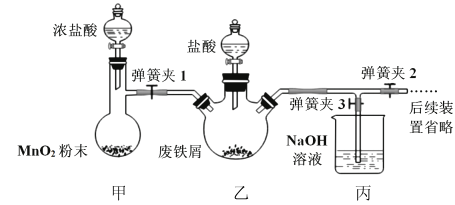 ①实验过程中装置甲中发生反应的离子方程式_________________________________。 ②为顺利达成实验目的,上述装置中甲中活塞、乙中活塞、弹簧夹1、2、3打开和关闭的顺序为__________。 ③反应结束后,将乙中溶液边加入___________,边进行加热浓缩、___________、过滤、洗涤、干燥即得到产品。 (2)氯化铁的性质探究: 已知:①氯化铁的熔点为306℃、沸点为315℃,易升华,气态FeCl3会分解成FeCl2和Cl2②FeCl2熔点670℃) 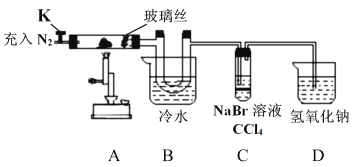
|
|||||||||||||
| 9. | 详细信息 |
无机研究开创绝不无“钴”的时代,例如:CoCl2·6H2O是一种饲料营养强化剂、草酸钴可用于指示剂和催化剂。其中草酸钴的制备可用水钴矿(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO、SiO2等)制取CoC2O4·2H2O工艺流程如下图所示: 已知: ①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等; ②酸性条件下,ClO3-不会氧化Co2+,ClO3-转化为Cl-; (1)浸出过程中加入Na2SO3的主要离子方程式为____________________。 (2)加入 NaClO3发生可以将溶液中Fe2+氧化,进而调节pH除去,但不能向“浸出液”中加过量 NaClO3的主要原因是:__________________。 (3)若“滤液Ⅰ”中c(Ca2+)=1.0×10-3mol·L-1,当除钙率达到99%时,溶液中c(F-)=___________mol/L。[已知Ksp(CaF2)=4.0×10-11] (4)萃取剂对金属离子的萃取率与pH的关系如图1所示,萃取剂的选择的标准是___________;其使用的适宜pH范围是___________(填字母代号)。 A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 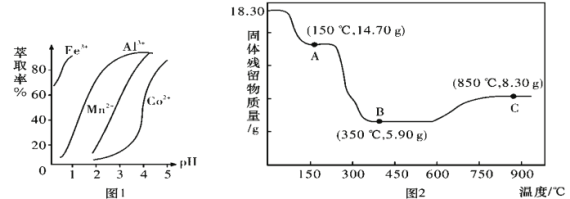 (5)CoC2O4·2H2O热分解质量变化过程如图2所示。其中600℃以前是隔绝空气加热,600℃以后是在空气中加热。A、B、C均为纯净物;用化学方程式表示从A点到B点的物质转化___________。C点所示产物的化学式是___________。(Co的相对原子质量是59) |
|
| 10. 综合题 | 详细信息 |
|
二甲醚制备两种方法原理如下 第一种方法:丹麦Topspe工艺的合成气一步法,是专门针对天然气原料开发的一项新技术。 ①2CH4(g)+O2(g) 第二种方法:二甲醚生产二步法,即先合成甲醇,甲醇在催化剂下制二甲醚。 ②CO(g)+2H2(g) ③2CH3OH(g) (1)若由合成气(CO、H2)直接制备 1molCH3OCH3(g),且生成H2O(1),整个过程中放出的热量为244kJ,则△H2=___________kJ·mol-1。(已知:H2O(1)=H2O(g) △H=+44.0 kJ/mol) (2)下列有关反应①叙述不正确的是___________ a.达到平衡后,升高温度,ν正减少、ν逆增大,平衡逆向移动 b.当四种物质的浓度相等,反应达到化学平衡状态 c.若改变条件,反应物的转化率一定增大,正反应速率一定大于逆反应速率 d.当达到平衡时2v正(O2)=v逆(CH4) e.向该恒容平衡体系中充入氩气,ν正、ν逆均增大,平衡向右移动 (3)有人模拟制备原理Ⅱ,绘制如图甲图像: i说明CO的转化率随温度升高先增大后减小的原因:______________________。 ii.反应②自发进行的条件是______________________。 iii.若在350℃时的2L的密闭容器中充入2 mol CO和6molH2,8min达到平衡,c(CH3OCH3)=0.3mol·L-1,用H2表示反应②的速率是___________;可逆反应③的平衡常数K3=___________。 iv.若350℃时测得容器中n(CH3OH)=n(CH3OCH3),此时反应③v(正)___________ν(逆),说明原因_________。  (4)光能储存一般是指将光能转换为电能或化学能进行储存,利用太阳光、CO2、H2O生成二甲醚的光能储存装置如图乙所示则b极的电极反应式为___________________________。 |
|
| 11. 综合题 | 详细信息 |
|
我国早期科技丛书《物理小识·金石类》写到:“青矾厂气熏人,衣服当之易烂,载木不盛,惟乌柏树不畏其气”,“青矾”则是绿矾,强热时发生如下反应: 2FeSO4·7H2O→Fe2O3+SO3+SO2+7H2O 回答下列问题: (1)基态硫原子的价层电子排布式___________,其最高能级上电子云形状是___________,上述四种元素电负性由大到小的顺序是___________,从结构的角度解释Fe3+稳定性强于Fe2+的原因是__________。 (2)氧、硫能形成许多化合物,如:H2O、SO2、SO3、SO42-,这些物质的中心原子杂化轨道类型为SP2的是___________,空间构型是V形的分子是___________,属于非极性分子的是___________。 (3)已知Fe2O3熔点为1565℃,在熔化状态下液体中存在两种粒子,则其晶体类型最可能是___________,若FeO与Fe2O3晶体类型相同,则二者熔点较高的物质是___________。 (4)铁的某种氧化物晶胞如图所示(实心球为铁原子);  ①该氧化物的化学式为___________。 ②氧、铁的原子半径分别为rO pm、rFe pm,晶体密度为ρg·cm-3,阿伏伽德罗常数的值为NA,该晶胞的空间利用率为___________(用含π的式子表示) |
|
| 12. 推断题 | 详细信息 |
2018年8月3日我国确诊首例非洲猪瘟疫情。10月25日,农业农村部新闻办公室发布,贵州省毕节市发生非洲猪瘟疫情。目前最有效的药物要主要成分的一种合成路线如图所示: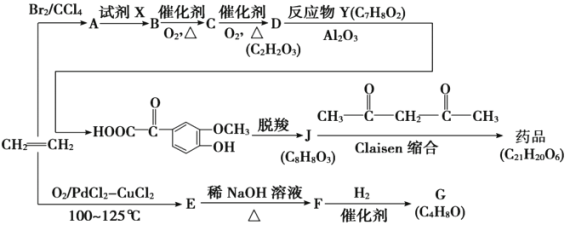 已知: ①E、G能发生银镜反应 ②R—CHO+R′—CH2—CHO  (R、R表示烃基或氢)。 (R、R表示烃基或氢)。请回答下列问题: (1)G的名称是____________________;D中所含官能团的名称是____________________。 (2)Y的结构简式为__________________;A生成B的反应类型是__________________。 (3)据最新报道,乙烯与双氧水在催化剂作用下反应生成B,产率较高。写出该反应的化学方程式____________________________________________。 (4)简述逐一检测出F中官能团的实验操作与现象结论______________________。 (5)在J的同分异构体中,同时满足下列条件的同分异构体有___________种。 i.既能发生水解反应,又能发生银镜反应; ii.遇氯化铁溶液发生显色反应。 (6)参照上述流程,以苯乙烯为原料,设计路线制备某药物中间体 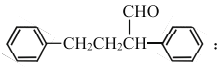 _________________________________。 _________________________________。 |
|
最近更新



