2019年高三上册第一次质检化学在线测验完整版(陕西省西安市长安一中)
| 1. 选择题 | 详细信息 |
|
化学与工农业生产、日常生活、材料等有密切的联系,下列说法正确的是( ) A.华为公司自主研发的“麒麟970芯片需要以高纯度的二氧化硅为原料 B.笔、墨、纸、砚为传统的文房四宝,上述物质中的(毛)笔与(宣)纸均含有机物 C.电影《红高梁》中用高粱酿酒的原理是通过蒸馏法将高梁中的乙醇分离出来 D.有机高分子明星材料石墨烯,具有优异的光学、电学、力学和热学性质 |
|
| 2. 选择题 | 详细信息 |
|
常温下,下列各组离子在指定溶液中一定能大量共存的是( ) A.氨水的饱和溶液中:Ca2+、NH4+、Cl-、HCO3- B.0.1mol͘·L-1的AlCl3溶中:Na+、Mg2+、CO32-、NO3- C.漂白粉的溶液中:Ba2+、K+、OH-、I- D.通入过量CO2的溶液中:Na+、NH4+、Cl-、SO42- |
|
| 3. 选择题 | 详细信息 |
|
正确掌握化学用语是学好化学的基础,下列化学用语中正确的是( ) A.硫酸铁铵的化学式:(NH4)2Fe(SO4)2 B.乙醚的分子式C2H4O C.苯乙烯的结构简式: D.四氯化碳分子的比例模型: |
|
| 4. 选择题 | 详细信息 |
|
下列物质性质与应用对应关系不正确的是( ) A.浓硝酸、浓盐酸均为易挥发的强酸,两者混合配成的“王水”具有强腐蚀性 B.浓氨水具有挥发性,可用于检验运送氯气的管道是否发生泄露 C.石墨具有导电性、稳定性,可用作电极材料 D.氯化铝是电解质,可以用于电解法冶炼金属铝 |
|
| 5. 选择题 | 详细信息 |
|
NA为阿伏伽德罗常数的值。下列说法正确的是( ) A.一定条件下,3molH2和1molN2充分反应后,可得2NA个NH3分子 B.室温下,1LpH=1的HCl溶液中,由水电离的H+数目为0.1NA C.0.1mol金属Na在空气中完全氧化生成Na2O和Na2O2,转移的电子数为0.1NA D.1mol/L的NaCN溶液中含CN-和HCN的数目之和为NA |
|
| 6. 选择题 | 详细信息 |
|
在实验室制备并收集纯净、干燥的氨气的过程中,下列装置一定不需要的是 ( ) A.  B.  C. D.  |
|
| 7. 选择题 | 详细信息 |
异丁烯与氯化氢可能发生的两种加成反应及相应的能量变化与反应过程如下图所示,下列说法错误的是( )  A.活化能:反应①大于反应② B.中间产物的稳定性:中间体1小于中间体2 C.产物的能量:产物1大于产物2 D.△H大小:反应①小于反应② |
|
| 8. 选择题 | 详细信息 |
一种从废弃钛酸锂电极材料[含Li4Ti5O12、铝箔、碳粉、PVDF(聚偏二氟乙烯)]中回收某些资源的流程如下: 已知:Li4Ti5O12+7H2SO4+5H2O2=2Li2SO4+5[TiO(H2O2)]SO4+7H2O,下列叙述错误的是() A.步骤的目的是除去碳粉与PVDF B.步骤H2O2的作用是氧化剂 C.从该电极材料中可回收的金属元素有Al、Ti、Li D.合理处理废旧电池,有利于环境保护和资源再利用 |
|
| 9. 选择题 | 详细信息 |
某烃的含氧衍生物的球棍模型如图所示(图中球与球之间连线代表化学键单键或双键)。下列关于该有机物的说法正确的是( ) A.该有机物的名称是乙酸乙酯 B.该有机物能使Br2的CCl4或酸性高锰酸钾褪色,原理相同 C.该有机物能发生取代反应、氧化反应和消去反应 D.该有机物的同分异构体中能与NaHCO3反应产生气体的链状结构只有3种 |
|
| 10. 选择题 | 详细信息 |
|
用惰性电极电解1.0 L c(Cl-)=3.0 mol/L的CuCl2、NaCl混合溶液,一段时间后,两极均收集到56.0 L的气体(标准状况下)。下列说法正确的是( ) A.阳极只收集到Cl2 B.电解前溶液呈弱酸性,电解结束后,溶液的酸性增强 C.整个过程中共转移电子5 mol D.原混合溶液中c(Cu2+)=1.0 mol/L |
|
| 11. 选择题 | 详细信息 |
|
已知化合物K2S2O8、CrO5中的硫与铬元素的化合价均为+6,则K2S2O8、CrO5中含有的过氧键(—O—O—)个数分别为( ) A.1个,1个 B.1个,2个 C.2个,1个 D.2个,2个 |
|
| 12. 选择题 | 详细信息 |
|
甲,乙两烧杯中各盛有500ml,相同浓度的盐酸和氢氧化钠溶液。向两个烧杯中分别加入18.0g的铝粉,反应结束后,测得生成的气体体积比为甲:乙=1:2,则下列说法正确的是 ①甲烧杯中盐酸不足。 ②乙烧杯中金属铝过量。 ③甲烧杯中生成的气体体积为11.2L ④乙烧杯中的c(NaOH)=2mol/L A.①③ B.①④ C.②③ D.②④ |
|
| 13. 选择题 | 详细信息 |
|
在给定的条件下,下列选项所示的物质间转化均能一步实现的是( ) A.SiO2 B.HClO C.Cu2(OH)2CO3 D.Al |
|
| 14. 选择题 | 详细信息 | ||||||||||||||||||||
下列实验中,对应的现象以及结论都正确,且两者具有因果关系的是( )
|
|||||||||||||||||||||
| 15. 选择题 | 详细信息 |
AG表示溶液酸度: A.0.1mol/L的 CH3COOH溶液的pH=3 B.m点加入NaOH的体积为25mL C.若pH=7,则溶液中水电离的c(OH-)=1.0×10-3.5 mol/L D.随着NaOH溶液滴入,溶液中水的电离程度逐渐增大,m点最大 |
|
| 16. 选择题 | 详细信息 |
|
W、X、Y、Z是原子序数依次增大的四种短周期主族元素,其中X为唯一的金属元素,其单质在空气中易形致密的稳定氧化膜;Y、Z、W族序数依次增大,Y的单质在空气中易发生自燃。下说法不正确的是( ) A.Y、Z均能形成不止一种氧化物 B.工业上获得X单质的主要方法是电解其熔融的氧化物 C.气态氢化物的稳定性:W>Z>Y D.W、X形成的化合物中一定是阴离子半径大于阳离子 |
|
| 17. 综合题 | 详细信息 |
汽车等机动车尾气,含(CO、NO等)是城市空气的污染源。利用NSR技术可有效降低CO、NO的排放,回答有关问题: I.CO、NO的检测 (1)O2-的移动方向为__________。(填“向Pt电极”或“向NiO电极”) (2)NiO电极上的电极反应为___________和__________。 II.NSR处理技术 NO的储存和还原在不同时段交替进行,实现两种有害气体,同时被处理,工作如图所示。 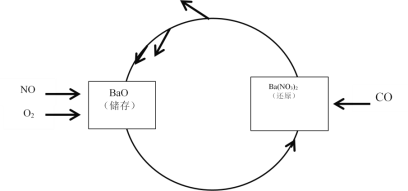 (3)已知:N2(g)+O2(g)=2NO(g) ΔH=+180.5 kJ/mol ① 2CO(g)+O2(g)=2CO2(g) ΔH=-566.0 kJ/mol ② 则NSR技术工作原理的热化学方程式:2CO(g)+2NO(g)=N2(g)+2CO2(g)③的ΔH=________ (4)在一定温度下,向2L恒容密闭容器中充入等物质的量的NO和CO,发生反应,反应过程中c(NO)随时间的变化曲线如图所示。  ①图中曲线a或b中表示在该温度下使用NSR催化技术的是__________。 ②曲线b中前10min内CO的平均反应速率v(CO)=_________;此温度下该反应的平衡常数K为_______。若平衡后,再向容器中充入CO和N2各0.8mol,则此时v(正)_____ v(逆)(填“>”、“<”或“=”)。 ③若保持其他条件不变,15min时将容器的体积压缩至1L,20min时反应重新达到平衡,NO的物质的量浓度对应的点可能是____点。(填字母) |
|
| 18. | 详细信息 |
镁是一种重要金属,号称国防金属。某设计小组利用硼镁矿制备镁和硼的流程如下: 已知:硼镁矿的主要成分Mg2B2O5·H2O,硼砂的化学式为Na2B4O7·10H2O,回答下列问题: (1)Mg2B2O5·H2O中B的化合价为________。在90℃的热水中,加入稀硫酸调节pH=2~3生成硼酸(H3BO3),反应的离子方程式为__________。 (2)硼的化合物种类繁多,NaBH4是有机合成中常见的还原剂,NaBH4的电子式为______。 (3)将MgCl2·6H2O置于HCl氛围中加热的目的是_____,Mg与X在高温下反应的化学方程式为________。 (4)若向硼镁矿中加入0.1 mol/L盐酸溶液,充分反应后测得溶液的pH=2时,溶液中c(Mg2+)为__________________________________(忽略溶液体积的变化)。 (5)电解熔融的无水氯化镁所得的镁蒸汽在特定的环境里冷却后即为固体镁,下列物质中可以作镁蒸汽的冷却剂的是_________(填字母序号) A氦气 B氮气 C水蒸气 D二氧化碳气体 E氯气 (6)Mg-H2O2是一种以海水为电解质(加入一定量的酸)的新型电池。该电池的负极材料为_____,正极的电极反应为________。 |
|
| 19. 实验题 | 详细信息 |
|
FeCl3为黑棕色固体,无水氯化铁在300℃以上升华,遇潮湿空气极易潮解。 (1)甲组同学拟用下列装置制取纯净干燥的氯气。 ①装置B的作用是_________ ②装置A中发生反应时消耗的氧化剂和还原剂的物质的量之比为__________ (2)乙组同学选用甲组实验中的装置ABC和下列装置制取FeCl3  ①乙组同学的实验装置中,依次连接的合理顺序为:a→_____→_____→_____→_____→_____→_____ ②连好装置,检查装置的气密性,先打开装置A中___________(填仪器的名称)的活塞,直到______再点燃装置F处的酒精灯,目的是_______ ③装置D的作用有_______ (3)实验结束后,取少量F中的固体加水溶解,欲对所得产物FeCl3中是否含有FeCl2进行检测,所需试剂是_______ a.KSCN b.H2O2 c.K3[Fe(CN)6] d. .K4[Fe(CN)6] 经检测发现溶液中含有Fe2+,丙同学认为所得产物FeCl3中一定含有FeCl2,丁同学认为不一定,理由是_____ |
|
| 20. 综合题 | 详细信息 |
|
硅及其化合物在材料领域中应用广泛。回答下列问题: (1)硅单质有晶体硅和无定形硅两种,区别晶体硅和无定形硅的科学方法是___________ (2)基态硅的价电子排布式为_________,其核外电子的运动状态有_____种。 (3)CCl4和SiCl4常温下均呈液态,SiCl4熔沸点较高的原因为________CCl4不水解,但SiCl4遇水即强烈水解,则SiCl4水解的化学方程式为__________。 (4)SiF4的热稳定性比SiCl4强的原因是 ____。 (5)碳化硅(SiC)的结构与金刚石类似,碳化硅的硬度仅次于金刚石,其晶胞结构如图所示。则Si原子的配位数为_______,若晶体的密度为ρg/cm3 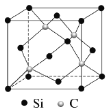 |
|
| 21. 推断题 | 详细信息 |
某相对分子质量为40的链状不饱和烃A,能发生如下转化: 已知:①羟基所连接的碳原子上无氢原子时,难以发生催化氧化;②E能与NaHCO3溶液反应产生气体;③F为酯类化合物。 (1)A的分子式为_____________,A转化为B的反应类型为______________,C转化为D的反应条件为_________________。 (2)B中所含有的官能团的名称为_____________,B中共平面的原子最多有________个。 (3)写出D转化为E的化学方程式:__________________ (4)与E互为同分异构体的芳香族化合物K,已知:①K与E具有相同的官能团;②K不能与FeCl3溶液发生显色反应;③K有二个取代基,则符合上述条件的K共有_________。(填字母代号) a.3种 b.6种 c. 9种 d.12种 (5)F的结构简式为_________________________。 |
|
最近更新



