天津市高三化学下册月考试卷考题同步训练
| 1. 选择题 | 详细信息 |
|
化学与社会、生产、生活密切相关。下列说法正确的是 A.石英只能用于生产光导纤维 B.复旦大学研究的能导电、存储的二维材料二硫化钼是一种新型有机功能材料 C.中国歼—20上用到的氮化镓材料是当作金属合金材料使用的 D.医用双氧水和酒精均可用于伤口清洗,两者消毒原理不相同 |
|
| 2. 选择题 | 详细信息 |
|
下列化学用语对事实的表述正确的是 A.硬脂酸与乙醇的酯化反应:C17H35COOH+C2H518OH B.向Na2SiO3溶液中通入过量的SO2:SiO32-+SO2+H2O=H2SiO3↓+SO32- C.由Na和C1形成离子键的过程: D.已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量CO2:2ClO-+CO2+H2O=2HClO+CO32- |
|
| 3. 选择题 | 详细信息 |
|
下列说法中不正确的是 A.N2分子有一个δ键,两个键 B.δ键比π键重叠程度大,形成的共价键强 C.电子排布图 D.气体单质中,一定有δ键,可能有π键 |
|
| 4. 选择题 | 详细信息 |
根据侯氏制碱原理制备少量NaHCO3的实验,经过制取氨气、制取NaHCO3、分离NaHCO3、干燥NaHCO3四个步骤,下列图示装置和原理能达到实验目的的是 |
|
| 5. 选择题 | 详细信息 |
|
下列与化学有关说法中正确的是( ) A. B. lmol碳酸钾晶体中含阴离子数为等于NA个 C. 分子式为C4H8O2的羧酸共有3种 D. 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+3H2O |
|
| 6. 选择题 | 详细信息 | |||||||||||||||||||||||||||
利用右图所示装置进行下列实验,能得出相应实验结论的是( )
|
||||||||||||||||||||||||||||
| 7. 选择题 | 详细信息 |
CO2是重要的温室气体,对地球温室效应的“贡献”最大,如何利用CO2是摆在科技工作者面前的重要课题。如图所示电解装置可将CO2 转化为乙烯,该装置的电解质溶液为强酸性水溶液,电极材料为惰性电极。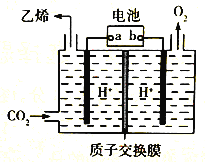 下列有关说法正确的是 A. a为电池的正极 B. 电解过程中H+移向阳极 C. 反应前后溶液的pH保持不变 D. 阴极反应式:2CO2+12H++12e-=C2H4+4H2O |
|
| 8. 选择题 | 详细信息 |
|
下列说法正确的是 A.反应A(g) ⇋ 2B(g) △H,若正反应的活化能为Ea kJ/mol,逆反应的活化能为Eb kJ/mol,则△H=-( Ea- Eb)kJ/mol B.常温下,pH相同的NaOH溶液和Ba(OH)2溶液中,水的电离程度相同 C.某温度氯化钠在水中的溶解度是20 g,该温度饱和氯化钠溶液的质量分数为20% D.将浓度为0.1 mol/L HF溶液加水不断稀释过程中,电离平衡常数Ka(HF)保持不变,始终保持增大 |
|
| 9. 选择题 | 详细信息 |
|
下列说法正确的是 A. 锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除去 B. 可采取加热蒸发的方法使FeCl3从水溶液中结晶析出 C. NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 D. 将SO2分别通入硝酸钡溶液和溶有氨气的氯化钡溶液中,产生沉淀的成分相同 |
|
| 10. 选择题 | 详细信息 |
|
常温下,电解质溶液的性质与变化是多样的,下列说法正确的是( ) A. pH相同的①CH3COONa ②NaClO ③NaOH三种溶液c(Na+)大小:①>②>③ B. 往稀氨水中加水, C. pH=4的H2S溶液与pH=10的NaOH溶液等体积混合,存在下列等式:c(Na+)+c(H+)c=(OH—)+2c(S2—) D. Ca(ClO)2溶液中通入少量CO2,ClO—水解程度增大,溶液碱性增强 |
|
| 11. 综合题 | 详细信息 |
|
Ⅰ.饮用水中含有砷会导致砷中毒,水体中溶解的砷主要以As(Ⅲ)亚砷酸盐和As(Ⅴ)砷酸盐形式存在。 (1)砷与磷为同一主族元素,砷的原子序数为________________。 (2)根据元素周期律,下列说法正确的是__________________。 a.酸性: H2SO4>H3PO4>H3AsO4 b.原子半径:S>P>As c.非金属性:S>P>As (3)关于地下水中砷的来源有多种假设,其中一种认为是富含砷的黄铁矿(FeS2)被氧化为Fe(OH)3,同时生成SO42-,导致砷脱离矿体进入地下水。FeS2被O2氧化的离子方程式为______。 Ⅱ.(4)A、B、C、X是中学化学常见的物质,A、B、C均由短周期元素组成,转化关系如图:  若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,将A、C的水溶液混合可得B的白色胶状沉淀。 ①A中含有的金属元素为________(写元素名称),它在周期表中的位置为______。 ②该金属元素的单质与某氧化物在高温下反应,常用于焊接铁轨及定向爆破,该反应的化学方程式为________。 Ⅲ.铁及其化合物在生活中有广泛应用。 (5)Fe3+基态核外电子排布式为______。 (6)氮化铁晶体的晶胞结构如图所示。该晶体中铁、氮的微粒个数之比为______。  (7)某铁的化合物结构简式如图所示:  ①上述化合物中所含有的非金属元素的电负性由大到小的顺序为______(用元素符号表示)。 ②上述化合物中氮原子的杂化方式为______。 |
|
| 12. 综合题 | 详细信息 |
在碱的作用下,两分子酯缩合形成β—羰基酯,同时失去一分子醇,该反应称克莱森(R·L·Claisen)酯缩合反应,其反应机理如下:2RCH2COOC2H5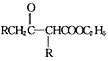 +C2H5OH。利用Claisen反应制备化合物H的一种合成路线如下: +C2H5OH。利用Claisen反应制备化合物H的一种合成路线如下: 回答下列问题: (1)A的名称为__________,C的结构简式为__________。 (2)F中含氧官能团的名称是__________;反应Ⅱ的反应类型是__________。 (3)E→F反应的化学方程式为_________________________________。 (4)B的含有苯环的同分异构体有_____________种(B自身除外),其中核磁共振氢谱显示3组峰的结构简式为__________、__________。 (5)乙酰乙酸乙酯( |
|
| 13. | 详细信息 |
通过沉淀-氧化法处理含铬废水,减少废液排放对环境的污染,同时回收K2Cr2O7。实验室对含铬废液(含有Cr3+、Fe3+、K+、SO42-、NO3-和少量Cr2O72-)回收与再利用工艺如下: 已知:①Cr(OH)3 + OH- = CrO2- + 2H2O; ②2CrO2- + 3H2O2 + 2OH- = 2CrO42- + 4H2O; ③H2O2在酸性条件下具有还原性,能将+6价Cr还原为+3价Cr。 (1)如图是用KOH固体配制250mL 6 mol·L-1 KOH溶液的过程示意图。 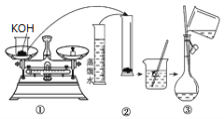 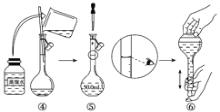 ①请你观察图示判断,其中不正确的操作有(填序号)________; ②其中配制250 mL溶液的体积容器是(填名称)_________________; ③如果用图示的操作配制溶液,所配制的溶液浓度将________(填“偏大”或“偏小”)。 (2)滤液Ⅰ酸化前,进行加热的目的是_________________。冰浴、过滤后,应用少量冷水洗涤K2Cr2O7,其目的是_______。 (3)称取产品重铬酸钾试样2.000g配成250mL溶液,取出25.00mL于锥形瓶中,加入10mL 2mol·L-1H2SO4和足量碘化钠(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL 淀粉指示剂,用0.1200 mol·L-1Na2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)。 ①写出重铬酸钾氧化碘化钠的离子方程式_________。 ②滴定终点的现象为_________。 ③若实验中共用去Na2S2O3标准溶液30.00mL,所得产品中的重铬酸钾的纯度为_________(设整个过程中其它杂质不参与反应)。 ④若滴定管在使用前未用Na2S2O3标准溶液润洗,测得的重铬酸钾的纯度将_____________(填“偏高”、“偏低”或“不变”)。 |
|
| 14. 综合题 | 详细信息 |
|
Ⅰ.含氮化合物在工农业生产中都有重要应用。 (1)氨和肼(N2H4)是两种最常见的氮氢化物。 己知:4NH3(g)+3O2(g)⇌2N2(g)+6H2O(g) ΔH1=-541.8kJ/mol,化学平衡常数为K1。N2H4(g)+O2(g)⇌N2(g)+2H2O(g) ΔH2=-534kJ/mol,化学平衡常数为K2。则用NH3和O2制取N2H4的热化学方程式为___________,该反应的化学平衡常数K=__________(用K1、K2表示)。 (2)对于2NO(g)+2CO(g)⇌N2(g)+2CO2(g),在一定温度下,于1L的恒容密闭容器中充入0.1molNO和0.3molCO,反应开始进行。 ①下列能说明该反应已经达到平衡状态的是____________(填字母代号)。 A.c(CO)=c(CO2) B.容器中混合气体的密度不变 C.v(N2)正=2v(NO)逆 D.容器中混合气体的平均摩尔质量不变 ②图为容器内的压强(P)与起始压强(P0)的比值(P/P0)随时间(t)的变化曲线。0~5min内,该反应的平均反应速率v(N2)= _____________,平衡时NO的转化率为______________。(已知气体的压强比等于其物质的量之比)  (3)使用间接电化学法可处理燃煤烟气中的NO,装置如图所示。已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式________________。  Ⅱ.采用氨水吸收烟气中的 SO2 若氨水与 SO2恰好完全反应生成正盐,则此时溶液呈_________性(填“酸”或“碱”)。 常温下弱电解质的电离平衡常数如下:氨水:Kb=1.8×10-5mol•Lˉ1;H2SO3 : Ka1=1.3×10-2mol•Lˉ1,Ka2=6.3×10-8mol•Lˉ1 |
|
最近更新




