2020年上海市中考化学模拟专题训练
| 1. 选择题 | 详细信息 |
|
属于化学变化的是( ) A.食物腐败 B.打磨宝石 C.矿石粉碎 D.河水结冰 |
|
| 2. 选择题 | 详细信息 |
|
生活中的“水”属于纯净物的是 A.天然水 B.自来水 C.蒸馏水 D.矿泉水 |
|
| 3. 选择题 | 详细信息 |
|
拉瓦锡用定量的方法研究空气成分时用到的反应物是( ) A.红磷 B.白磷 C.铜 D.汞 |
|
| 4. 选择题 | 详细信息 |
|
焰色反应火焰呈黄色的是( ) A.KNO3 B.MgO C.CuCl2 D.NaCl |
|
| 5. 选择题 | 详细信息 |
|
属于溶液的是( ) A.豆浆 B.冰水 C.牛奶 D.雪碧 |
|
| 6. 选择题 | 详细信息 |
|
84消毒液中有效成分为次氯酸钠NaClO,其中氯元素的化合价为 A.0 B.-1 C.+1 D.+2 |
|
| 7. 选择题 | 详细信息 |
|
下列实验操作正确的是 A. 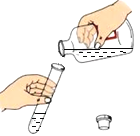 倾倒液体药品 B. 倾倒液体药品 B. 取用固体药品 C. 取用固体药品 C.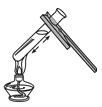 加热液体 加热液体 |
|
| 8. 选择题 | 详细信息 |
|
下图白球代表氢原子,黑球代表氦原子,表示等质量氢气与氦气的混合气体是 A. 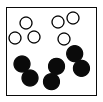 B. B.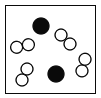 C. C.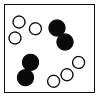 D. D.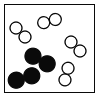 |
|
| 9. 选择题 | 详细信息 |
|
物质的用途既与化学性质有关又与物理性质有关的是( ) A.食盐:融雪剂 B.金刚石:切割玻璃 C.盐酸:除铁锈 D.二氧化碳:灭火 |
|
| 10. 选择题 | 详细信息 |
|
互为同素异形体的物质一定是 A.化学式不同 B.结构不同 C.性质相同 D.式量相同 |
|
| 11. 选择题 | 详细信息 |
|
物质的组成中一定不含氢元素是( ) A.酸性氧化物 B.酸 C.碱 D.盐 |
|
| 12. 选择题 | 详细信息 |
|
硫在氧气中燃烧是化学变化,判断的依据是( ) A.产生蓝紫色的火焰 B.产生大量的热 C.块状的硫磺逐渐消失 D.有刺激性气味的气体产生 |
|
| 13. 选择题 | 详细信息 |
|
相关说法正确的是 A. 尘土飞扬,说明分子是不断运动的 B. 水通电生成氢气和氧气,说明分子是可分的 C. 热胀冷缩,说明微粒的大小随温度的变化而变化 D. 碳酸分解前后原子的种类不变,说明原子是不可分的 |
|
| 14. 选择题 | 详细信息 |
|
符合事实且化学方程式书写正确的是( ) A.用硝酸银溶液鉴别稀盐酸和稀硫酸:AgNO3+HCl═AgCl↓+HNO3 B.铁与盐酸反应制取氢气:2Fe+6HCl═2FeCl3+3H2↑ C.正常雨水 pH 值约为 5.6 的原因:CO2+H2O═H2CO3 D.点燃法除去 CO2 中混有少量的 CO:2CO+O2 |
|
| 15. 选择题 | 详细信息 | ||||||||||
室温时几种物质的溶解度如表所示。室温下向 396g 硝酸钾饱和溶液中投入 20g 食盐,下列推断正确的是( )
|
|||||||||||
| 16. 选择题 | 详细信息 |
|
有关概念的叙述正确的是( ) A.能与酸反应的氧化物一定是碱性氧化物 B.均一、稳定、澄清的液体一定是溶液 C.反应物只有一种的化学反应一定是分解反应 D.元素存在形态发生改变的反应一定是化学变化 |
|
| 17. 选择题 | 详细信息 |
|
气体X可能含有氢气、一氧化碳和二氧化碳中的一种或几种。将气体X依次通过灼热氧化铜和澄清石灰水,观察到黑色固体变红、澄清石灰水变浑浊,气体X组成的可能性有( ) A. 2种 B. 3种 C. 4种 D. 5种 |
|
| 18. 选择题 | 详细信息 |
|
下列各组物质的溶液,只需组内物质相互反应就能区别的是( ) A.Ba(OH)2、Na2SO4、MgCl2、HCl B.BaCl2、K2SO4、Na2CO3、KOH C.FeCl3、HNO3、NaCl、NaOH D.H2SO4、KCl、ZnCl2、CuCl2 |
|
| 19. 选择题 | 详细信息 |
甲、乙、丙是初中化学中常见的物质,图中“﹣”表示相连的物质之间能发生反应,“→”表示由一种物质转化为另一种物质。说法错误的是( )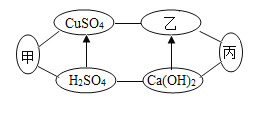 A.甲可能是金属 B.丙可能是氧化物 C.乙和丙反应可能是化合反应 D.乙与硫酸铜溶液反应可能生成两种沉淀 |
|
| 20. 填空题 | 详细信息 |
|
绿水青山,就是金山、银山,化学绿色化是我们共同的责任。 ①垃圾分类:剩饭、剩菜属于_____(填“干垃圾”或“湿垃圾”); ②植物光合作用可表示为:6H2O+6CO2  X+6O2,该反应涉及的物质中,造成温室效应的气体是_____,其中X的化学式是_____,X物质类别属于_____(填“酸”、“碱”、“盐”、“氧化物”或“有机物”)。 X+6O2,该反应涉及的物质中,造成温室效应的气体是_____,其中X的化学式是_____,X物质类别属于_____(填“酸”、“碱”、“盐”、“氧化物”或“有机物”)。③酒精(C2H5OH))是杀灭新型冠状病毒的主要消毒剂之一,其摩尔质量为_____,0.1mol酒精约含_____个氢原子,含碳元素的质量是_____g。 |
|
| 21. 填空题 | 详细信息 |
甲、乙两种固体物质的溶解度曲线如图.回答下列问题: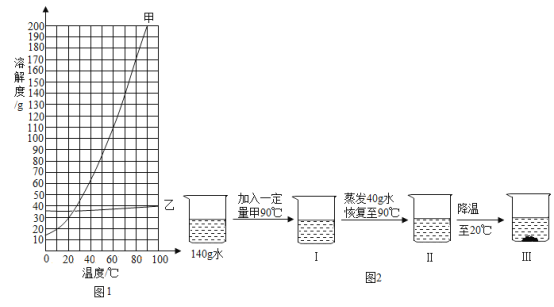 ①在10℃时,甲、乙两种物质的溶解度大小关系为_____。 ②某温度下,将甲的不饱和溶液转化为饱和溶液的方法之一是_____。 ③甲物质中含有少量乙物质时,提纯甲的方法是_____。 ④取一定量的甲物质和水进行如图2所示操作:若Ⅲ中析出116g固体(不含结晶水),则加入甲的质量是_____g; 下列对上述过程的分析正确的是_____。 A Ⅰ中溶液为不饱和溶液 B Ⅱ中溶液可能是饱和溶液 C 开始析出固体甲的温度在 70℃至 80℃之间 D 烧杯中溶液的溶质质量分数是Ⅱ>Ⅲ>Ⅰ |
|
| 22. 科学探究题 | 详细信息 |
|
同学们在实验室完成实验探究后得到废液 A,其中含有稀硫酸、硫酸亚铁和硫酸铜。老师将同学们分成甲乙两组,继续进行如下实验,请完成相关问题: (甲组任务)将废液转化成硫酸亚铁晶体。实验流程如图1: 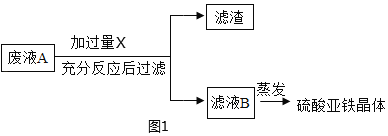 ①实验流程中X 是_____(写物质名称),过量的目的是_____,反应现象是_____,写出一个涉及的化学方程式是_____,该反应的基本类型_____。 (乙组任务)利用废液来探究金属铝的化学性质。实验流程如图2: 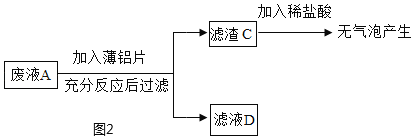 ②滤渣 C 中一定没有_____。 ③滤液 D 中一定含有的溶质是_____(填化学式,下同),可能含有的溶质是_____。 |
|
| 23. 科学探究题 | 详细信息 |
|
某化学兴趣小组利用下列实验来探究 CO2气体的制取和性质。 Ⅰ.实验室制取CO2气体。 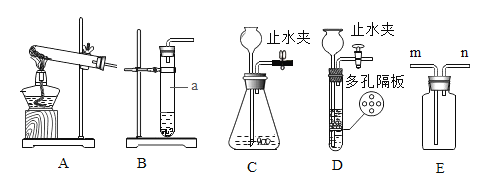 ①仪器a的名称是_____。 ②用于实验室制取CO2的发生装置是_____(填编号),收集CO2应与E 的_____处连接(选填“m”或“n”)。 ③利用C装置制取气体时,反应未停止前关闭止水夹,可观察到的现象是_____。 ④D装置作气体发生装置的适用范围是_____;与B装置相比,利用D装置制取气体的优点是_____。 ⑤用块状的石灰石与过量稀盐酸反应制取CO2,若参加反应的石灰石的纯度80%,质量为125g,则反应生成 CO2 的物质的量为_____mol(根据化学方程式列式计算); Ⅱ.探究CO2的性质。实验步骤如下: 步骤 1:如图1所示装置的气密性良好(图中 a 处连接气体压力传感器),甲、乙、丙三个烧瓶的容积均为250mL,分别收集满CO2,三个注射器内各装有85mL液体。 步骤 2:三位同学同时迅速将注射器内液体全部注入各自烧瓶中,关闭活塞;一段时间后,同时振荡烧瓶。 步骤 3:利用“数字化实验”测定烧瓶内的气压变化,得到如图2所示的烧瓶内压强与时间的关系曲线图,曲线 1、2、3分别表示甲、乙、丙三个烧瓶内的气压变化。 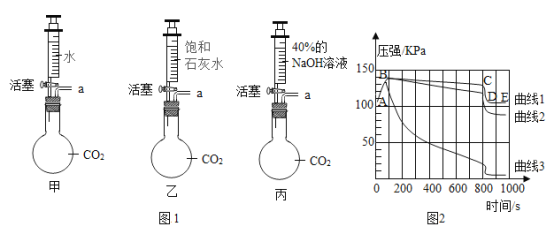 ①实验过程中,观察到烧瓶乙中有白色沉淀生成,该反应的化学方程式_____。 ②图 2中AB段气压快速增大的原因是_____; 曲线1中导致CD段气压快速变小的操作是_____。 ③对比曲线 1 与曲线3,能得出的结论是_____(填序号)。 a CO2能溶于水 b CO2能与水发生反应 c CO2能与NaOH溶液发生反应 ④对比曲线2与曲线3,造成气压变化差异大的主要原因是_____。 |
|
| 24. 流程题 | 详细信息 | ||||||||||||||||||||
K2CO3和KNO3在不同温度时的溶解度如下。
|
|||||||||||||||||||||
最近更新