2019-2020年高一下册5月复学线上教学诊断性考试化学题免费试卷(福建省福州市长乐高级中学)
| 1. 选择题 | 详细信息 |
|
据报载我国最近合成新的同位素,其中一种是 A.72 B.113 C.185 D.257 |
|
| 2. 选择题 | 详细信息 |
|
下列燃料中最理想的燃料是 A.煤 B.石油 C.天然气 D.氢气 |
|
| 3. 选择题 | 详细信息 |
|
下列气态氢化物中,最稳定的是 A.NH3 B.H2O C.HCl D.HF |
|
| 4. 选择题 | 详细信息 |
|
对Na、Mg、Al的有关性质的叙述正确的是 A.碱性:NaOH>Mg(OH)2>Al(OH)3 B.原子半径:Na<Mg<Al C.离子半径:Na+<Mg2+<Al3+ D.单质的还原性:Al>Mg>Na |
|
| 5. 选择题 | 详细信息 |
如图是元素周期表的一部分,下列说法中正确的是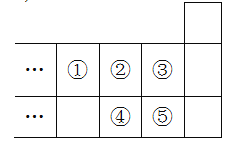 A.最高价氧化物对应水化物酸性:⑤>④ B.气态氢化物的稳定性:④>② C.元素①位于第二周期第ⅣA族 D.元素的最高正化合价:③=⑤ |
|
| 6. 选择题 | 详细信息 |
|
下列化合物的电子式书写错误的是( ) A. |
|
| 7. 选择题 | 详细信息 |
|
下列性质中,可以证明某化合物内一定存在离子键的是( ) A.可溶于水 B.具有较高的熔点 C.水溶液能导电 D.熔融状态能导电 |
|
| 8. 选择题 | 详细信息 |
|
关于氢键,下列说法正确的是 A.每一个水分子内含有两个氢键 B.冰、水和水蒸气中都存在氢键 C.HF的沸点比HI高,是由于HF分子间存在氢键所致 D.H2O是一种非常稳定的化合物,这是由于氢键所致 |
|
| 9. 选择题 | 详细信息 |
|
据报道,最近科学家在宇宙中发现O4分子,则O4和O3属于 A.同位素 B.同一种物质 C.同素异形体 D.以上都不是 |
|
| 10. 选择题 | 详细信息 |
|
下列各组物质中互为同分异构体的是 A.1H2、2H2与3H2 B.冰与干冰 C.金刚石和石墨 D.CH3CH2OH与CH3OCH3 |
|
| 11. 选择题 | 详细信息 |
|
属于石墨用途的是①切割玻璃②做润滑剂③做电极④做装饰品 A.①② B.②③ C.①③ D.①④ |
|
| 12. 选择题 | 详细信息 |
|
共价键、离子键和分子间作用力都是构成物质或分子时粒子间的作用力。下列物质中,只含有离子键的是 A.干冰 B.氯化钠 C.氢氧化钠 D.碘 |
|
| 13. 选择题 | 详细信息 |
|
下列物质的晶体中,不是分子晶体的是 A.二氧化碳 B.氢氧化钠 C.水 D.硫酸 |
|
| 14. 选择题 | 详细信息 |
|
反应A(g)+3B(g)⇌2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最小的是 A.v(A)=0.04mol/(L·s) B.v(B)=0.06mol/(L·s) C.v(C)=0.05mol/(L·s) D.v(D)=0.02mol/(L·s) |
|
| 15. 选择题 | 详细信息 |
|
用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是 A.加热 B.不用稀硫酸,改用浓硫酸 C.滴加少量浓硫酸 D.不用铁片,改用铁粉 |
|
| 16. 选择题 | 详细信息 |
|
对化学反应限度的叙述,错误的是 A.任何化学反应都有一定的限度 B.化学反应的限度与时间的长短无关 C.化学反应的限度是不可改变的 D.可逆反应达到限度时,正逆反应速率相等 |
|
| 17. 选择题 | 详细信息 |
|
一定温度和压强下N2+3H2 A.N2与H2不再化合,NH3不再分解 B.N2、H2化合成NH3的反应速率等于NH3分解的反应速率 C.H2、NH3的体积分数相等 D.N2、H2、NH3的物质的量浓度相等 |
|
| 18. 选择题 | 详细信息 |
|
在一定温度下,在恒定容积的密闭容器中进行的可逆反应A2(g)+B2(g)⇌2AB(g)达到化学平衡的标志是 A.单位时间内有nmolA2生成的同时就有2nmolAB生成 B.反应速率v(A2)=v(B2)= C.容器内的总压强不随时间而变化 D.容器内混合气体的密度不随时间而变化 |
|
| 19. 选择题 | 详细信息 |
|
下列化学反应既属于氧化还原反应又属于吸热反应的是 A.铝片和稀盐酸反应 B.氢氧化钡晶体和氯化铵反应 C.灼热的碳与CO2反应 D.甲烷在氧气中燃烧。 |
|
| 20. 选择题 | 详细信息 |
|
下列热化学方程式书写正确的是 A.H2(g)+ B.2SO2+O2⇌2SO3△H=-196.6kJ/mol C.2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ D.C(s)+O2(g)=CO2(g)△H=+393.5kJ/mol |
|
| 21. 选择题 | 详细信息 |
|
钢铁在某酸雨区的潮湿空气中发生电化学腐蚀,其负极上的反应是 A.O2+2H2O+4e-=4OH- B.2H++2e-=H2↑ C.Fe-2e-=Fe2+ D.4OH--4e-=2H2O+O2↑ |
|
| 22. 选择题 | 详细信息 |
如图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关判断正确的是 A.a为负极,b为阴极 B.c极发生还原反应,d极发生氧化反应 C.电解过程中,d电极质量增加 D.氯离子向d极移动 |
|
| 23. 选择题 | 详细信息 |
|
以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是 A.电能全部转化为化学能 B.粗铜接电源正极,发生还原反应 C.溶液中Cu2+向阳极移动 D.利用阳极泥可回收Ag、Pt、Au等金属 |
|
| 24. 填空题 | 详细信息 | ||||||||||||
分析下列实例,根据已有的知识和经验,填如表中。______________
|
|||||||||||||
| 25. 解答题 | 详细信息 | |||||||||||||||||||||||||||
下表是元素周期表的一部分,按要求填空(填元素符号或化学式):
|
||||||||||||||||||||||||||||
| 26. 填空题 | 详细信息 | ||||||||||||||||||||||||||||||||||||||||||||||||||
下表是某兴趣小组通过实验获得的稀硫酸与某金属反应的实验数据:
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
| 27. 解答题 | 详细信息 |
根据如图所示电化学实验装置图,回答有关问题。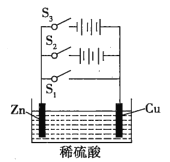 (1)若只闭合S1,该装置属于_______,能量转化形式为_______,锌极作_______极。 (2)若只闭合S2,该装置属于_______,能量转化形式为_______,锌极上的电极反应式为_______。 (3)若只闭合S3,该装置属于_______,铜极作_______极,锌极上的电极反应式为_______,总反应的化学方程式为_______。 |
|
| 28. 计算题 | 详细信息 |
|
向体积为2L的密闭容器中加入2molSO2和1molO2,进行可逆反应:2SO2+O2⇌2SO3反应2min时,测得O2的物质的量为0.8mol。 (1)2min内,SO2的物质的量减少了___________,SO3的物质的量增加了___________; (2)若用O2的浓度变化来表示该反应的反应速率,则v(O2)=___________; (3)若用SO3的浓度变化来表示该反应的反应速率,则v(SO3)=___________; (4)2min时SO2的浓度是___________。 |
|



