四川2020年高一化学下半年开学考试试卷完整版
| 1. 选择题 | 详细信息 |
|
化学与生活密切相关。下列说法错误的是( ) A.工业可用二氧化硫漂白纸浆、毛、丝、草帽辫等,也可用于杀菌消毒 B.医用消毒酒精中乙醇的浓度(体积分数)为 95% C.燃煤中加入 CaO 可以减少酸雨的形成却不能减少温室气体的排放 D.天然气和液化石油气是我国目前推广使用的清洁燃料 |
|
| 2. 选择题 | 详细信息 |
|
下列叙述中正确的是 ( ) ①汽车尾气中的氮氧化物与光化学烟雾的形成有关 ②大量燃烧含硫燃料是形成酸雨的主要原因 ③硅是制造太阳能电池和光导纤维的主要原料 ④减少CO2排放,可遏制全球气候变暖 ⑤碘盐中的碘可以直接用淀粉检验 ⑥点燃的硫在氧气中剧烈燃烧,发出蓝紫色火焰,生成三氧化硫 A. ①③⑤ B. ②③④⑤ C. ②④⑥ D. ①②④ |
|
| 3. 选择题 | 详细信息 |
|
下列关于元素周期表的说法正确的是( ) A. 元素周期表有7个周期,8个主族 B. 元素周期表有18个纵行,共16个族 C. 短周期元素中可能有副族元素 D. 元素周期表中的过渡元素就是副族元素 |
|
| 4. 选择题 | 详细信息 |
|
下列关于有机物的说法中,错误的是( ) A.在一定条件下葡萄糖能与新制Cu(OH)2发生反应 B.肥皂的主要成分是油脂在碱性条件下水解生成的 C.淀粉、纤维素和油脂都是天然高分子化合物 D.蛋白质溶液遇硫酸铜后产生的沉淀不能重新溶于水 |
|
| 5. 选择题 | 详细信息 |
|
除去二氧化碳中混有的少量二氧化硫气体,不可选用的试剂是( ) A.饱和碳酸钠溶液 B.高锰酸钾溶液 C.溴水 D.饱和碳酸氢钠溶液 |
|
| 6. 选择题 | 详细信息 |
|
铜锌合金的颜色酷似金的颜色,所以近来用铜锌合金制成的假金元宝欺骗行人的事件屡有发生。要检验市面上的金首饰是否为纯金或者真金,可取样品与一种试剂进行反应,根据现象即可判断,所取的试剂是(王水是3份浓盐酸和1份浓硝酸的混合物)( ) A.硫酸 B.“王水” C.盐酸 D.硝酸 |
|
| 7. 选择题 | 详细信息 |
|
化学实验中常将溶液或试剂进行酸化,下列酸化处理的措施正确的是 A. 定性检验SO B. 为提高高锰酸钾溶液的氧化能力,用盐酸将高锰酸钾溶液酸化 C. 检验溶液中是否含有Fe2+时,用硝酸酸化 D. 检验溶液中是否含有SO |
|
| 8. 选择题 | 详细信息 |
下图所示各为元素周期表中的一部分,表中数字是原子序数,其中X为35的是 A. A B. B C. C D. D |
|
| 9. 选择题 | 详细信息 |
|
有一酸性溶液可能含有Br-、SO42-、H2SO3、NH4+ 等微粒,对该酸性溶液分别进行实验: (1)加热,放出的气体可以使品红溶液褪色; (2)取原溶液加碱,调至溶液呈碱性,加热,放出的气体能使湿润的红色石蕊试纸变蓝; (3)取原溶液加氯水,溶液略显黄色,再加入BaCl2溶液,产生的白色沉淀不溶于稀硝酸。 对于下列微粒不能确认其在原溶液中是否存在的是 A.SO42- B.Br- C.H2SO3 D.NH4+ |
|
| 10. 选择题 | 详细信息 | |||||||||||||||
通过对实验现象的观察、分析推理得出结论是化学学习的方法之一。对下列实验事实解释正确的是( )
|
||||||||||||||||
| 11. 选择题 | 详细信息 |
|
以下指定化学反应的离子方程式正确的是 A. 常温下,将铁片置于浓硝酸中:Fe+6HNO3=Fe(NO3)3+3NO2↑+3H2O B. 向氯化铵的稀溶液中加入少量NaOH :NH4++OH― =NH3↑+H2O C. 向(NH4)2SO4溶液中加入适量Ba(OH)2 :Ba2++SO42— =BaSO4↓ D. 向浓硝酸中加入铜片:Cu+4H++2NO3―=Cu2++2NO2↑+2H2O |
|
| 12. 选择题 | 详细信息 |
下列实验装置不能达到实验目的的是 A. A B. B C. C D. D |
|
| 13. 选择题 | 详细信息 |
某兴趣小组探究 SO2 气体还原 Fe3+,他们使用的药品和装置如图所示,下列说法不合理的是( )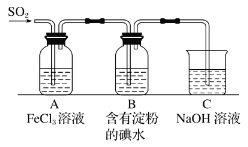 A.为了验证 A 中发生了氧化还原反应,加入KMnO4溶液,紫红色褪去 B.为了验证 A 中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2溶液,产生白色沉淀 C.能表明I-的还原性弱于SO2的现象是B中蓝色溶液褪色 D.装置C的作用是吸收SO2尾气,防止污染空气 |
|
| 14. 选择题 | 详细信息 |
|
NA 为阿伏加德罗常数的值,下列说法不正确的是( ) A.0.l mol Cl2与足量的铁粉充分反应转移的电子数为 0.2 NA B.1.0 mol CH4 与Cl2 在光照下反应生成的 CH3Cl 分子数为 1.0 NA C.标准状况下,11.2 L甲烷和乙烯(C2H4)混合物中含氢原子数目为2 NA D.0.1mol Cl2 通入水中,HClO、Cl-、ClO-粒子数之和小于 0.2 NA |
|
| 15. 选择题 | 详细信息 |
短周期元素W、X、Y、Z 的原子序数依次增加。m、p、r 是由这些元素组成的二元化合物,n 是元素Z 的单质,通常为黄绿色气体,q 的水溶液具有漂白性,r 溶于水是强酸,s 通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是 ( ) A.W 在周期表中所在族全是金属 B.X 的最高价氧化物的水化物为强酸 C.Y 的氢化物常温常压下为气态 D.1molZ 单质与氢氧化钠溶液反应转移 1mol 电子 |
|
| 16. 选择题 | 详细信息 |
|
下列说法正确的是( ) A.乙烯与环丙烷(C3H6)互为同系物 B.乙烯和聚乙烯均能和溴水发生加成反应而使溴水褪色 C.皮肤沾上浓HNO3变成黄色,立即用饱和NaOH溶液冲洗 D.丙酸、乙酸甲酯和2-羟基丙醛(CH3CHOHCHO)互为同分异构体 |
|
| 17. 选择题 | 详细信息 |
|
1.92g 铜投入一定量浓 HNO3 中,铜完全溶解,生成气体颜色越来越浅,共收集到672mL 气体(标况)。将盛有此气体的容器倒扣在水中,通入标况下一定体积的 O2,恰好使气体完全溶于水中,则通入O2 的体积可能是 A.504mL B.168mL C.336mL D.224mL |
|
| 18. 选择题 | 详细信息 |
某食用香料乙酸橙花酯的结构简式如图所示,则关于该有机物叙述中正确的个数是( )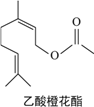 ①分子式为C12H20O2 ②它的同分异构体中有芳香族化合物 ③能使酸性KMnO4溶液褪色 ④1mol该有机物在一定条件下能和3mol H2反应 ⑤密度比水小 ⑥1mol该有机物水解时能消耗1molNaOH⑦能在一定条件下生成高分子化合物 A. 3个 B. 4个 C. 5个 D. 6个 |
|
| 19. 填空题 | 详细信息 |
|
请按要求回答下列问题: (1)醇的官能团的名称是_____。 (2)某气态有机物相对于氢气的密度为14,则其结构简式为_____。 (3)某有机物的结构简式如图所示,则其一氯代物共有_____种。 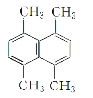 (4)新戊烷用系统命名法命名应为_____。 (5)分别将等物质的量的C3H8、C4H8完全燃烧,消耗氧气质量多的是_____(填分子式)。 (6)下列最简式中,只能代表一种有机物的有_____(选填对应的序号)。 ①CH3 ②CH2 ③CH2O ④CH4O |
|
| 20. 实验题 | 详细信息 |
某化学兴趣小组利用以下各装置连接成一整套装置,探究氯气与氨气之间的反应。其中D为纯净干燥的氯气与纯净干燥氨气反应的装置。 请回答下列问题: (1)连接好装置后,必需进行的一步实验操作是_____________。 (2)装置E的作用是___,橡胶管k的作用是___________________。 (3)从装置D的G处逸出的尾气中可能含有黄绿色的有毒气体,处理方法是_________。 (4)装置F中试管内发生反应的化学方程式_______________。 (5)接入D装置的两根导管左边较长、右边较短,目的是__________. (6)整套装置从左向右的连接顺序是(j)接(___)(___)接(f)(g)接(___)(___)接(___)(___)接(a)。 |
|
| 21. | 详细信息 | |||||||||
|
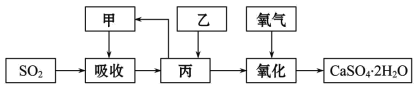
燃煤的烟气中含有 SO2,为了治理雾霾天气,工厂采用多种方法实现烟气脱硫。 Ⅰ.(1)“湿式吸收法”利用吸收剂与 SO2 发生反应从而脱硫。下列试剂中适合用作该法吸收剂的是_____(填字母序号)。 a. 石灰乳 b.CaCl2溶液 (2)某工厂利用含 SO2 的烟气处理含Cr2O72-的酸性废水,吸收塔中反应后的铬元素以Cr3+形式存在,具体流程如下:  ①用 SO2 处理含铬废水时,利用了 SO2 的_____性。 ②吸收塔中发生反应的离子方程式为_____。 Ⅱ.石灰-石膏法和烧碱法是常用的烟气脱硫法。石灰-石膏法的吸收反应为Ca(OH)2+SO2= CaSO3↓+H2O。吸收产物亚硫酸钙由管道输送至氧化塔氧化,反应为2CaSO3+O2+4H2O =2CaSO4·2H2O。其流程如图: 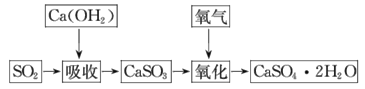 烧碱法的吸收反应为2NaOH+SO2=Na2SO3+H2O。该法的特点是氢氧化钠碱性强、吸收快、效率高。其流程如图:  已知:
|
||||||||||
| 22. 实验题 | 详细信息 |
|
1942年,我国化工专家侯德榜以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱,他的“侯氏制碱法”为世界制碱工业做出了突出贡献。有关反应的化学方程式如下: NH3+CO2+H2O=NH4HCO3; NH4HCO3+NaCl=NaHCO3↓+NH4Cl; 2NaHCO3 (1)“侯氏制碱法”把合成氨和纯碱两种产品联合生产,请写出工业合成氨的化学反应方程式_____。 (2)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是______。 a.碳酸氢钠难溶于水 b.碳酸氢钠受热易分解 c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出 (3)某探究活动小组根据上述制碱原理,欲制备碳酸氢钠,同学们按各自设计的方案进行实验。 第一位同学:将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如图所示(图中夹持、固定用的仪器未画出)。 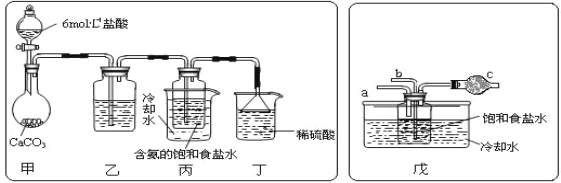 请回答: ①写出甲中发生反应的离子方程式______。 ②乙装置中的试剂是______。 ③实验结束后,分离出NaHCO3晶体的操作是______(填分离操作的名称)。 (4)第二位同学:用图中戊装置进行实验(其它装置未画出)。 ①为提高二氧化碳在此反应溶液中被吸收的程度,实验时,须先从a管通入______气体,再从b管中通入______气体。 ②装置c中的试剂为______(选填字母)。 e.碱石灰 f.浓硫酸 g.无水氯化钙 ③若该同学进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为______。 |
|
最近更新