重庆市第一中学2020届高三10月月考理综化学试卷带参考答案和解析
| 1. 选择题 | 详细信息 |
|
化学与生产和生活密切相关,下列说法错误的是 A.“硅胶”的主要成分是硅酸钠,可用作干燥剂和催化剂的载体 B.用SO2漂白纸浆和用活性炭为糖浆脱色的原理不相同 C.氢氧化铝、碳酸氢钠都是常见的胃酸中和剂 D.废旧钢材焊接前,可依次用饱和Na2CO3溶液、饱和NH4Cl溶液处理焊点 |
|
| 2. 选择题 | 详细信息 |
|
设NA代表阿伏加德罗常数的值,下列叙述正确的是 A.1mol ICl与H2O完全反应生成氯化氢和次碘酸,转移的电子数为NA B.常温常压下,56 g丁烯 (C4H8)中含有的共价单键总数为8 NA C.电解精炼铜时,阳极质量减少64g,闭合回路转移的电子数一定为2NA D.质量均为3.2g的S2、S4、S6中所含S原子数相等,都为0.1 NA |
|
| 3. 选择题 | 详细信息 |
水杨酸冬青油、阿司匹林的结构简式如图,下列说法不正确的是 A. 由水杨酸制冬青油的反应是取代反应 B. 阿司匹林的分子式为C9H8O4,在一定条件下水解可得水杨酸 C. 冬青油苯环上的一氯取代物有4种 D. 可用NaOH溶液除去冬青油中少量的水杨酸 |
|
| 4. 选择题 | 详细信息 | |||||||||||||||||||||||||
利用图示装置进行实验,反应进行足够长时间后装置II中实验现象正确的是
|
||||||||||||||||||||||||||
| 5. 选择题 | 详细信息 |
W、X、Y、Z为原子序数依次增大的短周期主族元素,其中Y元素在同周期中离子半径最小;甲、乙分别是元素Y、Z的单质;丙、 丁、戊是由W、X、Y、Z元素组成的二元化合物,常温下丁为液态;戊为酸性气体,常温下0.01mol·L-1戊溶液的pH大于2。上述物质转化关系如图所示。下列说法正确的是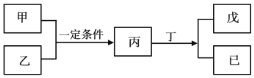 A.原子半径:Z>Y>X>W B.W和X形成的化合物既可能含有极性键也可能含有非极性键 C.Z的氧化物对应的水化物均为强酸 D.简单氢化物的热稳定性:X<Z |
|
| 6. 选择题 | 详细信息 |
因存在浓度差而产生电动势的电池称为浓差电池。利用如图所示装置进行实验,开始先闭合K2,断开Kl,电解一段时间后,再断开K2,闭合Kl,形成浓差电池,电流计指针偏转(Ag+浓度越大,氧化性越强)。下列说法不正确的是 A.闭合K2,断开Kl,NO3-从左池向右池移动 B.断开K2,闭合K1,X为正极 C.闭合K2,断开Kl一段时间后,右池c(AgNO3)增大 D.装置安装后若直接闭合Kl,电流计指针不发生偏转,但往左池加入适当的氨水后,指针偏转 |
|
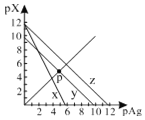
| 7. 选择题 | 详细信息 | ||||||||||||
已知:pAg=-lg c(Ag+),pX=-lg c(Xn-)。298 K时,几种物质的Ksp如下表:
|
|||||||||||||
| 8. 实验题 | 详细信息 |
|
长期缺碘和碘摄入过量都会对健康造成危害,目前加碘食盐中碘元素绝大部分以IO3-存在,少量以I-存在。现使用Na2S2O3对某碘盐样品中碘元素的含量进行测定。 I.I-的定性检测 (1)取少量碘盐样品于试管中,加水溶解。滴加硫酸酸化,再滴加数滴5%NaNO2和淀粉的混合溶液。若溶液变色,则存在I-,同时产生的无色气体产生遇空气变为红棕色,试写出该反应的离子方程式为_____________。 Ⅱ.硫代硫酸钠的制备 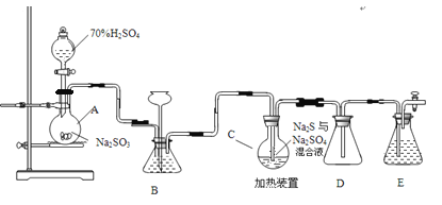 化学实验室可用如下装置(略去部分加持仪器)制备Na2S2O3•5H2O。烧瓶C中发生反应如下: Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (I) 2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (II) S(s)+Na2SO3(aq) (2)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若_____________,则整个装置气密性良好。装置D的作用是_____________ 。装置E中为_____________溶液。 (3)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为_____________。 (4)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择____________。 a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液 实验中,为使SO2缓慢进入烧瓶C,采用的操作是_____________。已知反应(III)相对较慢,则烧瓶C中反应达到终点的现象__________________。 (5)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出Na2S2O3•5H2O,其中可能含有Na2SO3、Na2SO4等杂质。利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作____________,现象和结论_________:。 已知Na2S2O3•5H2O遇酸易分解:S2O32‾+2H+=S↓+SO2↑+H2O 供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液 Ⅲ.碘含量的测定 巳知:①称取10.00g碘盐样品,置于250mL锥形瓶中,加水100mL溶解,加2mL磷酸,摇匀。 ②滴加饱和溴水至溶液呈现浅黄色,边滴加边摇,至黄色不褪去为止(约1mL)。 ③加热煮沸,除去过量的溴,再继续煮沸5min,立即冷却,加入足量15%碘化钾溶液,摇匀。 ④加入少量淀粉溶液作指示剂,再用0.002mol/L的Na2S2O3标准溶液滴定至终点。 ⑤重复两次,平均消耗Na2S2O3溶液9.00mL 相关反应为:I-+3Br2+3H2O = IO3-+6H++6Br-,IO3-+5I-+6H+ = 3I2+3H2O,I2+2S2O32-= 2I-+S4O62- (6)请根据上述数据计算该碘盐含碘量为_______________mg·kg-1。 |
|
| 9. | 详细信息 |
工业上利用废镍催化剂(主要成分为Ni,还含有一定量的Zn、Fe、SiO2、CaO)制备草酸镍晶体(NiC2O4·2H2O)的流程如下: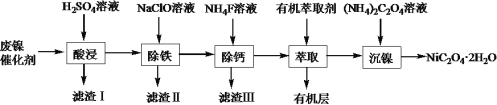 (1)NiC2O4·2H2O中C的化合价是______。既能加快“酸浸”反应速率又能提高“酸浸”原料利用率的操作措施为_____________。 (2)“滤渣Ⅰ”的主要成分是_____________。若控制温度为80℃、pH=2时,“除铁”产生的“滤渣Ⅱ”的主要成分为黄钠铁矾(Na2Fe6(SO4)4(OH)12),写出生成黄钠铁矾沉淀的离子方程式:__________________。 (3)已知“滤渣Ⅲ”的主要成分为CaF2,则“萃取”操作中加入有机萃取剂的作用是__________。 (4)在隔绝空气的条件下,高温煅烧无水NiC2O4得到Ni2O3和两种含碳元素的气体,该反应的化学方程式是_________。 (5)高能锂离子电池的总反应为2Li + FeS = Fe + Li2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF6·SO(CH3)2为电解质)。 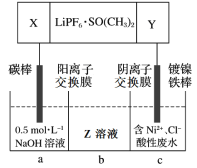 ①电极X的反应材料是_________(填化学式);中间隔室b可以得到的主要物质Z是_________(填化学式)。 ②电解总反应的离子方程式为_________。已知F=96500C/mol,若电池工作t min,维持电流强度为I A,理论回收Ni_________g(写出计算表达式即可)。 |
|
| 10. 综合题 | 详细信息 |
|
研究处理NOx、SO2,对环境保护有着重要的意义。回答下列问题: (1)SO2的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的SO2。已知吸收过程中相关反应的热化学方程式如下:① SO2(g) + NH3•H2O(aq) =NH4HSO3(aq) △H1 = a kJ•mol-1;② NH3•H2O(aq) + NH4HSO3(aq) =(NH4)2SO3(aq) + H2O(l)△H2 = b kJ•mol-1;③ 2(NH4)2SO3(aq) + O2(g) =2(NH4)2SO4(aq) △H3= c kJ•mol-1,则反应 2SO2(g) + 4NH3•H2O(aq) + O2(g) =2(NH4)2SO4(aq) + 2H2O(l) △H = ______。 (2)NOx的排放主要来自于汽车尾气,有人利用反应C (s) + 2NO(g) 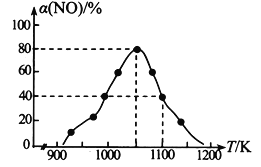 ①由图可知,1050K前反应中NO的转化率随温度升高而增大,原因是_________________________; 在1100K 时,CO2的体积分数为______。 ②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1050K、1.1×106Pa 时,该反应的化学平衡常数Kp=________(已知:气体分压=气体总压×体积分数)。 (3)在高效催化剂的作用下用CH4还原NO2,也可消除氮氧化物的污染。在相同条件下,选用A、B、C三种不同催化剂进行反应,生成 N2的物质的量与时间变化关系如图所示,其中活化能最小的是_________(填字母标号)。 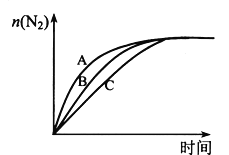 (4)在汽车尾气的净化装置中 CO和NO发生反应:2NO(g) + 2CO(g) ①达到平衡后,仅升高温度,k正增大的倍数_____(填" >”、“< ”或“=”) k逆增大的倍数。 ②若在1L 的密闭容器中充入1 mol CO和1 mol NO,在一定温度下达到平衡时,CO的转化率为40%,则 |
|
| 11. 综合题 | 详细信息 |
|
早在1998年,中国科学家便成功地在较低温度下制造出金刚石:CCl4+4Na (1)Ni原子价层电子的排布式为_______。元素C、Cl、Na中,第一电离能最大的是______________。 (2)石墨在高温高压下也可转变为金刚石。在石墨和金刚石中,C原子的杂化类型分别为_____________,熔点较高的是_____________,其原因为_______________。 (3)NH3易与Ni形成配合物 [Ni(NH3)6]SO4,该配合物中存在的化学键类型有_____________,其阴离子的空间构型为_____________。 (4)金属间化合物MgCNi3是一种新型超导体,呈钙钛矿构型,X射线衍射实验测得其晶胞参数为a=0.3812 nm,其晶胞结构如图所示。晶胞中C位于Ni所形成的正八面体的体心,该正八面体的边长为___________nm。(  (5)在MgCNi3晶胞结构的另一种表示中,Mg处于体心位置,则C处于________________位置,Ni处于_______________位置。 |
|
| 12. 推断题 | 详细信息 |
高分子材料尼龙66具有良好的抗冲击性、韧性、耐燃油性和阻燃、绝缘等特点,因此广泛应用于汽车、电气等工业中。以下是生产尼龙66的一些途径。 (1)A中所有碳原子都处于同一直线上,则A的结构简式为_____________。 (2)B的名称是_____________。 (3)反应①~④中,属于加成反应的有_____________,反应⑥~⑨中,属于氧化反应的有_____________。 (4)请写出反应⑥的化学方程式为_____________。 (5)高分子材料尼龙66中含有 (6)某聚合物K的单体与A互为同分异构体,该单体核磁共振氢谱有三个峰,峰面积之比为1:2:3,且能与NaHCO3溶液反应,则聚合物K的结构简式是_____________。 (7)聚乳酸( 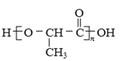 )是一种生物可降解材料,已知羰基化合物可发生下述反应: )是一种生物可降解材料,已知羰基化合物可发生下述反应: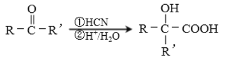 (R′可以是烃基或H原子)。用合成路线图表示用乙醇制备聚乳酸的过程_____________。 (R′可以是烃基或H原子)。用合成路线图表示用乙醇制备聚乳酸的过程_____________。 |
|
最近更新