2020еұҠй«ҳдёүеҢ–еӯҰдәҢиҪ®жҜҸе‘ЁеӨ§йўҳеҝ…з»ғ - -- ж— жңәе·ҘдёҡжөҒзЁӢйўҳ
| 1. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||
дёҖз§Қд»ҘиҪҜй”°зҹҝ(дё»иҰҒжҲҗеҲҶдёәMnO2гҖҒSiO2гҖҒAl2O3)е’Ңй»„й“Ғзҹҝ(FeS2гҖҒSiO2)дёәеҺҹж–ҷеҶ¶зӮјйҮ‘еұһй”°зҡ„е·ҘиүәжөҒзЁӢеҰӮеӣҫжүҖзӨәпјҡ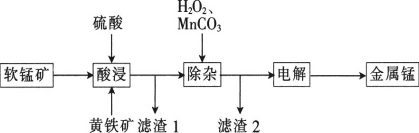 е·ІзҹҘзӣёе…ійҮ‘еұһзҰ»еӯҗ[c(MnпјӢ)пјқ0.1molВ·LпјҚ1]еҪўжҲҗж°ўж°§еҢ–зү©жІүж·Җзҡ„pHеҰӮдёӢпјҡ
|
|||||||||||||
| 2. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||||||
зЎ«й…ёй“ңжҳҜдёҖз§Қеә”з”ЁжһҒе…¶е№ҝжіӣзҡ„еҢ–е·ҘеҺҹж–ҷпјӣд»ҘдёӢжҳҜжҹҗе·ҘеҺӮз”Ёеҗ«й“Ғеәҹй“ңдёәеҺҹж–ҷз”ҹдә§иғҶзҹҫпјҲCuSO4вҖў5H2Oпјүе’ҢеүҜдә§зү©зҹіиҶҸпјҲCaSO4вҖў2H2Oпјүзҡ„з”ҹдә§жөҒзЁӢзӨәж„Ҹеӣҫпјҡ иғҶзҹҫе’ҢзҹіиҶҸеңЁдёҚеҗҢжё©еәҰдёӢзҡ„жә¶и§ЈеәҰпјҲg/100gж°ҙпјүи§ҒиЎЁгҖӮ
|
|||||||||||||||||||
| 3. | иҜҰз»ҶдҝЎжҒҜ |
д»Һй“қеңҹзҹҝ иҜ·еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ |
|
| 4. з»јеҗҲйўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
й“…еҸҠе…¶еҢ–еҗҲзү©еңЁе·Ҙдёҡз”ҹдә§гҖҒз”ҹжҙ»дёӯе…·жңүйқһеёёе№ҝжіӣзҡ„з”ЁйҖ”гҖӮ пјҲ1пјүз“ҰзәҪ科еӨ«жі•зҶ”зӮјй“…пјҢе…¶зӣёе…іеҸҚеә”зҡ„зғӯеҢ–еӯҰж–№зЁӢејҸеҰӮдёӢпјҡ в‘ 2PbS(s)+3O2(g)=2PbO(s)+2SO2(g) в–іH1пјқakJВ·mol-1 в‘ЎPbS(s)2PbO(s)=3Pb(s)+SO2(g) в–іH2пјқb kJВ·mol-1 в‘ўPbS(s)+PbSO4(s)=2Pb(s)+2SO2(g) в–іH3пјқc kJВ·mol-1 еҸҚеә”3PbS(s)+6O2(g)=3PbSO4(s) в–іHпјқ____________kJВ·mol-1пјҲз”Ёеҗ«aгҖҒbгҖҒcзҡ„д»Јж•°ејҸиЎЁзӨәпјү пјҲ2пјүд»Ҙеҗ«й“…еәҹж–ҷпјҲдё»иҰҒеҗ«PbгҖҒPbOгҖҒPbO2гҖҒPbSO4пјүдёәеҺҹж–ҷеҲ¶еӨҮй«ҳзәҜPbOпјҢе…¶дё»иҰҒжөҒзЁӢеҰӮдёӢпјҡ  в‘ вҖңй…ёжә¶вҖқж—¶пјҢеңЁFe2+еӮ¬еҢ–дёӢпјҢPbе’ҢPbO2еҸҚеә”жҲҗ1 mol PbSO4ж—¶иҪ¬з§»з”өеӯҗзҡ„зү©иҙЁзҡ„йҮҸдёә_________ molгҖӮ в‘Ўе·ІзҹҘпјҡPbOжә¶и§ЈеңЁNaOHжә¶ж¶ІдёӯпјҢеӯҳеңЁеҢ–еӯҰе№іиЎЎпјҡPbO(s)+NaOH(aq)  з»“еҗҲдёҠиҝ°дҝЎжҒҜпјҢе®ҢжҲҗз”ұзІ—е“ҒPbOпјҲжүҖеҗ«жқӮиҙЁдёҚжә¶дәҺNaOHжә¶ж¶Іпјүеҫ—еҲ°й«ҳзәҜPbOзҡ„ж“ҚдҪңпјҡе°ҶзІ—е“ҒPbOжә¶и§ЈеңЁдёҖе®ҡйҮҸ________пјҲеЎ«вҖң35пј…вҖқжҲ–вҖң10пј…вҖқпјүзҡ„NaOHжә¶ж¶ІдёӯпјҢеҠ зғӯиҮі110в„ғпјҢе……еҲҶжә¶и§ЈеҗҺпјҢ_______________пјҲеЎ« вҖңи¶ҒзғӯиҝҮж»ӨвҖқжҲ–вҖңи’ёеҸ‘жө“зј©вҖқпјүпјҢе°Ҷж»Өж¶ІеҶ·еҚҙз»“жҷ¶пјҢиҝҮж»ӨгҖҒжҙ—ж¶Ө并干зҮҘеҫ—еҲ°й«ҳзәҜPbOеӣәдҪ“гҖӮ пјҲ3пјүе°ҶзІ—е“ҒPbOжә¶и§ЈеңЁHClе’ҢNaClзҡ„ж··еҗҲжә¶ж¶ІдёӯпјҢеҫ—еҲ°еҗ«Na2PbCl4зҡ„з”өи§Јж¶ІпјҢз”өи§ЈNa2PbCl4жә¶ж¶Із”ҹжҲҗPbзҡ„иЈ…зҪ®еҰӮеӣҫ2жүҖзӨәпјҡ  в‘ йҳҙжһҒзҡ„з”өжһҒеҸҚеә”ејҸдёә______________________пјӣ в‘ЎеҪ“жңү4.14gPbз”ҹжҲҗж—¶пјҢйҖҡиҝҮиҙЁеӯҗдәӨжҚўиҶңзҡ„n(H+)=______________________гҖӮ пјҲ4пјүPbI2еҸҜз”ЁдәҺдәәе·ҘйҷҚйӣЁгҖӮеҸ–дёҖе®ҡйҮҸзҡ„PbI2еӣәдҪ“пјҢз”Ёи’ёйҰҸж°ҙй…ҚеҲ¶жҲҗtв„ғйҘұе’Ңжә¶ж¶ІпјҢеҮҶ确移еҸ–25.00 mL PbI2йҘұе’Ңжә¶ж¶ІеҲҶж¬ЎеҠ е…ҘйҳізҰ»еӯҗдәӨжҚўж ‘и„ӮRH+пјҲеҸ‘з”ҹеҸҚеә”пјҡ2RH++PbI2 =R2Pb+2H++2I-пјүпјҢз”Ё250mlжҙҒеҮҖзҡ„й”ҘеҪўз“¶жҺҘ收жөҒеҮәж¶ІпјҢеҗҺз”Ёи’ёйҰҸж°ҙж·Ӣжҙ—ж ‘и„ӮиҮіжөҒеҮәж¶Іе‘ҲдёӯжҖ§пјҢе°Ҷжҙ—ж¶Өж¶ІдёҖ并зӣӣж”ҫеҲ°й”ҘеҪўз“¶дёӯпјҲеҰӮеӣҫ3пјүгҖӮеҠ е…Ҙй…ҡй…һжҢҮзӨәеүӮпјҢз”Ё0.0050molВ·L-1NaOHжә¶ж¶Іж»ҙе®ҡпјҢеҪ“иҫҫеҲ°ж»ҙе®ҡз»ҲзӮ№ж—¶пјҢз”ЁеҺ»ж°ўж°§еҢ–й’ жә¶ж¶І10.00mLгҖӮеҸҜи®Ўз®—еҮәtв„ғж—¶Ksp(PbI2)дёә_________________гҖӮ |
|
| 5. | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||||||||
е…үзәӨйҖҡи®ҜжҳҜе…үеҜјзәӨз»ҙдј йҖҒдҝЎеҸ·зҡ„дёҖз§ҚйҖҡи®ҜжүӢж®өпјҢеҗҲжҲҗе…үеҜјзәӨз»ҙеҸҠж°®еҢ–зЎ…пјҲдёҖз§Қж— жңәж¶ӮеұӮпјүзҡ„е·ҘиүәжөҒзЁӢеҰӮдёӢпјҡ еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ пјҲ1пјүеҸҚеә”в… зҡ„еҢ–еӯҰж–№зЁӢејҸдёә2C+SiO2 пјҲ2пјүз»ҸеҸҚеә”в…ЎжүҖеҫ—зҡ„еӣӣж°ҜеҢ–зЎ…зІ—е“ҒдёӯжүҖеҗ«зҡ„зү©иҙЁеҰӮдёӢпјҡ
|
||||||||||||||||||||||
| 6. з»јеҗҲйўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
й“қжҳҜең°еЈідёӯеҗ«йҮҸжңҖеӨҡзҡ„йҮ‘еұһе…ғзҙ пјҢе…¶еҚ•иҙЁе’ҢеҢ–еҗҲзү©е№ҝжіӣеә”з”ЁдәҺж—Ҙеёёз”ҹжҙ»дёӯгҖӮ (1)й“қзІүе’Ңй“Ғзҡ„ж°§еҢ–зү©(FeO-Fe2O3)еҸҜй…ҚжҲҗй“қзғӯеүӮз”ЁдәҺз„ҠжҺҘй’ўиҪЁпјҢеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸжҳҜ____гҖӮ (2)д»Ҙй“қеңҹзҹҝ(дё»иҰҒжҲҗеҲҶдёәAl2O3.еҗ«SiO2е’ҢFe2O3зӯүжқӮиҙЁ)дёәеҺҹж–ҷз”ҹдә§й“қе’Ңй“өжҳҺзҹҫжҷ¶дҪ“[NH4Al(SO4)2В·12H2O]зҡ„дёҖз§Қе·ҘиүәжөҒзЁӢеҰӮдёӢпјҲе·ІзҹҘ:SiO2еңЁвҖңзўұжә¶вҖқж—¶иҪ¬еҢ–дёәй“қзЎ…й…ёй’ (NaAlSiO4В·nH2O)жІүж·ҖпјүгҖӮ 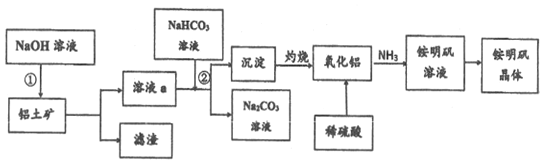 в‘ е®һйӘҢеүҚпјҢиҰҒе°Ҷй“қеңҹзҹҝзІүзІ№зҡ„зӣ®зҡ„жҳҜ_______гҖӮ в‘Ўз”Ёж°§еҢ–зү©зҡ„еҪўејҸиЎЁзӨәй“қзЎ…й…ёй’ зҡ„еҢ–еӯҰејҸ________гҖӮ в‘ўжӯҘйӘӨв‘Ўж¶үеҸҠеҲ°зҡ„зҰ»еӯҗж–№зЁӢејҸжҳҜ: _______гҖӮ в‘ЈеҶҷеҮәеҲ©з”ЁAl2O3еҲ¶еӨҮйҮ‘еұһAlзҡ„еҢ–еӯҰж–№зЁӢејҸ: _______гҖӮ в‘ӨиӢҘеҗҢж—¶еҲ¶еҸ–й“өжҳҺзҹҫе’ҢзЎ«й…ёй“қпјҢйҖҡиҝҮжҺ§еҲ¶зЎ«й…ёзҡ„з”ЁйҮҸи°ғиҠӮдёӨз§Қдә§е“Ғзҡ„дә§йҮҸгҖӮиӢҘж¬ІдҪҝеҲ¶еҫ—зҡ„й“өжҳҺзҹҫе’ҢзЎ«й…ёй“қзҡ„зү©иҙЁзҡ„йҮҸд№ӢжҜ”дёә1 : 1,еҲҷжҠ•ж–ҷж—¶й“қеңҹзҹҝдёӯзҡ„Al2O3е’ҢH2SO4зҡ„зү©иҙЁзҡ„йҮҸд№ӢжҜ”дёә_______гҖӮ |
|
| 7. | иҜҰз»ҶдҝЎжҒҜ |
й’ЁжҳҜжҲ‘еӣҪдё°дә§е…ғзҙ гҖӮз§‘з ”дё“е®¶з»ҸиҝҮй•ҝжңҹеӢҳжөӢиҜ„е®ЎпјҢдәҺ2016е№ҙе…ғжңҲзЎ®и®ӨжұҹиҘҝзңҒжө®жўҒеҺҝеӯҳеңЁзқҖдё–з•ҢдёҠжңҖеӨ§зҡ„й’ЁзҹҝгҖӮд»ҺиҖҢиҝӣдёҖжӯҘзЎ®з«ӢдәҶжұҹиҘҝзңҒвҖңдё–з•Ңй’ЁйғҪвҖқзҡ„ең°дҪҚгҖӮиҮӘ然з•Ңдёӯй’ЁжңүйғЁеҲҶжҳҜд»Ҙй’ЁпјҲ+6д»·пјүй…ёзӣҗзҡ„еҪўејҸеӯҳеңЁгҖӮй»‘й’Ёзҹҝзҡ„дё»иҰҒжҲҗеҲҶжҳҜй“Ғе’Ңй”°зҡ„й’Ёй…ёзӣҗпјҲFeWO4гҖҒMnWO4пјүпјҢеҗ«жңүSiO2гҖҒAl2O3зӯүжқӮиҙЁгҖӮзҺ°з”Ёй»‘й’ЁзҹҝеҲ¶еӨҮйҮ‘еұһй’Ёзҡ„жөҒзЁӢеӣҫеҰӮеӣҫпјҡ иҜҙжҳҺпјҡaпјҡеҸҚеә”в‘ жҳҜеңЁй«ҳжё©зҶ”иһҚдёӢиҝӣиЎҢзҡ„пјҢзғ§з»“зү©жҲҗеҲҶдёәпјҡFe2O3гҖҒMn2O4гҖҒNaAlO2гҖҒNa2SiO3гҖҒNa2WO4 bпјҡз”ҹжҲҗFe2O3зҡ„еҸҚеә”дёәпјҡ4FeWO4+4Na2CO3+O2=4Na2WO4+4CO2+2Fe2O3 cпјҡеңЁpHеҖј3.0пҪһ4.4зҡ„зғӯжә¶ж¶ІдёӯпјҢз”Ёзӣҗй…ёжІүж·ҖеҮәй’Ёй…ёдёҺжқӮиҙЁеҲҶзҰ»пјҢзҒјзғ§еҗҺеҚідёәдёүж°§еҢ–й’Ё еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ пјҲ1пјүеҶҷеҮәзғ§з»“зү©дёӯз”ҹжҲҗNa2SiO3зҡ„еҢ–еӯҰеҸҚеә”ж–№зЁӢејҸпјҡ__пјҢз”ҹжҲҗMn2O4дёҺз”ҹжҲҗFe2O3жүҖеҸ‘з”ҹзҡ„еҸҚеә”еҺҹзҗҶзӣёеҗҢпјҢиҜ·еҶҷеҮәз”ҹжҲҗMn3O4зҡ„еҢ–еӯҰеҸҚеә”ж–№зЁӢејҸпјҡ___гҖӮ пјҲ2пјүж“ҚдҪң3йңҖиҰҒз”ЁеҲ°зҺ»з’ғд»ӘеҷЁзҡ„жңүпјҡ__гҖӮ пјҲ3пјүйҖҡе…Ҙи¶ійҮҸCO2ж—¶еҸ‘з”ҹзҡ„зҰ»еӯҗеҸҚеә”ж–№зЁӢејҸдёәпјҡ___гҖҒ___гҖӮ пјҲ4пјүдёҠиҝ°жөҒзЁӢжңҖеҗҺжӯҘйӘӨдёӯй’Ёзҡ„еҲ¶еӨҮеұһдәҺе·ҘдёҡеҶ¶зӮјйҮ‘еұһзҡ„дҪ•з§Қж–№жі•___гҖӮ пјҲ5пјүжҲ‘еӣҪй’ЁеҢ–еӯҰз ”з©¶зҡ„еҘ еҹәдәәйЎҫзҝјдёңе…Ҳз”ҹйҮҮз”ЁеҸҰеӨ–зҡ„еҸҚеә”еҲ¶еҫ—дәҶдёҖз§Қй»„иүІзҡ„гҖҒйқһж•ҙжҜ”зҡ„й’Ёзҡ„ж°§еҢ–зү©WOпјҲ3-xпјүпјҢиҝҷз§Қи“қиүІж°§еҢ–й’Ёе…·жңүжҜ”иЎЁйқўеӨ§гҖҒжҳ“иҝҳеҺҹеҫ—дјҳзӮ№гҖӮдёҖиҲ¬и®ӨдёәпјҢи“қиүІж°§еҢ–й’Ёзҡ„йўңиүІе’Ңйқһж•ҙжҜ”жҡ—зӨәдәҶеңЁеҢ–еҗҲзү©дёӯеӯҳеңЁжӯЈдә”д»·е’ҢжӯЈе…ӯд»·дёӨз§ҚзҠ¶жҖҒзҡ„й’ЁпјҢиӢҘxзҡ„еҖјдёә0.1пјҢеҲҷи“қиүІж°§еҢ–й’ЁдёӯиҝҷдёӨз§Қд»·жҖҒзҡ„й’ЁеҺҹеӯҗж•°д№ӢжҜ”дёә___гҖӮ |
|
| 8. з»јеҗҲйўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
IгҖҒеҲ©з”ЁеӨӘйҳіиғҪпјҢд»Ҙ 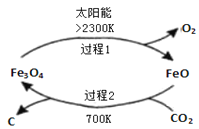 IIгҖҒиҝ‘е№ҙ科еӯҰ家жҸҗеҮәвҖңз»ҝиүІиҮӘз”ұвҖқжһ„жғіпјҺжҠҠеҗ«жңүеӨ§йҮҸ    еҲҷиҜҘ100mLеҗёж”¶ж¶ІиҝҳеҸҜеҗёж”¶ж ҮеҮҶзҠ¶еҶөдёӢ______ в…ў  |
|
| 9. з»јеҗҲйўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
ж°ҙжҳҜдёҖз§ҚйҮҚиҰҒзҡ„иҮӘ然иө„жәҗпјҢжҳҜдәәзұ»иө–д»Ҙз”ҹеӯҳдёҚеҸҜзјәе°‘зҡ„зү©иҙЁпјҢж°ҙиҙЁдјҳеҠЈзӣҙжҺҘеҪұе“ҚдәәдҪ“еҒҘеә·пјҢиҜ·еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ пјҲ1пјүжҹҗиҙ«еӣ°еұұеҢәпјҢдёәдәҶеҜ»жүҫеҗҲйҖӮзҡ„йҘ®з”Ёж°ҙпјҢеҜ№еұұдёҠзҡ„жіүж°ҙиҝӣиЎҢдәҶеҲҶжһҗеҢ–йӘҢпјҢз»“жһңжҳҫзӨәпјҢж°ҙдёӯдё»иҰҒеҗ«Ca2+гҖҒMg2+гҖҒClп№Је’ҢSO42п№ЈгҖӮеҲҷиҜҘзЎ¬ж°ҙеұһдәҺ_____(еЎ«вҖңжҡӮж—¶вҖқжҲ–вҖңж°ёд№…вҖқ)зЎ¬еәҰпјҢиӢҘиҰҒйҷӨеҺ»Ca2+гҖҒMg2+пјҢеҸҜд»ҘеҫҖж°ҙдёӯеҠ е…ҘзҹізҒ°е’ҢзәҜзўұпјҢиҜ•еүӮеҠ е…Ҙж—¶е…ҲеҠ ______еҗҺеҠ ___________гҖӮ пјҲ2пјүжҲ‘еӣҪ规е®ҡйҘ®з”Ёж°ҙзҡ„зЎ¬еәҰдёҚиғҪи¶…иҝҮ25еәҰпјҢзЎ¬еәҰзҡ„иЎЁзӨәж–№жі•жҳҜпјҡе°Ҷж°ҙдёӯзҡ„Ca2+е’ҢMg2+йғҪзңӢдҪңCa2+пјҢ并е°Ҷе…¶жҠҳз®—жҲҗCaOзҡ„иҙЁйҮҸпјҢйҖҡеёёжҠҠ1еҚҮж°ҙдёӯеҗ«жңү10mg CaOз§°дёә1еәҰпјҢжҹҗеҢ–еӯҰе®һйӘҢе°Ҹз»„еҜ№жң¬ең°еҢәең°дёӢж°ҙзҡ„зЎ¬еәҰиҝӣиЎҢжЈҖжөӢгҖӮ е®һйӘҢдёӯж¶үеҸҠзҡ„йғЁеҲҶеҸҚеә”пјҡ M2+(йҮ‘еұһзҰ»еӯҗ)+EBTп№Ј(铬黑T)в•җMEBT+ и“қиүІ й…’зәўиүІ M2+(йҮ‘еұһзҰ»еӯҗ)+Y4п№Ј(EDTA)в•җMY2п№Ј MEBT++Y4п№Ј(EDTA)в•җMY2п№Ј+EBTп№Ј(铬黑T ) е®һйӘҢиҝҮзЁӢпјҡ в‘ еҸ–ең°дёӢж°ҙж ·е“Ғ25.00mLиҝӣиЎҢйў„еӨ„зҗҶпјҢеҶҷеҮәз”ұMg2+еј•иө·зҡ„жҡӮж—¶зЎ¬еәҰзҡ„ж°ҙз”ЁеҠ зғӯж–№жі•еӨ„зҗҶж—¶жүҖеҸ‘з”ҹеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸпјҡ_______________гҖӮ в‘Ўйў„еӨ„зҗҶзҡ„ж–№жі•жҳҜеҗ‘ж°ҙж ·дёӯеҠ е…Ҙжө“зӣҗй…ёпјҢз…®жІёеҮ еҲҶй’ҹпјҢз…®жІёзҡ„зӣ®зҡ„жҳҜ______________гҖӮ в‘ўе°ҶеӨ„зҗҶеҗҺзҡ„ж°ҙж ·иҪ¬з§»еҲ°250mLзҡ„й”ҘеҪўз“¶дёӯпјҢеҠ е…Ҙж°Ёж°ҙп№Јж°ҜеҢ–й“өзј“еҶІжә¶ж¶Іи°ғиҠӮpHдёә10пјҢж»ҙеҠ еҮ ж»ҙ铬黑Tжә¶ж¶ІпјҢз”Ё0.010 00molвҖўLп№Ј1зҡ„EDTAж ҮеҮҶжә¶ж¶ІиҝӣиЎҢж»ҙе®ҡпјҢж»ҙе®ҡз»ҲзӮ№ж—¶е…ұж¶ҲиҖ—EDTAжә¶ж¶І15.00mLпјҢеҲҷиҜҘең°дёӢж°ҙзҡ„зЎ¬еәҰдёә________________гҖӮ пјҲ3пјүжҹҗе·Ҙдёҡеәҹж°ҙдёӯеҗ«жңүCNп№Је’ҢCr2O72п№ЈзӯүзҰ»еӯҗпјҢйңҖз»ҸжұЎж°ҙеӨ„зҗҶиҫҫж ҮеҗҺжүҚиғҪжҺ’ж”ҫпјҢжұЎж°ҙеӨ„зҗҶеҺӮжӢҹз”ЁдёӢеҲ—жөҒзЁӢиҝӣиЎҢеӨ„зҗҶпјҡ 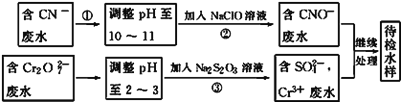 еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ в‘ жөҒзЁӢв‘ЎдёӯпјҢеҸҚеә”еҗҺж— ж°”дҪ“ж”ҫеҮәпјҢиҜҘеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸдёә______________________гҖӮ в‘Ўеҗ«Cr3+еәҹж°ҙйңҖиҝӣдёҖжӯҘеӨ„зҗҶпјҢиҜ·дҪ и®ҫи®ЎдёҖдёӘеӨ„зҗҶж–№жЎҲпјҡ________________________гҖӮ |
|
| 10. | иҜҰз»ҶдҝЎжҒҜ |
з”ұеҗ«зўҳеәҹж°ҙеҲ¶еҸ–зўҳй…ёй’ҫзҡ„дёҖз§Қе·ҘиүәеҰӮдёӢпјҡ в‘ҙ еҶҷеҮәKIO3еңЁж—Ҙеёёз”ҹжҙ»дёӯзҡ„дёҖдёӘйҮҚиҰҒеә”з”Ё________________________гҖӮ в‘ө жЈҖйӘҢвҖңеҗ«зўҳеәҹж°ҙвҖқдёӯжҳҜеҗҰеҗ«жңүеҚ•иҙЁI2зҡ„еёёз”ЁиҜ•еүӮжҳҜ________(еҶҷиҜ•еүӮеҗҚз§°)гҖӮ ⑶ йҖҡе…ҘSO2зҡ„зӣ®зҡ„жҳҜе°ҶI2иҝҳеҺҹдёәIпјҚпјҢиҜҘеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸдёә______________________гҖӮ в‘· е·Ҙиүәдёӯдә”з§Қзү©иҙЁзҡ„еҲ¶еӨҮеҸҚеә”дёӯпјҢдёҚж¶үеҸҠж°§еҢ–иҝҳеҺҹеҸҚеә”зҡ„жӯҘйӘӨжҳҜвҖңеҲ¶________вҖқгҖӮ в‘ё вҖңеҲ¶KI(aq)вҖқж—¶пјҢиҜҘжё©еәҰдёӢж°ҙзҡ„зҰ»еӯҗз§ҜдёәKwпјқ1.0Г—10пјҚ13пјҢKsp[Fe(OH)2]пјқ9.0Г—10пјҚ15гҖӮ дёәйҒҝе…Қ0.9 molВ·LпјҚ1 FeI2жә¶ж¶ІдёӯFe2+ж°ҙи§Јз”ҹжҲҗиғ¶зҠ¶зү©еҗёйҷ„I-пјҢиө·е§ӢеҠ е…ҘK2CO3еҝ…йЎ»дҝқжҢҒжә¶ж¶Ізҡ„pHдёҚеӨ§дәҺ______гҖӮ в‘№ вҖңеҲ¶KIO3жә¶ж¶ІвҖқеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸдёә__________________гҖӮ  в‘ә KClгҖҒKIO3зҡ„жә¶и§ЈеәҰжӣІзәҝеҰӮеӣҫжүҖзӨәгҖӮжөҒзЁӢдёӯз”ұвҖңKIO3(aq)вҖқеҫ—еҲ°KIO3жҷ¶дҪ“зҡ„ж“ҚдҪңжӯҘйӘӨдёә_____________________гҖӮ |
|
| 11. е®һйӘҢйўҳ | иҜҰз»ҶдҝЎжҒҜ |
е…°е°јй•ҚжҳҜдёҖз§ҚеёҰжңүеӨҡеӯ”з»“жһ„зҡ„з»Ҷе°Ҹжҷ¶зІ’з»„жҲҗзҡ„й•Қй“қеҗҲйҮ‘пјҢиў«е№ҝжіӣз”ЁдҪңжңүжңәзү©зҡ„ж°ўеҢ–еҸҚеә”зҡ„еӮ¬еҢ–еүӮгҖӮд»Ҙзәўеңҹй•ҚзҹҝпјҲдё»иҰҒжҲҗеҲҶдёәNiSгҖҒFeSе’ҢSiO2зӯүпјүдёәеҺҹж–ҷеҲ¶еӨҮе…°е°јй•Қзҡ„е·ҘиүәжөҒзЁӢеҰӮдёӢеӣҫжүҖзӨәпјҡ пјҲ1пјүеңЁеҪўжҲҗNiпјҲCOпјү4зҡ„иҝҮзЁӢдёӯпјҢзўіе…ғзҙ зҡ„еҢ–еҗҲд»·жІЎжңүеҸҳеҢ–пјҢеҲҷNiпјҲCOпјү4дёӯзҡ„Niзҡ„еҢ–еҗҲд»·дёә___________пјӣ пјҲ2пјүе·ІзҹҘзәўеңҹй•Қзҹҝз……зғ§еҗҺз”ҹжҲҗNi2O3пјҢиҖҢеҠ еҺӢй…ёжөёеҗҺжөёеҮәж¶ІAдёӯеҗ«жңүNi2+пјҢеҶҷеҮәжңүе…ій•Қе…ғзҙ зҡ„еҠ еҺӢй…ёжөёзҡ„еҢ–еӯҰеҸҚеә”ж–№зЁӢејҸ______________________пјӣ пјҲ3пјүеҗ‘жөёеҮәж¶ІAдёӯйҖҡе…ҘH2Sж°”дҪ“пјҢеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸжҳҜ____________________пјӣ пјҲ4пјүвҖңй«ҳжё©зҶ”иһҚвҖқж—¶иғҪеҗҰе°ҶйҖҡе…Ҙж°©ж°”жҚўдёәCO并иҜҙжҳҺеҺҹеӣ _____________________пјӣ пјҲ5пјүвҖңзўұжөёвҖқзҡ„зӣ®зҡ„жҳҜдҪҝй•Қй“қеҗҲйҮ‘дә§з”ҹеӨҡеӯ”з»“жһ„пјҢд»ҺиҖҢеўһејәеҜ№ж°ўж°”зҡ„ејәеҗёйҷ„жҖ§пјҢжӯӨиҝҮзЁӢ дёӯеҸ‘з”ҹеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸдёә___________________гҖӮжөёеҮәеҸҚеә”жүҖз”Ёзҡ„NaOHжә¶ж¶Ізҡ„жө“еәҰиҰҒеӨ§пјҢиӢҘNaOHжә¶ж¶ІиҫғзЁҖж—¶пјҢеҲҷдјҡдә§з”ҹе°‘йҮҸзҡ„AlпјҲOHпјү3жІүж·ҖиҖҢйҳ»жӯўжөёеҮәеҸҚеә”зҡ„жҢҒз»ӯиҝӣиЎҢпјҢиҜ·з”ЁеҢ–еӯҰеҸҚеә”еҺҹзҗҶеҠ д»Ҙи§ЈйҮҠпјҡ________________________гҖӮ пјҲ6пјүжөёеҮәж¶ІBеҸҜд»Ҙеӣһ收пјҢйҮҚж–°з”ҹжҲҗй“қд»ҘдҫҝеҫӘзҺҜеҲ©з”ЁгҖӮиҜ·и®ҫи®Ўз®ҖеҚ•зҡ„еӣһ收жөҒзЁӢпјҡ жөёеҮәж¶ІBвҶ’________________________гҖӮпјҲзӨәдҫӢпјҡCuOCu2+Cuпјү |
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
жҹҗеҢ–еӯҰе…ҙи¶Је°Ҹз»„еҲ©з”ЁзЎ«й“Ғзҹҝзғ§жёЈ(дё»иҰҒжҲҗеҲҶдёә иҜ·еӣһзӯ”дёӢеҲ—й—®йўҳ пјҲ1пјүй…ёжә¶иҝҮзЁӢдёӯеҸ‘з”ҹеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸжҳҜпјҡ______пјӣ пјҲ2пјүдёәдәҶжҸҗй«ҳй…ёжөёж—¶зҡ„йҖҹзҺҮпјҢйҷӨдәҶйҖӮеҪ“еўһеӨ§зЎ«й…ёзҡ„жө“еәҰеӨ–пјҢиҝҳеҸҜд»ҘйҮҮеҸ–зҡ„жҺӘж–Ҫжңүпјҡ______ пјҲ3пјүжЈҖйӘҢжӯҘйӘӨв…ўеҸҚеә”еҗҺзҡ„жә¶ж¶ІдёӯйҮ‘еұһйҳізҰ»еӯҗзҡ„иҜ•еүӮжҳҜпјҡ______пјӣ пјҲ4пјүжӯҘйӘӨв…ӨдёӯпјҢ пјҲ5пјүжӯҘйӘӨв…ӨеҸҚеә”жҲҗ пјҲ6пјүж¬ІжөӢе®ҡзЎ«й“Ғзҹҝзғ§жёЈдёӯFeе…ғзҙ зҡ„иҙЁйҮҸеҲҶж•°пјҢз§°еҸ–wgж ·е“ҒпјҢе……еҲҶй…ёжә¶гҖҒж°ҙжә¶еҗҺиҝҮж»ӨпјҢеҗ‘ж»Өж¶ІдёӯеҠ е…Ҙи¶ійҮҸзҡ„ |
|
- жҘҡйӣ„еёӮй«ҳдәҢеҢ–еӯҰдёҠеҶҢжңҲиҖғиҜ•еҚ·еҲ·йўҳз»ғд№
- еҢ—дә¬2018е№ҙй«ҳдёүдёҠеӯҰжңҹеҢ–еӯҰжңҹдёӯиҖғиҜ•зҪ‘дёҠиҖғиҜ•з»ғд№
- еҸҢеі°еҺҝ第дёҖдёӯеӯҰй«ҳдәҢеҢ–еӯҰжңҲиҖғжөӢйӘҢпјҲ2019е№ҙдёӢжңҹпјүеҗҢжӯҘз»ғд№
- еҚ—жҳҢеёӮиҜ•еҚ·еёҰзӯ”жЎҲе’Ңи§Јжһҗ
- 2018иҮі2019е№ҙй«ҳдәҢдёӢеҶҢжңҹжң«иҖғиҜ•еҢ–еӯҰе…Қиҙ№иҜ•еҚ·пјҲе№ҝиҘҝеҚ—е®ҒеёӮвҖң4NвҖқй«ҳдёӯиҒ”еҗҲдҪ“пјү
- е№ҝиҘҝйҡҶжһ—еҺҝ第дәҢдёӯеӯҰй«ҳдёҖеҢ–еӯҰдёҠеҶҢжңҹжң«иҖғиҜ•ж‘ёеә•иҖғиҜ•йўҳеҗҢжӯҘи®ӯз»ғ
- 2019еұҠй«ҳдёүеүҚеҚҠжңҹ第дёүж¬ЎжңҲиҖғеҢ–еӯҰиҖғиҜ•пјҲеӨ©жҙҘеёӮ第дёҖдёӯеӯҰпјү
- еӨҜеҹәжҸҗиғҪй«ҳдёүеҢ–еӯҰдёҠеҶҢдё“йўҳз»ғд№ йўҳе…Қиҙ№иҜ•еҚ·



