2017-2018年科粤版初三化学第八单元第二节基础练习
| 1. 选择题 | 详细信息 |
将一套如图所示的密闭装置放在天平上,使天平平衡,经过一段时间后出现的情况是( ) A. 指针偏左,食盐溶液一定变浓,烧碱变质 B. 指针偏左,食盐溶液一定变浓,烧碱潮解 C. 指针偏右,食盐溶液一定变浓,烧碱潮解 D. 指针偏右,食盐溶液一定饱和,烧碱潮解 |
|
| 2. 选择题 | 详细信息 |
|
浓盐酸敞口放置一段时间后,下列关于浓盐酸溶液pH变化的说法正确的是 A.变大 B.不变 C.变小 D. 先变小后变大 |
|
| 3. 选择题 | 详细信息 |
|
类比常常应用在化学学习中,下列说法正确的是( ) A.浓盐酸敞口放置后溶液浓度减小;浓硫酸敞口放置后溶液浓度也减小 B.二氧化锰能加快氯酸钾的分解;二氧化锰也能加快高锰酸钾的分解 C.铝制品表面易形成致密的氧化铝薄膜,很耐腐蚀;铁制品表面易形成铁锈, 也很耐腐蚀 D.4g 硫与 4g 氧气充分反应后生成 8g 气体;4g 碳与 4g 氧气充分反应后也生成8g 气体 |
|
| 4. 选择题 | 详细信息 |
|
常温下,某反应 M+碱→N+盐,其中 M、N 所属的物质类别不可能是( ) A.氧化物、氧化物 B.盐、碱 C.酸、氧化物 D.单质、单质 |
|
| 5. 选择题 | 详细信息 |
|
向 H2SO4 和 CuSO4 的混合溶液中,逐滴加入 NaOH 溶液,下图曲线正确的是( ) A. 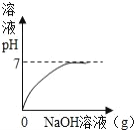 B. B. C. C. D. D. |
|
| 6. 选择题 | 详细信息 |
|
盛浓硫酸和浓盐酸的两个试剂瓶敞口放置一段时间,则两瓶溶液 A.质量都增加了 B.溶质的质量分数都变大了 C.溶质的质量分数都变小了 D.溶质的质量分数都不变 |
|
| 7. 选择题 | 详细信息 |
|
氢氧化钙是一种重要的碱,也是一种重要的建筑材料.下列做法或说法错误 的是( ) A.在农业生产中,常用熟石灰来改良酸性土壤 B.在建筑业中,常用石灰将来抹墙,为使墙壁快点干燥,常在室内生个炭火盆 C.为使氢氧化钙溶液底部的少量固体溶解,通常采用升温的方法 D.在工业生产中,常用氢氧化钙来中和酸性废水,防止污染 |
|
| 8. 选择题 | 详细信息 |
|
滴有酚酞的石灰水与足量的下列物质充分反应,酚酞仍显红色的是 A.稀硫酸 B.盐酸 C.硫酸铜溶液 D.碳酸钠溶液 |
|
| 9. 选择题 | 详细信息 |
|
在氧化铜和铁粉的化合物中,加入一定量的稀硫酸,微热,待反应停止后过滤,滤出不溶物后,再往滤液里加入一枚铁钉,过一会儿将铁钉取出,发现铁钉无变化,则正确的叙述是 A.不溶物一定是铜 B.不溶物一定是铁 C.滤液是硫酸亚铁溶液 D.滤液是硫酸铜和硫酸亚铁混合物 |
|
| 10. 选择题 | 详细信息 |
|
生活中产生的污垢,常可用稀盐酸来清洗.但下列有一种污垢是不宜用稀盐 酸来清洗的,它是( ) A.不锈钢茶杯内的茶垢 B.陶瓷水槽内的黄色铁锈斑 C.保温瓶内的水垢(主要成分是 CaCO3) D.长期盛放石灰水试剂瓶内壁上的白色固体 |
|
| 11. 选择题 | 详细信息 |
|
下列物质中,与CO2、CuCl2溶液、Na2CO3溶液都能发生反应,且都有明显现象的是( ) A.NaOH B.Ca(OH)2 C.H2SO4 D.HCl |
|
| 12. 选择题 | 详细信息 |
|
在 M+H2SO4(稀)=Fe2(SO4)3+N(M、N 分别代表一种物质)反应中,M 可能 是下列物质中的( ) ①Fe ②Fe2O3 ③Fe(OH)3 ④FeCl2 A.①② B.②③ C.①②③ D.全部 |
|
| 13. 选择题 | 详细信息 |
|
对于反应:X + 2 NaOH == 2 Y + Cu(OH)2↓,下列分析中正确的是 A.X中一定含有氧元素 B.X和Y的相对分子质量之差为18 C.Y中一定含有钠元素 D.Y可能是Na2SO4 |
|
| 14. 选择题 | 详细信息 |
|
氢氧化钠是重要的化工原料,其俗称是 A. 纯碱 B. 烧碱 C. 小苏打 D. 熟石灰 |
|
| 15. | 详细信息 |
某课外兴趣小组的同学,通过实验测定浓硫酸吸水性的有关数据,绘制成下图的函数图像,其中横坐标表示时间,纵坐标可以表示:①溶质的质量分数;②溶液的质量;③溶液的体积;④溶液中所含水的质量.其中正确的是 ( ) A. ①② B. ②③ C. ②③④ D. ①②③④ |
|
| 16. 选择题 | 详细信息 |
取一滤纸条,等间距滴10滴紫色石蕊试液,然后装入玻璃管中(如图所示),两端管口同时放入分别蘸有浓氨水和浓盐酸的棉球,几秒后观察到图示现象.下列说法不正确的是( ) A.氨水的pH大于7,盐酸的pH小于7 B.浓氨水和浓盐酸都易挥发 C.氨分子和氯化氢分子的运动速率相等 D.酸、碱能使紫色石蕊试液显示不同颜色 |
|
| 17. 填空题 | 详细信息 |
构建知识网络是学习化学的重要方法之一.某同学在学习酸、碱和盐的化学 性质后,归纳的知识网络如图,图中“﹣”两端的物质可以反应.请帮助该同学进 行完善和纠正. (1)图中的 A 类物质可能是_____,请列举一个反应的化学方程式_____. (2)该同学针对金属和酸的反应,写出了下面一个化学方程式:Cu+H2SO4(稀)═CuSO4+H2↑,有的同学认为该化学方程式不正确,理由是_____. (3)老师告诉同学们:对于酸和盐的反应,可以用厨房中的常见物品进行实验, 其中能发生反应的两种物品是_____和_____(填名称或俗称). |
|
| 18. 填空题 | 详细信息 |
| 浓盐酸的质量为 A,敞口放置一段时间后,测得其质量为 B,则 A_____B(填“<”“>”或“=”,下同),浓硫酸的质量分数为 A,敞口放置一段时间后的质 量分数为 B,则 A_____B. | |
| 19. 填空题 | 详细信息 |
|
化学就在我们身边,从①H2SO4、②Ca(OH)2、③NaCl、④CaCO3、⑤CH4,五种物质中学出与下列用途对应物质的序号填写在空白处: (1)可用作金属制品除锈的是_____. (2)我国“西气东输”的气体主要成分是_____. (3)欲除去溶液中含有的少量盐酸,在不用酸碱指示剂的条件下应加入的试剂是_____. |
|
| 20. 填空题 | 详细信息 |
| 氢氧化钠是一种白色固体,它俗称_____.该物质露置在空气中易吸水潮 解.在实验室可用于干燥气体,但 CO2 不能用它干燥,原因是_____(用化学 方程式表示) | |
| 21. 填空题 | 详细信息 |
|
铁是最常见的金属,有广泛的用途. (1)铁在潮湿的空气中最容易生锈,试用稀盐酸除锈的化学方程式是_____. 一般情况下,两种活动性不同的金属在潮湿环境中接触时,活动性强的金属首先 被腐蚀.造船工业为了避免乱串的钢铁外壳被腐蚀,通常在轮船外壳镶嵌的金属 是_____(填字母序号) A 银 B 铜 C 铅 D 锌 (2)向硝酸银,硝酸铜,硝酸镁的混合溶液中加入一些铁粉,待完全反应后, 再过滤,下列情况说法正确的是_____. A 滤纸上有 Ag,滤液中有 Ag+、Cu2+、Fe2+、Mg2+ B 滤纸上有 Ag、Cu,滤液中有 Ag+、Fe2+、Mg2+ C 滤纸上有 Ag、Cu、Fe,滤液中有 Fe2+、Mg2+ D 滤纸上有 Ag、Cu、Fe、Mg,滤液中有 Fe2+. |
|
| 22. 填空题 | 详细信息 |
(7分)下图是某实验中各物质间的转化关系: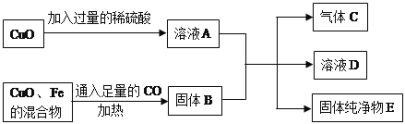 请回答下列问题: (1)写出氧化铜与稀硫酸反应的化学方程式 。 (2)气体C的化学式是 。 (3)溶液D中一定含有的溶质是 (写化学式); 可能有的溶质是 。 (4)写出得到气体C的化学方程式 。 |
|
| 23. 填空题 | 详细信息 |
| 敞口放置的浓盐酸和浓硫酸,一段时间后,质量分数会变小.原因是浓盐酸 具有_____;浓硫酸具有_____. | |
| 24. 填空题 | 详细信息 |
|
氢氟酸(HF 的水溶液)是工业上一种常见的酸,在国防和民用工业上有广泛的用途. (1)氢氟酸能在玻璃上刻划美丽的图案,它与玻璃中的二氧化硅反应生成了四 氟化硅气体和水,写出该反应的化学方程式_____. (2)氢氟酸具有强烈的腐蚀性,如果不小心沾在皮肤上,要立即用水冲洗,再 用 3%﹣5%的_____(填化学式)溶液清洗. (3)要配制(2)中的清洗用溶液 100g,至少需要称取溶质的质量为_____g. |
|
| 25. 填空题 | 详细信息 |
|
酸是一类非常重要的化合物,请回答下列问题 (1)向三氧化二铁中放入足量盐酸,充分反应后,观察到的现象_______________________,反应的化学方程式是______________________________________。 (2)白醋、柠檬酸溶液也能与三氧化二铁发生类似反应,说明白醋、柠檬酸溶液和盐酸中都含有的离子是________(填离子符号)。 (3)甲酸可解离出H+和HCOO—,甲酸溶液与氢氧化钠反应的化学方程式为 HCOOH+NaOH=HCOONa+H2O,请写出甲酸溶液与镁反应的方程式___________________。 |
|
| 26. 实验探究题 | 详细信息 | ||||||||||||
化学小组的同学探究二氧化碳与氢氧化钠的反应,实验方案如下:
|
|||||||||||||
初中化学 试卷推荐
- 2019届九年级上学期期末联考化学试卷完整版(甘肃省静宁县第二大片区)
- 安徽省宿州市埇桥区教育集团2020-2021年初三上册第三次月考化学在线测验完整版
- 山东省济宁市鱼台县实验中学2020-2021年九年级上半期期中化学在线测验完整版
- 2019届初三下半年中考模拟化学试卷完整版(湖北省十堰市官渡镇中学)
- 2019-2020年初三上半年期末化学题开卷有益(湖北省鄂州市梁子湖区)
- 2019-2020年九年级前半期期中化学在线测验完整版(山东省菏泽市成武县)
- 初三下学期期中化学题免费试卷(2019-2020年黑龙江省齐齐哈尔市建华区朝鲜族学校)
- 2020年5月黑龙江省哈尔滨市南岗区萧红中学中考模拟化学考题
最近更新




