江西高一化学月考测验(2020年下册)免费试卷完整版
| 1. 选择题 | 详细信息 |
|
含有共价键的离子化合物是( ) A.NaCl B.NH3 C.NH4Cl D.O2 |
|
| 2. 选择题 | 详细信息 |
|
元素周期表是学习化学的重要工具,下列关于元素周期表的说法不正确的是( ) A.可以在过渡元素区域寻找优良的催化剂和耐高温耐腐蚀的合金材料 B.ⅠA族是包含元素种类最多的纵行 C.第2纵行全部为金属元素 D.根据元素周期表可以预测元素的存在及其性质 |
|
| 3. 选择题 | 详细信息 |
|
某元素最高价氧化物对应的水化物的分子式是H4RO4,则其气态氢化物的分子式是( ) A.RH3 B.RH4 C.H2R D.HR |
|
| 4. 选择题 | 详细信息 |
|
下列说法正确的是( ) A.等质量的硫蒸气和硫固体分别与氧气完全燃烧,后者放出的热量多 B.放热反应在常温下一定很容易发生 C.由C(石墨,s)=C(金刚石,s)反应吸热可知,金刚石比石墨稳定 D.酒驾是一种极不负责任的危害社会的行为,利用测酒仪可以检测酒精含量,利用的是酒精的还原性 |
|
| 5. 选择题 | 详细信息 |
|
对化学学科的学习从思维角度去看,本质是对化学符号的操控,对以下化学符号的表达正确的是( ) A.F-的离子结构示意图: B.NH4Cl的电子式:  C.次氯酸的结构式:H-Cl-O D.H2O2的电子式: |
|
| 6. 选择题 | 详细信息 |
|
X、Y、Z、W是短周期元素,其原子序数依次增大,X原子最外层电子数是其K层电子数的3倍,Y原子的K层电子数与M层相同。Z单质是良好的半导体材料,W与X属于同一主族,下列说法正确的是( ) A.W元素在周期表中的位置是第三周期第VI族 B.元素W的最高价氧化物对应水化物的酸性比Z的强 C.元素简单气态氢化物的沸点W比X的高 D.化合物YX、ZX2、WX3中化学键类型相同 |
|
| 7. 选择题 | 详细信息 |
|
X、Y、Z、W是原子序数依次增大的四种短周期元素,其中只有一种是金属元素,X的某种核素无中子,X、W同主族且能形成一种离子化合物WX;Y的气态氢化物、最高价氧化物的水化物可反应生成一种盐;Z原子的最外层电子数与其电子总数之比为3∶4。下列说法中正确的是( ) A.原子半径:W>Z>Y>X B.氢化物稳定性:Y>Z C.X与Z可形成10电子和18电子分子 D.WY3中只有离子键没有共价键 |
|
| 8. 选择题 | 详细信息 |
锌-空气电池(原理如图)适宜用作城市电动车的动力电源,放电时Zn转化为ZnO。则该电池放电时下列说法正确的是( )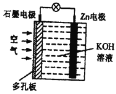 A.将电能转化为化学能 B.电子由Zn电极经导线流向石墨电极 C.氧气在石墨电极上发生氧化反应 D.该电池放电时OH-向石墨电极移动 |
|
| 9. 选择题 | 详细信息 |
微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极材料分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应式为Zn+2OH−−2e−===Zn(OH)2,Ag2O+H2O+2e−===2Ag+2OH−。下列叙述中正确的是( ) A. 在使用过程中,电解质KOH不断被消耗 B. 使用过程中,电子由Ag2O极经外电路流向Zn极 C. Zn电极发生还原反应,Ag2O电极发生氧化反应 D. Zn是负极,Ag2O是正极 |
|
| 10. 选择题 | 详细信息 |
|
下列条件一定能使反应速率加快的是( ) ①增加反应物的物质的量②升高温度③缩小反应容器的体积④加入生成物⑤加入MnO2 A.全部 B.①②⑤ C.②③ D.② |
|
| 11. 选择题 | 详细信息 |
|
已知反应A(s)+3B(g) A.2min末,气体D在标准状况下的体积无法计算 B.用物质B、C、D来分别表示该反应的速率之比为3:2:1 C.由于A为纯固体,物质的量浓度是常数,故无法利用A的相关物理量的变化来表示该反应的速率大小 D.单位时间内,每消耗0.3molB气体,同时消耗0.1molD气体,此时该反应达到最大限度 |
|
| 12. 选择题 | 详细信息 |
|
在一定条件下,向恒容密闭容器中充入1molN2与4molH2,发生化学反应N2(g)+3H2(g) A.V(N2)=V(NH3) B.单位时间内,断裂1molN C.此时,容器内气体的平均摩尔质量不再变化 D.此时,该反应不一定达到了化学平衡状态 |
|
| 13. 选择题 | 详细信息 |
|
下列关于甲烷的叙述中,错误的是( ) A.通常情况下,甲烷跟强酸、强碱、强氧化剂不反应 B.甲烷化学性质比较稳定,不能被任何氧化剂氧化 C.甲烷的二氯代物不存在同分异构体,说明甲烷是正四面体结构而不是平面正方形结构 D.光照条件下甲烷与Cl2反应的四种有机产物都难溶于水 |
|
| 14. 选择题 | 详细信息 |
|
下列各组物质相互间一定互为同系物的是( ) A.淀粉和纤维素 B.C4H10与C10H22 C.C3H6与C4H8 D.蔗糖和麦芽糖 |
|
| 15. 选择题 | 详细信息 |
|
将W1g光亮的铜丝在空气中加热一段时间后,迅速伸入下列物质中,取出干燥,如此反复几次,最后取出铜丝用蒸馏水洗涤、干燥,称得其质量为W2g。实验时由于所伸入的物质不同,铜丝的前后质量变化可能不同,下列所插物质与铜丝的质量关系正确的是( ) A.NaOH溶液,W1=W2 B.NaHSO4溶液,W1<W2 C.无水乙醇,W1=W2 D.CO,W1>W2 |
|
| 16. 选择题 | 详细信息 |
|
法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得2016年诺贝尔化学奖。轮烷是一种分子机器的“轮子”,合成轮烷的基本原料有丙烷、戊醇、苯,下列说法不正确的是( ) A.苯与足量氢气在镍催化作用下会发生加成反应生成环己烷 B.丙烯能使溴水褪色 C.戊醇与乙醇都含有羟基 D.苯与溴水在催化剂作用下会发生取代反应 |
|
| 17. 填空题 | 详细信息 |
|
按要求回答问题: (1)氢氧燃料电池以KOH溶液作电解质溶液时, ①负极反应式为___; ②正极反应式为___; (2)葡萄糖生物发酵产生乙醇的化学方程式___。 (3)乙酸和乙醇在浓硫酸和加热条件下反应的化学方程式___。 |
|
| 18. 解答题 | 详细信息 | ||||||||||||||||||||||||
下表为元素周期表的一部分,根据表中所列出的元素回答下列问题。
|
|||||||||||||||||||||||||
| 19. 解答题 | 详细信息 | ||||||||||||||
|
(1)反应3Fe(s)+4H2O(g) ①保持体积不变充入Ne,其反应速率___。 ②保持压强不变充入Ne,其反应速率____。 (2)在一定条件下发生反应:6NO(g)+4NH3(g) 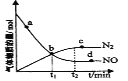 (3)一定条件下,在2L密闭容器内,发生反应2NO2(g)
|
|||||||||||||||
| 20. 解答题 | 详细信息 |
从本质入手看物质及其能量的变化,可以让我们更加深入的去理解所学知识的内涵及外延应用。对于《原电池》这部分知识也是如此,如图是原电池的基本构造模型: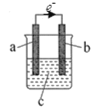 (1)若a和b的电极材料为Al或Mg。 ①若c为稀NaOH溶液时,则a的电极材料为__,该极电极方程式为___。 ②若c为稀H2SO4时,则a的电极材料为___,该极电极方程式为__。 (2)对于原电池的应用,以下说法正确的是__。 A.选择构成原电池两极材料时,必须选择活泼性不同的两种金属材料 B.构成原电池时,负极材料的活泼性一定比正极材料的强 C.构成原电池时,作为负极材料的金属受到保护 D.从能量转化角度去看,如图的氧化还原反应能量变化曲线,则不能够设计原电池  |
|
| 21. 推断题 | 详细信息 |
用石油裂化和裂解过程得到的乙烯、丙烯来合成丙烯酸乙酯的路线如图: 根据以上材料和你所学的化学知识,回答下列问题: (1)乙烯的结构简式为___,官能团的名称是___。 (2)乙烯是重要的工业原料,下列有关乙烯叙述不正确的是(__________) A.常温常压下是气体 B.能使溴的四氯化碳溶液褪色 C.可使酸性高锰酸钾溶液发生加成反应而褪色 D.在氧气中燃烧有明亮的火焰 (3)除去甲烷中的乙烯所用的试剂是___(填序号)。 A.稀硫酸 B.溴水 C.水 D.酸性高锰酸钾溶液 (4)反应①的化学方程式是___,反应类型是____。 (5)反应④的化学方程式是___,反应类型是____。 |
|
最近更新



