江苏2019年高一上学期化学月考测验试卷完整版
| 1. 选择题 | 详细信息 |
|
CaO常用于食品的干燥。CaO属于( ) A. 碱 B. 酸 C. 盐 D. 氧化物 |
|
| 2. 选择题 | 详细信息 |
|
如果你家里的食用花生油不小心混入了大量的水,利用你所学的知识,最简便的分离方法是( ) A.  B. C. D.  |
|
| 3. 选择题 | 详细信息 |
|
下列反应属于氧化还原反应的是( ) A. SO3+ H2O= H2SO4 B. NH4Cl C. Fe+CuSO4= FeSO4+Cu D. NaOH+HNO3=NaNO3+H2O |
|
| 4. 选择题 | 详细信息 |
|
为了除去粗盐中的CaCl2、MgCl2、Na2SO4及泥沙,可将粗盐溶于水,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤,不正确的操作顺序是 A. ③②①⑤④ B. ③①②⑤④ C. ②③①⑤④ D. ②①③⑤④ |
|
| 5. 选择题 | 详细信息 |
|
溶液、胶体和浊液这三种分散系的本质区别是( ) A. 是否有丁达尔现象 B. 是否能通过滤纸 C. 分散质粒子的大小 D. 是否均一、透明、稳定 |
|
| 6. 选择题 | 详细信息 |
|
工业上可用金属钠和氯化钾反应制备金属钾,其化学方程式为Na+KCl A. 置换反应 B. 复分解反应 C. 分解反应 D. 化合反应 |
|
| 7. 选择题 | 详细信息 |
实验操作的规范是实验的基本要求。下列实验操作正确的是 |
|
| 8. 选择题 | 详细信息 |
|
下列说法正确的是 (NA为阿伏加德罗常数的值) ( ) A. 28 g氮气含有的原子数为NA B. 4 g金属钙变成钙离子时失去的电子数为0.1 NA C. 1 mol O2分子的质量等于1 mol氧原子的质量 D. 24 g O2 和24 g O3所含的氧原子数目相等 |
|
| 9. 选择题 | 详细信息 |
|
下列电离方程式正确的是( ) A. H2SO4 = 2H+ + S6+ + 4O2- B. NaHCO3 =Na++ H+ + CO3- C. Ba(OH)2 = Ba2+ + 2OH- D. Na2CO3 = Na2+ + CO32- |
|
| 10. 选择题 | 详细信息 |
|
下列说法中正确的是( ) A. 某溶液与NaOH溶液共热,产生能使湿润的红色石蕊试纸变蓝的气体,说明原溶液中存在NH4+ B. 某溶液中加入盐酸后有无色气体产生,该气体能够使澄清的石灰水变浑浊,则原溶液中含CO32- C. 用铂丝蘸取某溶液在酒精灯的火焰上灼烧时,火焰呈黄色,说明原溶液中只含有Na+,不含有K+ D. 某溶液中加入BaCl2溶液时,产生白色沉淀,加稀硝酸沉淀不溶解,说明原溶液中存在SO42- |
|
| 11. 选择题 | 详细信息 |
|
下列物质水溶液能导电,但该物质属于非电解质的是( ) A. NaOH B. NaCl C. NH3 D. CO2 |
|
| 12. 选择题 | 详细信息 |
|
下列说法错误的是(NA为阿伏加德罗常数的值) ( ) A. 硫酸的摩尔质量是98 g B. 1molO2的质量是32g/mol C. 2g氢气所含原子数目为2NA D. 标准状况下,11.2LCH4的物质的量为0.5mol |
|
| 13. 选择题 | 详细信息 |
|
实验室制取O2和Cl2的化学反应方程式分别为①2KClO3 A. 均为氧化还原反应 B. ②中MnO2为还原剂 C. ①中反应前后MnO2质量不发生变化 D. ①中反应前后MnO2化学性质改变 |
|
| 14. 填空题 | 详细信息 |
|
选择下列实验方法分离物质,将分离方法的序号填在横线上 A 萃取分液法 B 结晶法 C 分液法 D 蒸馏法 E 过滤法 ①__ ___分离饱和食盐水与沙子的混合物。 ②___ _分离水和汽油的混合物。 ③____ __分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。 ④___ __从碘的水溶液里提取碘。 ⑤____ __从硝酸钾和氯化钠的混合液中获得硝酸钾。 |
|
| 15. 填空题 | 详细信息 |
| 相同物质的量的NH3和H2S的质量比 ______ ,分子个数比为 ______ ,同温同压下的体积比 ______ ,所含氢原子的个数比为 ______ . | |
| 16. 综合题 | 详细信息 |
实验室需要制备纯净的氯化钾。现有含少量KBr和K2SO4的氯化钾样品,按照下图所示的实验方案进行提纯。 (1)KCl中K+检验时,透过蓝色钴玻璃观察焰色为:___________。 (2) 若用硝酸钡来代替氯化钡,请判断是否可行:______(填“是”或“否”),并说明理由:________。 (3)在过滤后的滤液中通入过量氯气即可将滤液中的KBr杂质除去,发生的反应为:2KBr + Cl2 = 2KCl + Br2,如果按是否有元素的化合价发生了变化来分类,该反应属于_______________反应。 (4) 某同学认为该实验方案中加适量氯化钡溶液不容易控制,应加入过量氯化钡溶液,他的思路如下。请写出沉淀A的化学式:A:_________。 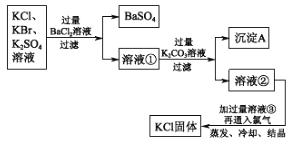 |
|
| 17. 计算题 | 详细信息 |
|
实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为MnO2+4HCl=MnCl2+Cl2+2H2O,欲制得标准状况下4.48L氯气。 (1)氯气的物质的量是多少___? (2)参与反应的HCl的物质的量是多少___? |
|
最近更新



