甘肃省武威第一中学2020届高三12月月考化学试卷带参考答案和解析
| 1. 选择题 | 详细信息 |
|
下列有关说法错误的是( ) A.成语“百炼成钢”、“蜡炬成灰”中均包含了化学变化 B.常温下,成语“金戈铁马”中的金属能溶于浓硝酸 C.谚语“雷雨肥庄稼”,其过程中包含了氧化还原反应 D.《荷塘月色》中“薄薄的青雾浮起在荷塘里”中的“青雾”属于胶体 |
|
| 2. 选择题 | 详细信息 |
|
下列各组变化中,前者是物理变化,后者是化学变化的是( ) A.碘的升华、石油的分馏 B.NH4Cl溶液除铁锈、食盐水导电 C.蛋白质溶液中加饱和(NH4)2SO4溶液、蓝色的胆矾常温下变白 D.热的饱和KNO3溶液降温析出晶体、二硫化碳洗涤试管内壁上的硫 |
|
| 3. 选择题 | 详细信息 |
|
下列有关物质性质与用途具有对应关系的是 A. FeSO4具有氧化性,可用作食品抗氧化剂 B. SiO2熔点高、硬度大,可用于制光学仪器 C. Al(OH)3具有弱碱性,可用于制胃酸中和剂 D. NH3具有还原性,可用作制冷剂 |
|
| 4. 选择题 | 详细信息 |
|
同温同压下,m g甲气体和2m g乙气体所占体积之比为1∶2,根据阿伏加德罗定律判断,下列叙述不正确的是( ) A. 甲与乙的相对分子质量之比为1∶1 B. 同温同压下,甲和乙的密度之比是1∶1 C. 同温同体积下,等质量的甲和乙的压强之比是1∶1 D. 等质量的甲和乙中的原子数之比是1∶1 |
|
| 5. 选择题 | 详细信息 |
|
常温下,下列各组离子在指定溶液中一定能大量共存的是( ) A. c(H+)<c(OH-)的溶液中:Na+、K+、SO42-、ClO- B. 能使酚酞变红的溶液中:Na+、Cu2+、CO32-、NO3- C. 0.1 mol·L-1 FeCl3溶液中:K+、NH4+、I-、SCN- D. 加入铝粉能产生氢气的溶液中:NH4+、Fe2+、NO3-、SO42- |
|
| 6. 选择题 | 详细信息 |
|
下列物质的转化在给定条件下不能实现的是( ) A.NH3 B.浓盐酸 C.Al2O3 D.葡萄糖 |
|
| 7. 选择题 | 详细信息 |
|
ClO2是一种新型水处理剂,工业上用NaClO2与盐酸反应制备ClO2的反应如下: ①5NaClO2+4HCl(稀)===5NaCl+4ClO2↑+2H2O; ②NaClO2+4HCl(浓)===NaCl+2Cl2↑+2H2O。 下列说法中正确的是( ) A. 两种反应中HCl均是还原剂 B. 盐酸浓度越大,还原性越强 C. ①中氧化产物与还原产物物质的量之比为4∶5 D. ②中每生成1 mol Cl2转移2 mol电子 |
|
| 8. 选择题 | 详细信息 |
|
取m g相对原子质量为M的某金属与足量稀硫酸反应,在标准状况下产生a L氢气,该反应生成的硫酸盐中金属元素的化合价为( ) A. +aM/(22.4m) B. +am/(11.2M) C. +11.2m/(aM) D. +aM/(11.2m) |
|
| 9. 选择题 | 详细信息 |
|
下列溶液中,溶质的物质的量浓度不是1 mol/L的是( ) A. 10 g NaOH固体溶解在水中配成250 mL溶液 B. 将80 g SO3溶于水并配成1 L的溶液 C. 将0.5 mol/L的NaNO3溶液100 mL加热蒸发掉50 g水的溶液 D. 标况下,将22.4 L氯化氢气体溶于水配成1 L溶液 |
|
| 10. 选择题 | 详细信息 |
|
下列化学反应的离子方程式正确的是 A. 0.01mol/L NH4Al(SO4)2溶液与0.02mol/LBa(OH)2溶液等体积混合产生沉淀:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3•H2O B. 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+ C. NH4HCO3溶液与过量NaOH溶液共热:NH4++OH- D. 浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+ |
|
| 11. 选择题 | 详细信息 |
|
依据元素周期律进行推断,下列不正确的是( ) A.原子半径:Cl<S B.氧化性:Cl2>S C.稳定性:HBr>HI D.酸性:HCl>HF |
|
| 12. 选择题 | 详细信息 |
|
下列物质中所有原子最外层达到8电子稳定结构的化合物是( ) A.NH3 B.P4 C.PCl5 D.CCl4 |
|
| 13. 选择题 | 详细信息 |
|
设NA为阿伏伽德罗常数的值。下列说法正确的是 A.1molCl2与足量Fe反应,转移的电子数为3NA B.在反应KIO3+6HI=3I2+KI+3H2O中,每生成3molI2转移电子数为5NA C.向FeI2溶液中通入适量Cl2,当有1molFe2+被氧化时,共转移电子的数目为NA D.1molCl2参加反应转移电子数一定为2NA |
|
| 14. 选择题 | 详细信息 |
|
关于反应过程中的先后顺序,下列评价正确的是 A.向浓度都为0.1mol/L的FeCl3和CuCl2加入铁粉,溶质CuCl2首先与铁粉反应 B.向过量的Ba(OH)2溶液中滴加少量的KAl(SO4)2溶液,开始没有白色沉淀生成 C.向浓度都为0.1mol/L 的Na2CO3和NaOH的混合溶液通入CO2气体,NaOH首先反应 D.向浓度为0.1mol/L的FeCl3溶液中,加入质量相同、颗粒大小相同的铁和铜,铜单质首先参加反应 |
|
| 15. 选择题 | 详细信息 |
某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),设计了如下流程: 下列说法不正确的是( ) A. 溶解烧渣选用足量硫酸,试剂X选用铁粉 B. 固体1中一定含有SiO2,控制pH是为了使Al3+转化为Al(OH)3,进入固体2 C. 从溶液2得到FeSO4·7H2O产品的过程中,须控制条件防止其氧化和分解 D. 若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4·7H2O |
|
| 16. 选择题 | 详细信息 |
|
化学用语是学好化学知识的重要基础,下列有关化学用语表示正确的有( ) ①用电子式表示HCl的形成过程: ②MgCl2的电子式: ④乙烯、乙醇结构简式依次为:CH2=CH2、C2H6O ⑤S2﹣的结构示意图: ⑥次氯酸分子的结构式:H-O-Cl ⑦CO2的分子模型示意图: A. 3个 B. 4个 C. 5个 D. 6个 |
|
| 17. 选择题 | 详细信息 |
|
同温同压下,在3支相同体积的试管中分别充有等体积混合的2种气体,它们是①NO和NO2②NO2和O2③NH3和 A. |
|
| 18. 选择题 | 详细信息 |
同一短周期元素甲、乙、丙、丁原子序数依次增大。常温下,含甲的化合物r浓度为0.1mol·L-1时溶液pH=13。同周期元素简单离子中,乙离子的半径最小。p和q分别是元素丙和丁的单质,其中p为浅黄色固体。上述物质的转化关系如图所示(产物水已略去)。下列说法不正确的是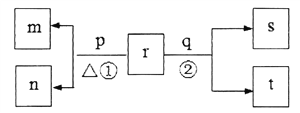 A. 原子半径的大小关系:甲>乙>丙>丁 B. 反应②的离子方程式为:C12+H2O C. m、n的阴离子在酸性条件下不能大量共存 D. 甲、乙、丁的最高价氧化物对应水化物两两之间均可以发生反应 |
|
| 19. 选择题 | 详细信息 |
|
主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。W、X、Z最外层电子数之和为10;W与Y同族;W与Z形成的化合物可与浓硫酸反应,其生成物可腐蚀玻璃。下列说法正确的是 A. 常温常压下X的单质为气态 B. Z的氢化物为离子化合物 C. Y和Z形成的化合物的水溶液呈碱性 D. W与Y具有相同的最高化合价 |
|
| 20. 选择题 | 详细信息 |
合成氨及其相关工业中,部分物质间的转化关系如下图所示,下列说法不正确的是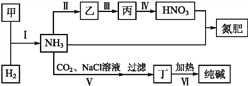 A. 甲、乙、丙三种物质中都含有氮元素 B. 反应Ⅰ、Ⅱ、Ⅲ中含氮元素的反应物都被氧化 C. Ⅴ中发生反应:NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl D. Ⅵ利用丁物质受热易分解的性质 |
|
| 21. 选择题 | 详细信息 |
|
下列物质按只含离子键、只含共价键、既含离子键又含共价键的顺序排列的是 A.氯气 二氧化碳 氢氧化钠 B.氯化钠 氦气 氢氧化钠 C.氯化钠 过氧化钠 氯化铵 D.氯化钠 过氧化氢 氯化铵 |
|
| 22. 选择题 | 详细信息 |
|
2.56克Cu完全溶于一定量的浓HNO3中,生成的气体恰好充满500mL的烧瓶,然后将该烧瓶倒置于水中,缓缓通入一定量的氧气后容器内刚好充满水,则通入的氧气为( ) A.0.16g B.0.02mol C.0.224g D.0.32g |
|
| 23. 选择题 | 详细信息 |
|
2.8gFe全部溶于一定浓度200mL的HNO3溶液中,得到标准状况下的气体1.12L,测得反应后溶液的pH为1。若反应前后溶液体积变化忽略不计,则下列说法正确的是( ) A.反应后溶液中存在Fe3+和Fe2+ B.反应后的溶液最多还能溶解1.82g Fe C.反应后溶液中c(NO3-)=0.75mol/L D.1.12L气体是NO、NO2的混合气体 |
|
| 24. 综合题 | 详细信息 |
|
(1)按要求写出电子式:CO2_________ COCl2_________ NaCN______ N2H (2)元素周期表中“对角线规则”是指处于周期表中对角线位置(左上和右下方)的两元素,其性质具有相似性,例如:Be和Al处于对角线位置。写出Be与氢氧化钠溶液反应的化学方程式:_________________________________。 (3)写出氢,氧,钠,硫四种元素组成的两种酸式盐发生复分解反应的离子方程式:___________________。 |
|
| 25. 实验题 | 详细信息 |
亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量。某兴趣小组用下图所示装置制备NaNO2并对其性质作如下探究(A中加热装置已略去)。 【背景素材】 ①2NO+Na2O2=2NaNO2; ②NO能被酸性KMnO4氧化成NO ③在酸性条件下NaNO2能把I-氧化为I2;S2O32-能把I2还原为I-。 【制备NaNO2】 (1) 装置A三颈烧瓶中发生反应的化学方程式为 。 (2) B装置的目的是① ,② 。 (3) 为保证制得的亚硝酸钠的纯度,C装置中盛放的试剂可能是 (填序号)。 A. P2O5 B. 碱石灰 C. 无水CaCl2 D. 生石灰 (4) E装置发生反应的离子方程式是 。 【测定NaNO2纯度】 (5) 本小题可供选择的试剂有: A.稀硫酸 B.c1mol·L-1KI溶液 C.淀粉溶液 D.c2mol·L-1Na2S2O3溶液 E.c3mol·L-1酸性KMnO4溶液 ①利用NaNO2的还原性来测定其纯度,可选择的试剂是 (填序号)。 ②利用NaNO2的氧化性来测定其纯度的步骤是:准确称取质量为m g的NaNO2样品放入锥形瓶中,加适量水溶解 (请补充完整实验步骤)。 |
|
| 26. 综合题 | 详细信息 |
下图是部分短周期元素的常见化合价与原子序数的关系图: (1)元素A在周期表中的位置 __________________________。 (2)用电子式表示D2G的形成过程____________________________,其所含化学键类型为___________。 (3)C2-、D+、G2-离子半径由大到小顺序是____________________(用离子符号回答)。 (4)某同学设计实验证明A、B、F的非金属性强弱关系。 ①溶液a和b分别为 ______________,________________。 ②溶液c中的离子方程式为________________________________________。  (5)将0.5 mol D2C2投入100 mL 3 mol/L ECl3溶液中: ①转移电子的物质的量为_____________________________________。 ②用一个离子方程式表示该反应 __________________________________________。 |
|
| 27. | 详细信息 |
电解精炼铜的阳极泥中主要含Ag、Au等贵重金属。以下是从精炼铜的阳极泥中回收银、金的流程图: (1)氯金酸(HAuCl4)中的Au的化合价为________。 (2)铜阳极泥氧化时,采用“低温焙烧”而不采用“高温焙烧”的原因是_____________________。 (3)“焙烧渣”在“①酸浸”时发生反应的离子方程式为______________________________________。 (4)“②浸金”反应中,H2SO4的作用为___________________________________________,该步骤的分离操作中,需要对所得的AgCl进行水洗。简述如何判断AgCl已经洗涤干净? _____________________________________________________。 (5)氯金酸(HAuCl4)在pH为2~3的条件下被草酸还原为Au,同时放出二氧化碳气体,则该反应的化学方程式为_____________________________________________________。 (6)甲醛还原法沉积银,通常是在搅拌下于室温及弱碱性条件下进行,甲醛被氧化为碳酸氢根离子,则该反应的离子方程式为___________________________________________。 |
|
最近更新



