2019届初三后半期6月中考模拟理科综合化学考题同步训练(湖南省长沙市明德华兴中学)
| 1. | 详细信息 |
|
下列所涉及的变化属于化学变化的是 A. 干冰升华 B. 钢铁生锈 C. 水结冰 D. 酒精挥发 |
|
| 2. | 详细信息 |
|
生活中的下列物品,主要材料属于合成材料的是( ) A. 全棉毛巾 B. 青花瓷瓶 C. 铝合金门窗 D. 塑料袋 |
|
| 3. | 详细信息 |
|
正确、规范的实验操作是科学探究成败的关键因素之一.下列实验操作不正确的是( ) A. 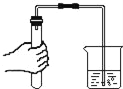 检查气密性 B. 检查气密性 B. 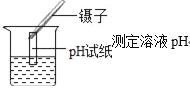 测定溶液pH 测定溶液pHC.  稀释浓硫酸 D. 稀释浓硫酸 D.  过滤 过滤 |
|
| 4. | 详细信息 |
|
生日蛋糕是当代少年儿童生日时爱吃的食物,生日蛋糕中的奶油含有对人体有害的反式脂肪酸,其化学式为 A. 反式脂肪酸由碳、氢、氧三种元素组成 B. 反式脂肪酸不是有机物 C. 反式脂肪酸由54个原子构成 D. 反式脂昉酸中碳、氧元素的质量比是9:1 |
|
| 5. | 详细信息 |
|
下列关于金属材料的说法不正确的是( ) A. 用稀盐酸可以鉴别黄金和黄铜(铜锌合金) B. 铁在干燥的空气中容易生锈 C. 硬铝(铝合金)的硬度大于纯铝 D. 金属资源的回收利用既保护了环境,又节约了金属资源 |
|
| 6. | 详细信息 |
|
质量守恒定律是帮助我们认识化学反应实质的重要理论.某物质与水和氧气反应的化学方程式为 A. FeS B. Fe2S3 C. FeO D. FeS2 |
|
| 7. | 详细信息 |
|
将甲、乙、丙三种金属分别放入试管中,滴加稀硫酸后只有丙金属表面有气体产生;再将乙金属放入甲金属的盐溶液中,乙金属表面有甲析出.则甲、乙、丙三种金属的金属活动性由强到弱的顺序为 A.乙>甲>丙 B.丙>乙>甲 C.乙>丙>甲 D.甲>乙>丙 |
|
| 8. | 详细信息 |
|
下列化学实验现象描述正确的是 ( ) A. 铁丝在氧气中燃烧时火星四射,有黑色四氧化三铁固体生成 B. 一氧化碳还原氧化铁的反应中,黑色粉末变成了红色 C. 硫在空气中燃烧发出微弱的淡蓝色火焰 D. 打开浓盐酸试剂瓶的瓶塞,瓶口上方出现大量白烟 |
|
| 9. | 详细信息 |
|
下列金属制品中最不容易被酸雨腐蚀的是( ) A. 镀锌水管 B. 铝合金门窗 C. 铁制栏杆 D. 铜制器皿 |
|
| 10. | 详细信息 |
|
学习化学的目的并不在于人人都要成为化学家,更重要的是学会用化学知识去解决生产生活中的问题,下列做法中错误的是( ) A. 用活性炭制品清除异味 B. 油库着火,用水扑灭 C. 用含有适量氢氧化钠的清洁剂去除炉具上的油污 D. 用燃烧法鉴别羊毛制品和化纤制品 |
|
| 11. | 详细信息 |
|
下列各组离子在pH=1的溶液中能大量共存的是 A. C. Cu2+、OH-、Cl-、Ba2+ D. Ag+、 |
|
| 12. | 详细信息 | |||||||||||||||||||||||||
下列除杂方法正确的是
|
||||||||||||||||||||||||||
| 13. | 详细信息 |
|
用化学用语填空: (1)两个镁离子_____; (2)空气中含量最高的气体_____。 |
|
| 14. | 详细信息 |
|
水是生命之源,我们应该了解水、爱护水. (1)目前部分农村的饮用水,主要是取地下水,可用________检验地下水是硬水还是软水. (2)净化地下水可用简易净水器,其中活性炭起________作用. |
|
| 15. | 详细信息 |
|
请写出下列变化的化学方程式 (1)工业上炼赤铁矿____________________。 (2)硫酸铜溶液与氢氧化钠溶液反应_______________________。 |
|
| 16. | 详细信息 |
如图是甲、乙、丙三种固体物质的溶解度曲线, (1)请写出P点代表的意义____________ (2)将接近饱和的丙溶液变成饱和溶液,可采取的措施有____________(写一条) (3)t2℃,甲、乙、丙三种物质的饱和溶液溶质质量分数的大小关系为______. |
|
| 17. | 详细信息 |
某工厂的废水中含有MgSO4和FeCl3,技术人员逐渐加入NaOH溶液调节废水的pH,先后分离出两种沉淀,并通过系列处理得到有价值的产品。操作流程如下图所示。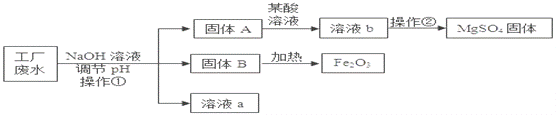 (1)操作①中玻璃棒的作用是_______________。 (2)固体B加热的产物是两种常见氧化物,则另一种氧化物的化学式为____________。 (3)溶液a除了可能含有NaOH外,还一定含有的溶质是_____________________。 |
|
| 18. | 详细信息 |
已知A~H为初中化学中常见的物质,它们之间的关系如图所示,“→”表示转化关系,“−”表示相互之间能反应(部分反应物、生成物以及反应条件省略)。其中A是使用最广泛的金属; B俗称烧碱,C为人体胃液的主要成分,C和E所属类别相同,固态D可用于人工降雨,F的溶液呈蓝色,可用于配制波尔多液,G常用于改良酸性土壤。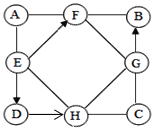 (1)A的化学式为______; (2)写出H与G反应的化学方程式:____________。 |
|
| 19. | 详细信息 |
根据如图所示的装置,结合所学知识回答下列问题。 (1)写出图中标号①所指仪器的名称:_______; (2)实验室用大理石和稀盐酸反应制取CO2,应选择的发生装置是_______(填字母),一般不用D装置收集CO2的原因是________________; (3)实验室制取O2,若选择E装置用排水法收集O2,先将E装置装满水,将气体从__________(a或b)端通入。 |
|
| 20. | 详细信息 |
为探究CO2与NaOH溶液发生的反应,某兴趣小组尝试用不同的方式进行实验。 (查阅资料)本实验条件下,Na2CO3溶液和NaHCO3溶液的pH分别约为11.0和8.5。 (实验探究)(1)实验一:小雨设计了如左图所示的实验,观察到的现象是_______,并得到广口瓶中的溶液X。 (2)实验二:为检验CO2与NaOH溶液反应的产物,小亮取实验一所得溶液X少许,向其中滴加过量____________,有气泡产生。 (3)实验三:小华取实验一所得溶液X少许,向其中加入过量的BaCl2溶液,振荡,静置,取上层清液,滴入1滴酚酞试液,发现溶液呈红色,证明溶液X中溶质一定有_____________________。 (4)实验四:兴趣小组将CO2持续通入一定浓度一定量的NaOH溶液中,用数字化实验技术测定反应过程中溶液的pH和温度变化,结果如图1、图2所示。 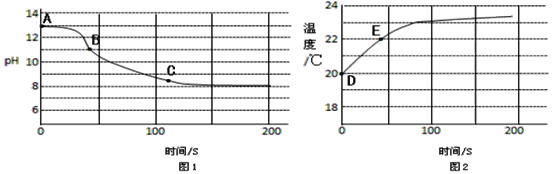 ①图1中,BC段发生反应的化学方程式为_________________________。 ②图2中,DE段温度变化的原因可能是______________________。 (反思感悟)(5)实验从CO2减少、Na2CO3生成等物质的变化,以及温度转化等视角多维度探究CO2与NaOH发生了反应,对于现象不明显的化学反应,可以通过现代技术手段进行数据测定,实现反应过程的“可视化”。 |
|
| 21. | 详细信息 |
|
某化学兴趣小组为了测定贝壳中碳酸钙的质量分数,做如下实验:取贝壳样品12g装入烧杯中,向其中加入100克稀盐酸恰好完全反应(杂质不溶于水也不参加反应),实验完成后烧杯中物质一共107.6克。试计算: (1)生成气体____________克 (2)稀盐酸中溶质的质量分数________。 |
|
最近更新



