四川省雅安中学2020-2021年高一上学期开学考试化学免费试题带答案和解析
| 1. 选择题 | 详细信息 |
|
下列用途利用了物质的化学性质的是( ) A.铜丝作导线 B.生石灰用作干燥剂 C.木炭用作吸附剂 D.干冰用于人工降雨 |
|
| 2. 选择题 | 详细信息 |
|
臭氧(O3)能够吸收紫外线保护地球生命,打雷放电时,空气中有极少量氧气会转化成臭氧(O3),即3O2 ①一个O3分子由3个氧原子构成 ②O2和O3的分子构成不同 ③该变化属于物理变化 ④相同质量的O2和O3,所含分子的数目相同 ⑤O2和O3互为同素异形体 A.①③④ B.①②⑤ C.②③⑤ D.②③④ |
|
| 3. 选择题 | 详细信息 | |||||||||||||||
“宏观辨识与微观探析”是化学学科核心素养之一。下列客观事实的微观解释正确的是( )
|
||||||||||||||||
| 4. 选择题 | 详细信息 |
利用下列仪器制取相关气体,不能实现的是( ) A.用锌和稀硫酸制取氢气 B.用双氧水和二氧化锰制取氧气 C.用高锰酸钾加热分解制取氧气 D.用石灰石和稀盐酸制取二氧化碳 |
|
| 5. 选择题 | 详细信息 |
|
下列实验操作正确的是( ) A.药品称量  B.稀释浓硫酸  C.pH 试纸使用  D.验满CO2  |
|
| 6. 选择题 | 详细信息 |
|
生活在密闭狭小的特殊环境(如潜艇、太空舱)里,O2会越来越少,CO2会越来越多,因此将CO2转化为O2,不仅有科学意义也有重要的实用价值。据科学文献报道,NiFe2O4在一定条件下既能促进CO2分解又可重复使用。NiFe2O4在此反应中是( ) A.粘合剂 B.制冷剂 C.防腐剂 D.催化剂 |
|
| 7. 选择题 | 详细信息 |
|
钴(Co)的化合物在锂电池中有很好的应用,LiCoO2(钴酸锂)在酸性介质中有强氧化性,其化学方程式为:2LiCoO2 + H2O2 + 3H2SO4 =Li2SO4 + 2CoSO4 + 4H2O + O2↑。已知锂与钠有相似的化学性质,且反应中只有钴和氧元素的化合价发生了改变,则下列说法正确的是( ) A.该反应是复分解反应 B.该反应中钴的化合价由+3价变为+2价 C.该反应中氧的化合价降低 D.钴酸根离子式 |
|
| 8. 选择题 | 详细信息 |
|
“绿色化学”要求原料物质中所有的原子完全被利用,全部转入期望的产品中,即原子利用率为100%。由C2H4(乙烯)合成C4H8O2(乙酸乙酯)的过程中,为使原子利用率达到100%,在催化剂作用下还需加入的物质是( ) A.HCOOH B.H2O和CO2 C.O2和H2O D.O2 |
|
| 9. 选择题 | 详细信息 | |||||||||||||||||
根据如表信息,相关说法正确的是( )
|
||||||||||||||||||
| 10. 选择题 | 详细信息 | |||||||||||||||
为达到下列实验目的,对应的实验方案正确的是( )
|
||||||||||||||||
| 11. 选择题 | 详细信息 |
我国科学家研究出碳化钼负载金原子的催化体系,使CO和H2O在120℃下发生反应,其微观过程如图所示。下列说法正确的是( ) A.图中仅有1种金属元素的原子 B.反应前后分子种类、数目均不变 C.金原子对CO起吸附催化作用 D.反应的化学方程式为:CO+H2O |
|
| 12. 选择题 | 详细信息 |
|
下列图象能正确反映其对应实验操作的是( ) A.将等质量的Mg、Zn分别与溶质质量分数相同的足量稀硫酸反应  B.加热一定量的高锰酸钾固体 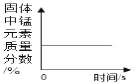 C.向硫酸和硫酸铜的混合溶液中加入过量的氢氧化钠溶液  D.电解一定质量的水  |
|
| 13. 选择题 | 详细信息 |
|
将密封良好的饼干从平原带到高原,包装袋会鼓起,这是因为( ) A.饼干的质量变大 B.袋内气体分子个数增多 C.高原地区大气压强较大 D.袋内气体分子间的间隙变大 |
|
| 14. 选择题 | 详细信息 | ||||||||||||||||||||
除去下列各物质中混有的少量杂质,拟订的实验方案可行的是( )
|
|||||||||||||||||||||
| 15. 选择题 | 详细信息 |
下图是探究金属化学性质的四个实验,有关叙述不正确的是( ) A.由①和②可以得出金属活动性:Zn>Fe B.由③和④可以得出金属活动性:Fe>Cu>Ag C.③中铜丝表面有银白色物质析出,溶液变成蓝色 D.②中反应的化学方程式为:Fe + H2SO4 =FeSO4 +H2↑ |
|
| 16. 选择题 | 详细信息 |
向某盐酸和氯化镁的混合溶液中加入某浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法不正确的是( ) A.a 点溶液中滴入紫色石蕊试液变红 B.bc 段(不含 b 点)反应的化学方程式为MgCl2+2NaOH═Mg(OH)2↓+2NaCl C.整个变化过程中氯离子数目没有改变 D.d 点溶液中含有两种溶质 |
|
| 17. 选择题 | 详细信息 |
|
如图是金属活动性顺序的部分内容,则下列说法正确的是( ) A.金属①是Mg B.2Fe+6HCl=2FeCl3+3H2↑ C.金属②能置换出稀盐酸中的氢气 D.金属①、②都能与硝酸银溶液发生置换反应 |
|
| 18. 选择题 | 详细信息 |
|
双氧水是过氧化氢(H2O2)的无色透明水溶液,广泛应用于工业漂白、外科消毒等领域。下列关于H2O2的说法正确的是( ) A.H2O2中氧元素化合价为-2价 B.1个H2O2分子中含1个氢分子 C.相对分子质量为34g D.氢元素与氧元的质量比为1:16 |
|
| 19. 选择题 | 详细信息 |
|
分析推理是化学学习中常用的思维方法。下列说法正确的是( ) ①单质只含有一种元素,所以含一种元素的物质一定属于单质; ②Na2MoO4中钼(Mo)元素的化合价是+6价; ③盐是由金属离子和酸根离子组成的,NH4NO3中没有金属离子,不属于盐; ④化学变化中,原子的种类和个数不变; ⑤带电的微粒都称为离子; ⑥NaOH溶液中的OH-能与酸反应,则KOH溶液中的OH‑也能与酸反应 A.①②④ B.②④⑥ C.①③⑤ D.③⑤⑥ |
|
| 20. 选择题 | 详细信息 |
|
一定质量的甲烷在不充足的氧气中燃烧,甲烷完全反应,生成物只有CO、CO2和H2O,且总质量为20.8g,其中H2O的质量为10.8g,则CO2的质量为( ) A.5.6g B.8.8g C.4.4g D.4.8g |
|
| 21. 选择题 | 详细信息 | ||||||||||||||||||||
a、b、c、d可能是Na2CO3、AgNO3、BaCl2、HCl四种溶液中的各一种,它们两两混合后产生如表现象:则a、b、c、d依次是( )
|
|||||||||||||||||||||
| 22. 填空题 | 详细信息 |
科学精神与社会责任,是化学学科素养更高层面的价值追求。在一次实践活动中,小红和同学们一起参观了某钢铁公司,大家对矿石选取、冶铁和炼钢的工艺流程(如图)、生铁和钢的区别等,有了全新的认识。 (1)用赤铁矿石冶铁的反应原理是______(用化学方程式表示)。 (2)分析工艺流程,三脱装置中发生反应的化学方程式是______。(写一个)。 (3)向精炼炉中吹入氩气使钢水循环流动,各成分均匀混合,相当于化学实验中______的作用(填一种仪器的名称)。 (4)在钢水铸件机中,高温钢加工成钢制零件时,充入氮气的作用是______(合理即可)。 |
|
| 23. | 详细信息 |
|
元素周期表是学习和研究化学的重要工具。 (1)原子序数为 1~18 的元素在元素周期表中的位置如下表所示。  ①Al原子的核电荷数为____。②钠离子的结构示意图为____。 ③周期表中磷元素的有关信息为 (2)根据周期表体现的结构与性质之间的关系,某同学构建了铜及其化合物的“化合价﹣物质类别”关系图。 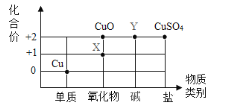 ①写出物质 X 的化学式:________________。 ②写出由物质 Y 转化为 CuSO4 的化学反应方程式:_______________。 ③氧化还原反应是化学学习中的核心概念,对氧化还原反应的定义为有化合价升降的反应,下列转化中属于氧化还原反应的是_________________。 A、Cu—X B、X—CuO C、CuO—Y D、Y—CuSO4 |
|
| 24. 实验题 | 详细信息 |
|
气体制取是化学实验基本技能之一,请按要求回答有关问题。 (1)实验室用固体和液体制取O2的化学方程式是______。 (2)从图中选用4个装置来制取一瓶干燥纯净的CO2气体。 ①正确的接口顺序从左到右依次为:a→ ((___________)→______→______→______)→e; ②所选装置有一处明显的错误是______,B中盛放的液体是______(填名称)。  (3)用图中的F装置可以制造十分有趣的“化学喷泉”。将胶头滴管中的NaOH溶液挤进圆底烧瓶时,很快看到长导管顶端产生“喷泉”现象。烧瓶中发生反应的化学方程式是______。若将烧瓶内的CO2换成下列四种气体中的___________(填字母序号)仍可产生“喷泉”现象。 A.SO2 B.H2 C.CO D.N2 |
|
| 25. 实验题 | 详细信息 | ||||||||||||||||
|
化学兴趣小组的同学发现实验台上有一瓶标签残缺的试剂(如图),同学们对此进行了如下探究。 (提出问题)这是一瓶什么溶液? (猜想与假设)海天同学的猜想是Na2SO3溶液;刘浩同学的猜想是Na2SO4溶液;你的猜想是______(写一种). (查阅资料) Ⅰ、白色沉淀BaSO3不溶于水,但要溶于稀盐酸. Ⅱ、硝酸具有强氧化性,能将BaSO3氧化成BaSO4. Ⅲ、Na2SO3与稀盐酸反应产生SO2,SO2能使石灰水变浑浊,也能使品红溶液褪色. (进行实验) Ⅰ、海天同学取适量的该溶液于试管中,滴加稀盐酸,产生无色气体,他认为自己的猜想成立,而刘浩同学认为他的结论不合理,原因是______. Ⅱ、刘浩同学为了验证自己的猜想,做了如下实验: 取适量的该溶液于试管中,先滴加足量的BaCl2溶液,再滴加过量稀硝酸,现象为______,刘浩同学认为自己的猜想成立. Ⅲ、卓玛同学对刘浩同学的猜想又提出了质疑,她认为加BaCl2和稀硝酸,Na2SO3也会产生沉淀,为了验证自己的观点,做了如下实验:
|
|||||||||||||||||
| 26. 填空题 | 详细信息 |
硫化氢的转化是资源利用和环境保护的重要研究课题,将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应用以回收S,其物质转化如图所示。 (1)反应中当有34g H2S转化为硫单质时,保持溶液中Fe3+的量不变,需消耗O2的质量为______。 (2)在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施是___________________________________。 (3)写出图中各步转化的化学方程式:_______________________。 |
|



