дёҠжө·еёӮ2019е№ҙй«ҳдёүеҗҺеҚҠжңҹеҢ–еӯҰй«ҳиҖғжЁЎжӢҹиҜ•еҚ·е®Ңж•ҙзүҲ
| 1. | иҜҰз»ҶдҝЎжҒҜ |
|
жө·ж°ҙж·ЎеҢ–еҸҜи§ЈеҶіж·Ўж°ҙиө„жәҗзјәд№Ҹзҡ„й—®йўҳгҖӮдёӢеҲ—еҸҜеә”з”ЁдәҺжө·ж°ҙж·ЎеҢ–жҠҖжңҜзҡ„ж“ҚдҪңжҳҜ( ) A. и’ёйҰҸ B. иҝҮж»Ө C. иҗғеҸ– D. з»“жҷ¶ |
|
| 2. | иҜҰз»ҶдҝЎжҒҜ |
|
еҗ‘з©әж°”дёӯвҖңжҢ–зҹҝвҖқпјҢдёәдәәзұ»зІ®йЈҹеўһдә§еҒҡеҮәе·ЁеӨ§иҙЎзҢ®зҡ„еҢ–еӯҰе·ҘдёҡжҳҜ( ) A. зЎ«й…ёе·Ҙдёҡ B. еҗҲжҲҗж°Ёе·Ҙдёҡ C. зәҜзўұе·Ҙдёҡ D. зҹіжІ№еҢ–е·Ҙ |
|
| 3. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҗ«ж°®еҫ®зІ’зҡ„еҢ–еӯҰз”ЁиҜӯиЎЁиҫҫжӯЈзЎ®зҡ„жҳҜ( ) A. ж°®-14еҺҹеӯҗпјҡ C. ж°Ёж°”зҡ„з”өеӯҗејҸпјҡ |
|
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
е’ҢзәҜй“ҒзӣёжҜ”пјҢз”ҹй“ҒдёҚе…·жңүзҡ„зү№зӮ№жҳҜ( ) A. зЎ¬еәҰжӣҙеӨ§ B. зҶ”зӮ№жӣҙдҪҺ C. жӣҙиҖҗи…җиҡҖ D. жҳ“еҶ¶зӮјеҫ—еҲ° |
|
| 5. | иҜҰз»ҶдҝЎжҒҜ |
|
дёҚжҳҜз…Өе№ІйҰҸдә§зү©зҡ„жҳҜ( ) A. з…ӨжІ№ B. з„ҰзӮӯ C. з„ҰзӮүж°” D. зІ—ж°Ёж°ҙ |
|
| 6. | иҜҰз»ҶдҝЎжҒҜ |
|
й“өжҖҒж°®иӮҘеңЁдҪҝз”Ёж—¶иҰҒжіЁж„ҸдҪҺжё©дҝқеӯҳе’Ңж·ұж–Ҫзӣ–еңҹпјҢеҺҹеӣ жҳҜй“өжҖҒж°®иӮҘпјҲ пјү A. жҳ“жә¶дәҺж°ҙ B. йҒҮзўұжҳ“и·‘ж°Ё C. жҳ“иў«ж°§еҢ– D. еҸ—зғӯжҳ“еҲҶи§Ј |
|
| 7. | иҜҰз»ҶдҝЎжҒҜ |
|
и‘Ўиҗ„й…’дёӯеҠ е…Ҙе°‘йҮҸSO2пјҢеҸҜйҳІжӯўй…’дёӯзҡ„д№ҷйҶҮиҪ¬еҢ–дёәд№ҷй…ёпјҢиҝҷжҳҜеҲ©з”ЁдәҶSO2зҡ„( ) A. ж°§еҢ–жҖ§ B. иҝҳеҺҹжҖ§ C. жјӮзҷҪжҖ§ D. й…ёжҖ§ |
|
| 8. | иҜҰз»ҶдҝЎжҒҜ |
|
е…ідәҺж°ҜеҢ–ж°ўзҡ„иҜҙжі•й”ҷиҜҜзҡ„жҳҜпјҲ пјү A. жә¶дәҺж°ҙж—¶з ҙеқҸе…ұд»·й”® B. еҸҜз”ЁдәҺеҒҡе–·жіүе®һйӘҢ C. йҒҮж°Ёж°”дә§з”ҹзҷҪзғҹ D. еҸҜйҖҡиҝҮе…ұд»·й”®еҪўжҲҗжҷ¶дҪ“ |
|
| 9. | иҜҰз»ҶдҝЎжҒҜ |
|
дёҚиғҪдҪҝй…ёжҖ§й«ҳй”°й…ёй’ҫжә¶ж¶ІиӨӘиүІзҡ„жҳҜпјҲ пјү A. д№ҷзғҜ B. д№ҷзӮ” C. иӢҜ D. з”ІиӢҜ |
|
| 10. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зү©иҙЁйңІзҪ®еңЁз©әж°”дёӯпјҢдјҡеҸ‘з”ҹеҢ–еӯҰеҸҚеә”дё”жңүйўңиүІеҸҳеҢ–зҡ„жҳҜ( ) A. NaClO B. NaOH C. Na2O2 D. NaCl |
|
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
з”Ёзғ§зўұеӣәдҪ“й…ҚеҲ¶0.100mol/L NaOHжә¶ж¶Ізҡ„йғЁеҲҶж“ҚдҪңеҰӮеӣҫжүҖзӨәпјҢе…¶дёӯдёҚйңҖиҰҒзҡ„жҳҜ( ) A.  жЈҖжјҸ B. жЈҖжјҸ B. 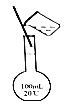 иҪ¬з§» D. иҪ¬з§» D.  е®ҡе®№ е®ҡе®№ |
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
|
е…ідәҺж°§еҢ–й“қе’Ңж°ўж°§еҢ–й“қзҡ„иҜҙжі•й”ҷиҜҜзҡ„жҳҜ( ) A. йғҪжҳҜзҷҪиүІеӣәдҪ“ B. йғҪйҡҫжә¶дәҺж°ҙ C. йғҪе…·жңүдёӨжҖ§ D. йғҪеҸ—зғӯжҳ“еҲҶи§Ј |
|
| 13. | иҜҰз»ҶдҝЎжҒҜ |
|
жёҜзҸ жҫіеӨ§жЎҘи®ҫи®ЎеҜҝе‘Ҫдёә120е№ҙпјҢеҜ№жЎҘдҪ“й’ўеҲ¶жһ„件йҮҮз”ЁдәҶеӨҡз§ҚйҳІи…җжҺӘж–ҪпјҢдёӢеҲ—йҳІи…җжҺӘж–Ҫй”ҷиҜҜзҡ„жҳҜ( ) A. з”ЁеҜјзәҝдёҺзҹіеўЁзӣёиҝһ B. з”ЁеҜјзәҝдёҺз”өжәҗиҙҹжһҒзӣёиҝһ C. й’ўеҲ¶жһ„件дёҠз„ҠжҺҘй”Ңеқ— D. иЎЁйқўе–·ж¶ӮеҲҶеӯҗж¶ӮеұӮ |
|
| 14. | иҜҰз»ҶдҝЎжҒҜ |
|
з”Ёж ҮеҮҶзӣҗй…ёж»ҙе®ҡеҫ…жөӢNaOHжә¶ж¶Іж—¶пјҢзӣёе…іиҜҙжі•жӯЈзЎ®зҡ„жҳҜ( ) A. еҸҜз”Ёзҹіи•ҠдҪңжҢҮзӨәеүӮ B. ж»ҙе®ҡж—¶зңјзқӣжіЁи§Ҷж»ҙе®ҡз®Ўдёӯж¶ІйқўдёӢйҷҚ C. йңҖеҒҡе№іиЎҢе®һйӘҢ2~3ж¬Ў D. еҪ“жә¶ж¶ІйўңиүІеҸҳеҢ–ж—¶з«ӢеҚіиҜ»ж•° |
|
| 15. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—е…ідәҺе®һйӘҢе®ӨеҲ¶еӨҮд№ҷй…ёд№ҷй…Ҝзҡ„ж“ҚдҪңй”ҷиҜҜзҡ„жҳҜ( ) A. й…Қж–ҷпјҡеҠ е…ҘиҝҮйҮҸд№ҷйҶҮ B. еҠ зғӯпјҡз”Ёж°ҙжөҙеҠ зғӯ C. еҲҶзҰ»пјҡз”Ёиҫ№еҸҚеә”иҫ№еҲҶзҰ»зҡ„ж–№жі• D. еҮҖеҢ–пјҡдә§зү©з”Ёж°ўж°§еҢ–й’ жә¶ж¶Іжҙ—ж¶Ө |
|
| 16. | иҜҰз»ҶдҝЎжҒҜ |
AгҖҒBгҖҒCгҖҒDеӣӣз§Қзҹӯе‘Ёжңҹе…ғзҙ еңЁе‘ЁжңҹиЎЁдёӯзҡ„дҪҚзҪ®еҰӮеӣҫжүҖзӨәпјҢжңүе…іиҜҙжі•жӯЈзЎ®зҡ„жҳҜ( ) A. е…ғзҙ жңҖй«ҳжӯЈд»·ж•°еҖјжңҖеӨ§зҡ„жҳҜA B. еҚ•иҙЁзҶ”зӮ№жңҖй«ҳзҡ„жҳҜC C. зҰ»еӯҗеҚҠеҫ„пјҡA<C D. йҮ‘еұһжҖ§пјҡB>C |
|
| 17. | иҜҰз»ҶдҝЎжҒҜ |
еҰӮеӣҫжүҖзӨәпјҢе°Ҷжө“зЎ«й…ёж»ҙиҮідёӢеҲ—зү©иҙЁдёҠпјҢж— жҳҺжҳҫзҺ°иұЎзҡ„жҳҜпјҲ пјү A. A B. B C. C D. D |
|
| 18. | иҜҰз»ҶдҝЎжҒҜ |
жҹҗеҗ«ж°§иЎҚз”ҹзү©зҡ„зҗғжЈҚжЁЎеһӢеҰӮдёӢеӣҫжүҖзӨәпјҢдёӢеҲ—е…ідәҺиҜҘзү©иҙЁзҡ„иҜҙжі•й”ҷиҜҜзҡ„жҳҜ( )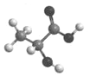 A. еҲҶеӯҗејҸдёәC3H6O3 B. еҗ«жңүдёӨз§Қе®ҳиғҪеӣў C. иғҪеҸ‘з”ҹеҸ–д»ЈеҸҚеә”пјҢдёҚиғҪеҸ‘з”ҹж¶ҲеҺ»еҸҚеә” D. ж—ўиғҪдёҺз”ҹзҹізҒ°еҸҚеә”пјҢеҸҲиғҪдёҺж°ўжәҙй…ёеҸҚеә” |
|
| 19. | иҜҰз»ҶдҝЎжҒҜ |
|
ж°Ёзўұжі•дёҺдҫҜж°ҸеҲ¶зўұжі•зҡ„з”ҹдә§е·ҘиүәдёӯпјҢзӣёеҗҢзҡ„жҳҜ( ) A. дё»еҸҚеә”еҺҹзҗҶ B. еүҜдә§е“Ғ C. йЈҹзӣҗеҲ©з”ЁзҺҮ D. еҫӘзҺҜзү©иҙЁ |
|
| 20. | иҜҰз»ҶдҝЎжҒҜ |
|
жҹҗжә¶ж¶ІдёӯеҸҜиғҪеҗ«жңүNa+гҖҒFe2+гҖҒNH4+гҖҒK+гҖҒCl-гҖҒSO42-гҖҒSO32-дёӯзҡ„еҮ з§ҚпјҢдё”жүҖеҗ«зҰ»еӯҗзү©иҙЁзҡ„йҮҸжө“еәҰеқҮдёә0.01mol/LгҖӮеҗ‘жә¶ж¶Ідёӯж»ҙеҠ е°‘йҮҸжәҙж°ҙеҗҺпјҢжә¶ж¶Іе‘Ҳж— иүІгҖӮдёӢеҲ—е…ідәҺиҜҘжә¶ж¶Ізҡ„еҲӨж–ӯжӯЈзЎ®зҡ„жҳҜ( ) A. еҸҜиғҪеҗ«жңүNa+ B. еҸҜиғҪеҗ«жңүSO42- C. дёҖе®ҡдёҚеҗ«Cl- D. дёҖе®ҡеҗ«жңүNH4+ |
|
| 21. | иҜҰз»ҶдҝЎжҒҜ |
|
еӨ©з„¶ж°”е№ҝжіӣз”ЁдәҺж°‘з”ЁзҮғж°”е’ҢеҢ–е·Ҙз”ҹдә§пјҢдё»иҰҒжҲҗеҲҶжҳҜCH4пјҢиҝҳеҗ«жңүе°‘йҮҸH2Sе’Ңж°ҙи’ёж°”гҖӮ (1)зўігҖҒж°ўгҖҒж°§гҖҒзЎ«еӣӣз§Қе…ғзҙ дёӯпјҢжңҖеӨ–еұӮз”өеӯҗж•°жҳҜз”өеӯҗеұӮж•°дёӨеҖҚзҡ„жҳҜ______(еЎ«е…ғзҙ з¬ҰеҸ·)пјҢйқһйҮ‘еұһжҖ§жңҖејәе…ғзҙ зҡ„еҺҹеӯҗж ёеӨ–з”өеӯҗжҺ’еёғејҸдёә__________________гҖӮ (2) еӨ©з„¶ж°”зҡ„з”ЁйҖ”д№ӢдёҖжҳҜеҲ©з”Ёз”Ізғ·й«ҳжё©еҲҶи§ЈеҲ¶зӮӯй»‘гҖӮиӢҘеҲҶи§Ј16gз”Ізғ·пјҢйңҖиҰҒеҗёж”¶258kJзҡ„зғӯйҮҸпјҢеҶҷеҮәиҜҘеҸҚеә”зҡ„зғӯеҢ–еӯҰж–№зЁӢејҸпјҡ____________________________________________гҖӮ (3)еӨ©з„¶ж°”еңЁдҪҝз”ЁеүҚпјҢйңҖиҝӣиЎҢи„ұзЎ«еӨ„зҗҶгҖӮз”ЁзәҜзўұжә¶ж¶Іеҗёж”¶е…¶дёӯзҡ„H2SпјҢиҝҮзЁӢдёӯдјҡз”ҹжҲҗдёӨз§Қй…ёејҸзӣҗпјҢиҜҘеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸдёә____________________________________________гҖӮиӢҘж”№з”ЁNaOHжә¶ж¶Іеҗёж”¶H2SпјҢд»ҺйҖҡе…Ҙж°”дҪ“иҮіиҝҮйҮҸпјҢжә¶ж¶Ідёӯc(S2-)зҡ„еҸҳеҢ–и¶ӢеҠҝжҳҜ______________________гҖӮ (4)еҫ®жіўеҠ зғӯжҠҖжңҜзҡ„еҺҹзҗҶжҳҜпјҡеҲ©з”ЁжһҒжҖ§еҲҶеӯҗеҶ…йғЁжӯЈиҙҹз”өиҚ·еҲҶеёғдёҚеқҮеҢҖзҡ„зү№зӮ№пјҢеңЁз”өзЈҒеңәдҪңз”ЁдёӢдјҡйў‘з№ҒиҝҗеҠЁж‘©ж“ҰпјҢдҪҝжё©еәҰеҚҮй«ҳгҖӮз”Ёз”Ізғ·еҲ¶зӮӯй»‘зҡ„е·Ҙдёҡз”ҹдә§дёӯпјҢжҳҜеҗҰйҖӮеҗҲдҪҝз”ЁиҜҘжҠҖжңҜеҠ зғӯпјҢеҺҹеӣ жҳҜ_____________гҖӮзЎ«еҢ–ж°ўеҲҶеӯҗз»“жһ„дёҺж°ҙеҲҶеӯҗзӣёдјјпјҢеҠ зғӯж—¶зЎ«еҢ–ж°ўиҫғж°ҙжӣҙжҳ“еҲҶи§Јеҫ—еҲ°ж°ўж°”пјҢд»Һе…ғзҙ е‘ЁжңҹеҫӢи§’еәҰеҲҶжһҗе…¶еҺҹеӣ ___________________гҖӮ |
|
| 22. | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||||||||||||
з”ЁCl2з”ҹдә§еҗ«ж°Ҝжңүжңәзү©ж—¶дјҡдә§з”ҹHClпјҢеҲ©з”ЁеҰӮдёӢеҸҚеә”еҸҜе®һзҺ°ж°Ҝзҡ„еҫӘзҺҜеҲ©з”ЁгҖӮ4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)+Q(Q>0)еңЁ2LеҜҶй—ӯе®№еҷЁдёӯиҝӣиЎҢиҜҘеҸҚеә”пјҢеңЁдёҚеҗҢж—¶й—ҙжөӢеҫ—е®һйӘҢж•°жҚ®еҰӮдёӢиЎЁпјҡ
|
||||||||||||||||||||||||||
| 23. | иҜҰз»ҶдҝЎжҒҜ |
|
еӨ©з„¶ж°ҙеӨ§еӨҡеҗ«Ca2+гҖҒMg2+гҖҒHCO3-зӯүзҰ»еӯҗпјҢеҠ зғӯдјҡдә§з”ҹж°ҙеһўпјҢж°ҙеһўдёӯдёҖе®ҡеҗ«жңүCaCO3е’ҢMg(OH)2пјҢеҸҜиғҪеҗ«жңүMgCO3гҖӮ (1)еӨ©з„¶ж°ҙдёӯзҡ„HCO3-жқҘиҮӘдәҺз©әж°”дёӯзҡ„CO2гҖӮз”Ёзӣёе…іж–№зЁӢејҸиЎЁзӨәCO2жә¶дәҺж°ҙеҪўжҲҗHCO3-зҡ„иҝҮзЁӢгҖӮ______________________________________________________________ (2)еӨ©з„¶ж°ҙз…®жІёж—¶пјҢе…¶дёӯеҫ®жә¶зҡ„MgCO3иҪ¬жҚўжҲҗйҡҫжә¶зҡ„Mg(OH)2пјҢеҶҷеҮәеҸ‘з”ҹеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸгҖӮ____________________________________________ дёәзЎ®е®ҡжҹҗж°ҙеһўж ·е“Ғзҡ„жҲҗеҲҶпјҢеҲ©з”ЁCaCO3гҖҒMgCO3гҖҒMg(OH)2й«ҳжё©еҲҶи§Јзҡ„жҖ§иҙЁпјҢзІҫзЎ®з§°йҮҸ5.000gж°ҙеһўж ·е“ҒпјҢз”ЁеҰӮдёӢеӣҫиЈ…зҪ®иҝӣиЎҢе®һйӘҢгҖӮ 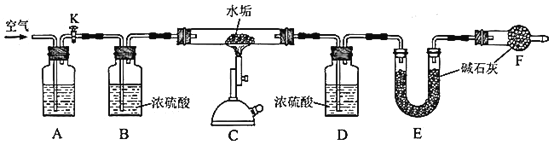 (3)Aдёӯзӣӣж”ҫзҡ„иҜ•еүӮжҳҜ__________гҖӮиЈ…зҪ®Fзҡ„дҪңз”ЁжҳҜ_________________________гҖӮеҸҚеә”з»“жқҹеҗҺпјҢйңҖиҰҒеҶҚйҖҡе…ҘдёҖж®өж—¶й—ҙзҡ„з©әж°”пјҢзӣ®зҡ„жҳҜ_______________________гҖӮ (4)еҲ©з”ЁдёҠиҝ°иЈ…зҪ®жөӢе®ҡж°ҙеһўдёӯMg(OH)2зҡ„еҗ«йҮҸж—¶пјҢйңҖиҰҒжөӢйҮҸзҡ„ж•°жҚ®жңү__________гҖӮ (5)е®һйӘҢжөӢеҫ—иЈ…зҪ®EеўһйҮҚ2.200gпјҢиҜ·й—®ж°ҙеһўж ·е“ҒдёӯжҳҜеҗҰеҗ«жңүMgCO3?еҲӨж–ӯдҫқжҚ®жҳҜ_______________________________________________________гҖӮ |
|
| 24. | иҜҰз»ҶдҝЎжҒҜ |
е·ҘдёҡдёҠз”ЁиӢҜз”ІйҶӣ( е®ҢжҲҗдёӢеҲ—еЎ«з©әпјҡ (1)еҸҚеә”в‘ зҡ„дә§зү©йҷӨдәҶAпјҢиҝҳжңүдёҖз§Қж— жңәе°ҸеҲҶеӯҗпјҢе…¶еҲҶеӯҗејҸжҳҜ_____________гҖӮеҸҚеә”в‘ўзҡ„еҸҚеә”зұ»еһӢжҳҜ__________________гҖӮ (2)еҸҚеә”в‘Өзҡ„еҢ–еӯҰж–№зЁӢејҸ____________________________________________гҖӮеҶҷеҮәиӢҜдёҒдәҢзғҜзҡ„дёҖз§ҚеҠ иҒҡдә§зү©зҡ„з»“жһ„з®ҖејҸ__________________________гҖӮ (3)жөҒзЁӢдёӯи®ҫи®ЎеҸҚеә”в‘Ўе’Ңв‘Јзҡ„зӣ®зҡ„жҳҜ__________________________________гҖӮ (4)еҶҷеҮәж»Ўи¶ідёӢеҲ—жқЎд»¶зҡ„иӢҜз”ІйҶӣзҡ„еҗҢзі»зү©_______________________гҖӮ в‘ жҜ”иӢҜз”ІйҶӣеӨҡдёӨдёӘзўіеҺҹеӯҗпјҢв‘ЎиӢҜзҺҜдёҠеҸӘжңүдёҖдёӘеҸ–д»ЈеҹәпјҢв‘ўеҗ«жңүдёҖдёӘз”ІеҹәгҖӮ (5)дёҷйҶӣжҳҜдёҷй…®зҡ„еҗҢеҲҶејӮжһ„дҪ“пјҢи®ҫи®Ўз”ұдёҷйҶӣеҗҲжҲҗ |
|
- 2018иҮі2019е№ҙй«ҳдәҢдёӢеҚҠжңҹ5жңҲд»ҪиҖғиҜ•еҢ–еӯҰеңЁзәҝжөӢйӘҢе®Ңж•ҙзүҲпјҲдә‘еҚ—зңҒзҺүжәӘеёӮжұҹе·қдәҢдёӯпјү
- ж№–еҢ—зңҒе®ңжҳҢеёӮ2020е№ҙ4жңҲй«ҳдёүиҒ”иҖғеңЁзәҝи°ғиҖғзҗҶз»јеҢ–еӯҰиҖғйўҳеҗҢжӯҘи®ӯз»ғ
- жҷҜеҫ·й•ҮдёҖдёӯй«ҳдәҢеҢ–еӯҰдёҠеҶҢжңҹжң«иҖғиҜ•е…Қиҙ№иҜ•еҚ·е®Ңж•ҙзүҲ
- жұҹиӢҸзңҒеёёзҶҹеёӮ2021еұҠй«ҳдёүдёҠеҚҠжңҹйҳ¶ж®өжҖ§жҠҪжөӢдәҢеҢ–еӯҰйўҳеёҰеҸӮиҖғзӯ”жЎҲ
- й«ҳдёүеҢ–еӯҰдёҠеҶҢжңҲиҖғиҜ•еҚ·жЁЎжӢҹиҖғиҜ•и®ӯз»ғ
- дёҠжө·2019е№ҙй«ҳдёүеҢ–еӯҰдёҠеҶҢжңҲиҖғжөӢйӘҢзҪ‘дёҠеңЁзәҝеҒҡйўҳ
- 2019-2020е№ҙй«ҳдёҖдёӢеӯҰжңҹжңҹжң«иҖғиҜ•еҢ–еӯҰиҖғиҜ•еҚ·еёҰеҸӮиҖғзӯ”жЎҲе’Ңи§ЈжһҗпјҲе№ҝдёңзңҒе№ҝе·һеёӮи¶Ҡз§ҖеҢәзңҒе®һи¶Ҡз§ҖеӯҰж Ўпјү
- зҰҸе·һеёӮй«ҳдёҖеҢ–еӯҰдёӢеҶҢжңҹдёӯиҖғиҜ•иҜ•еҚ·еёҰеҸӮиҖғзӯ”жЎҲе’Ңи§Јжһҗ



