2019-2020年高三上期期中考试化学考试(上海市同济大学第一附属中学)
| 1. 选择题 | 详细信息 |
|
下列对化学科学的认知错误的是 A.化学是一门以实验为基础的自然科学 B.化学家可以制造出自然界中不存在的物质 C.物质发生化学反应都伴随着能量变化 D.化学研究会造成严重的环境污染,人类终将毁灭在化学物质中 |
|
| 2. 选择题 | 详细信息 |
垃圾分类有利于资源回收利用下列垃圾归类不合理的是( ) A.A B.B C.C D.D |
|
| 3. 选择题 | 详细信息 |
|
下列有关化学用语表示正确的是( ) A.N2的电子式: B.S2-的结构示意图:  C.质子数为53,中子数为78的碘原子: D.邻羟基苯甲酸的结构简式:  |
|
| 4. 选择题 | 详细信息 |
|
下列关于石油的说法正确的是 A. 石油属于可再生矿物能源 B. 石油主要含有碳、氢两种元素 C. 石油裂化属于物理变化 D. 石油分馏属于化学变化 |
|
| 5. 选择题 | 详细信息 |
如图是一种有机物的模型,该模型代表的有机物可能是( ) A.饱和一元醇 B.羟基酸 C.羧酸酯 D.饱和一元醛 |
|
| 6. 选择题 | 详细信息 |
|
有关NaCl晶体的性质,正确的是( ) A.易导热 B.易熔化 C.熔融状态能导电 D.有延展性 |
|
| 7. 选择题 | 详细信息 |
|
水的离子积常数随温度升高而升高。关于一定量的水,下列叙述正确的是 A. 温度升高,水中分子总数减少 B. 水中c(OH-)随温度升高而降低 C. 水的pH随温度升高而升高 D. 水的电离过程是放热过程 |
|
| 8. 选择题 | 详细信息 |
|
CH3COOH溶液与NaHCO3溶液反应的离子方程式正确的是 A. H + HCO3 → H2O + CO2↑ B. 2CH3COOH + CO32 → H2O + CO2↑ + 2CH3COO C. CH3COOH + HCO3 → H2O + CO2↑ + CH3COO D. 2H + CO32 → H2O + CO2↑ |
|
| 9. 选择题 | 详细信息 |
|
在稳定人体血液的pH中起作用的离子是 A.Na+ B.HCO3- C.Fe2+ D.Cl- |
|
| 10. 选择题 | 详细信息 |
|
2-氯丁烷常用于有机合成等,有关2-氯丁烷的叙述正确的是( ) A.它的同分异构体除本身外还有4种 B.与硝酸银溶液混合产生不溶于稀硝酸的白色沉淀 C.微溶于水,可混溶于乙醇、乙醚、氯仿等多数有机溶剂 D.与氢氧化钠、乙醇在加热条件下的消去反应有机产物只有一种 |
|
| 11. 选择题 | 详细信息 |
一定温度下,恒容密闭容器中发生N2(g)+3H2(g) A.平衡状态Ⅱ时的c(H2)一定小 B.平衡状态Ⅱ时的c(NH3)一定大 C.平衡常数K一样大 D.平衡状态Ⅱ时的v(正)一定大 |
|
| 12. 选择题 | 详细信息 |
|
关于氯化铵溶液,下列有关说法正确的是( ) A.溶液中c(NH4+)=c(Cl-) B.加水稀释后溶液酸性增强 C.可除去某些金属表面的氧化物 D.微热促进水解平衡右移氯离子数目增多 |
|
| 13. 选择题 | 详细信息 |
|
元素的原子结构决定其性质和周期表中的位置。下列说法正确的是 A. 元素原子的最外层电子数等于元素的最高化合价 B. 多电子原子中,在离核较近的区域内运动的电子能量较高 C. P,S,Cl得电子能力和最高价氧化物对应的水化物的酸性均依次增强 D. 元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
|
| 14. 选择题 | 详细信息 |
|
室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的是 A. 溶液中导电粒子的数目减少 B. 溶液中  不变 不变C. 醋酸的电离程度增大,C(H+)亦增大 D. 再加入10mlpH=11的NaOH溶液,混合液pH=7 |
|
| 15. 选择题 | 详细信息 |
|
为探究雾霾颗粒中的可溶性成分,某课外活动小组采集雾霾颗粒样品,用蒸馏水浸取得到浸取液,取浸取液进行以下实验,其中根据实验现象得出的结论正确的是 A.滴入NaOH溶液,有白色沉淀产生,说明雾霾中一定含Mg2+ B.滴入AgNO3溶液,有白色沉淀产生,说明雾霾中一定含Cl― C.滴入硝酸酸化的BaCl2溶液,有白色沉淀产生,说明雾霾中一定含SO42― D.加入浓NaOH溶液微热,试管口的湿润红色石蕊试纸变蓝,说明雾霾中一定含NH4+ |
|
| 16. 选择题 | 详细信息 |
|
已知还原性I->Fe2+ >Br-,在只含有I-、Fe2+、Br-的溶液中通入一定量的氯气,所得溶液中可能存在的离子是( ) A.I-、Fe3+ B.Fe2+、Br- C.Fe2+、Fe3+ D.Fe2+、I- |
|
| 17. 选择题 | 详细信息 |
|
下列制取SO2、验证其漂白性、收集并进行尾气处理的装置和原理能达到实验目的的是( ) A.  制取SO2 B. 制取SO2 B. 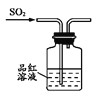 验证漂白性 验证漂白性C.  收集SO2 D. 收集SO2 D.  尾气处理 尾气处理 |
|
| 18. 选择题 | 详细信息 |
|
常温下a mol/L稀氨水和b mol/L稀盐酸等体积混合,对混合后溶液判断一定正确的是( ) A.若a<b,则c(OH-)<c(H+) B.若a=b,则c(NH4+)=c(Cl―) C.若a>b,则c(NH4+)>c(Cl―) D.若a>b,则c(OH-)>c(H+) |
|
| 19. 选择题 | 详细信息 |
下列试验中,所选装置不合理的是 A. 分离Na2CO3溶液和CH3COOC2H5,选④ B. 用CC14提取碘水中的碘,选③ C. 用FeC12,溶液吸收C12,选⑤ D. 粗盐提纯,选①和② |
|
| 20. 选择题 | 详细信息 |
H2O2分解速率受多种因素影响。实验测得 70 ℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是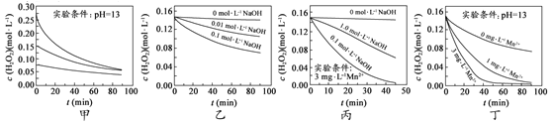 A.图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快 B.图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快 C.图丙表明,少量Mn 2+存在时,溶液碱性越强,H2O2分解速率越快 D.图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大 |
|
| 21. 填空题 | 详细信息 |
|
“常见无机物”,主要是指的铝、铁、硫、氯四种元素的单质及化合物。完成下列填空: (1)四种元素原子的半径大小Fe>__>__>__。 (2)铝原子核外电子排布式___,有___种不同能量的电子。 (3)若铝热剂的成分是铝粉与氧化铁的混合物,写出该铝热反应的化学方程式__,并标明该反应的电子转移方向和数目。 (4)工业上用氯气和___制取得到漂粉精,其有效成分是___(写化学式)。 (5)硫的非金属性___于氯(选填“强”、“弱”),请用一个事实证明___,再从原子结构的角度加以解释___。 |
|
| 22. 综合题 | 详细信息 |
|
可用以下方法处理尾气中的SO2。 方法一:活性炭还原法: 反应原理:恒温恒容2C(s)+2SO2(g) 反应进行到不同时间测得各物质的浓度如图:  (1)第一次达到平衡的时间是第___min;0~20min化学反应速率表示v(SO2)=___。 (2)30min时平衡发生移动的条件是___。 (3)40min时,平衡常数的计算式为___。(指代入具体数值的算式) 方法二:亚硫酸钠吸收法 (4)Na2SO3溶液吸收SO2的离子方程式为___; (5)如图是Na2SO3溶液中各离子浓度的相对大小关系示意图。  其中③是___。(填微粒符号) 常温下,当吸收至pH=6时,吸收液中相关离子浓度关系一定正确的是__(填序号) a.c(Na+)+c(H+)>c(SO32-)+c(HSO3-)+c(OH-) b.c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3) c.水电离出c(OH一)=1×l0-8mol/L |
|
| 23. 综合题 | 详细信息 |
聚合物F的合成路线图如图: 已知:HCHO+RCH2CHO  请据此回答: (1)A中含氧官能团名称是________________,C的系统命名为_____________________ 。 (2)检验B中所含官能团所用的试剂有______________、_____________;E→F的反应类型是______________,B+D (3)写出A→B的化学方程式__________________________________________________。 (4)写出C→D的化学方程式__________________________________________________。 (5)参照上述合成路线,设计一条由甲醛、乙醛和甲醇为主要原料制备 |
|
最近更新



