绵阳市高二化学上册期末考试同步考试检测
| 1. 选择题 | 详细信息 |
|
中国独创最大钻井平台“蓝鲸二号”助力“可燃冰”开采。下列关于“可燃冰”的说法错误的是 A.是巨大的潜在能源 B.是一种配合物 C.属于分子晶体 D.其中存在氢键 |
|
| 2. 选择题 | 详细信息 |
|
下列分子或离子的VSEPR模型与空间立体构型一致的是 A.BF3 B.NH3 C.H2O D.ClO3- |
|
| 3. 选择题 | 详细信息 |
|
处于基态的下列微粒,核外电子中未成对电子数最多的是 A.O B.P C.Cr D.Fe3+ |
|
| 4. 选择题 | 详细信息 |
|
下列图像分别表示有关反应的反应过程与能量变化的关系。据此判断下列说法正确的是 A. 石墨转变为金刚石的反应是吸热反应  B. 白磷比红磷稳定  C. S(g)=S(s) ΔH>0  D. H2(g)+I2(g) 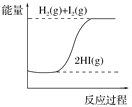 |
|
| 5. 选择题 | 详细信息 |
|
我国的超级钢研究居于世界领先地位。某种超级钢中除Fe外,还含Mn 10%、C 0.47%、Al 2%、V 0.7%。下列说法中错误的是 A.上述五种元素中,有两种位于周期表的p区 B.超级钢的晶体一定是金属晶体 C.X-射线衍射实验可以确定超级钢的晶体结构 D.超级钢中存在金属键和离子键 |
|
| 6. 选择题 | 详细信息 |
|
某同学在实验报告中记录了下列数据,其中正确的是 A.用托盘天平称取5.85 g食盐 B.用10 mL量筒量取7.35 mL盐酸 C.用pH计测出某溶液pH为3.52 D.从碱式滴定管放出酸性KMnO4溶液15.60 mL |
|
| 7. 选择题 | 详细信息 | |||||||||||||||
对下列实验事实的理论解释错误的是
|
||||||||||||||||
| 8. 选择题 | 详细信息 |
|
下列叙述错误的是 A.金属晶体中,六方最密堆积的空间利用率大于面心立方最密堆积 B.由于ZnS的晶格能大于PbS的晶格能,所以岩浆冷却时ZnS先析出 C.干冰晶体中,每个CO2分子周围距离相等且最近的CO2分子共有12个 D.AgCl沉淀不溶于硝酸,但能溶于氨水 |
|
| 9. 选择题 | 详细信息 |
|
W、X、Y、Z为原子序数依次增大的短周期元素,它们原子的最外层电子数之和为18。W的族序数是周期数的2倍,X与W位于相邻主族,Y的最外层电子数等于X的次外层电子数。下列说法正确的是 A.原子半径:Z>Y>X B.气态氢化物的热稳定性:W>X C.Y与Z可形成离子化合物 D.Z的氧化物的水化物均为强酸 |
|
| 10. 选择题 | 详细信息 |
|
NA代表阿伏加德罗常数的值。下列叙述正确的是 A.含28 g硅的SiO2晶体中存在的共价键总数为2NA B.标准状况下,2.24 L乙烯中含有的π键数目为0.1NA C.室温时,pH=2的盐酸中H+ 数目为1.0×10-2NA D.124 g P4(正四面体)中P-P键数目为4NA |
|
| 11. 选择题 | 详细信息 |
|
下列物质的性质比较,结论错误的是 A.硬度:金刚石>碳化硅>晶体硅 B.离子半径:S2->Cl->Na+>O2- C.熔点:NaF>NaCl>NaBr>NaI D.沸点:  |
|
| 12. 综合题 | 详细信息 |
298 K时,在20.0 mL 0.10 mol/L H2SO4溶液中滴入0.10 mol/L的NaOH溶液,溶液的pH与所加NaOH溶液的体积关系如图所示。下列叙述正确的是 A.滴定过程最好用甲基橙作指示剂 B.a点溶液的pH=1.0 C.b点溶液中c(H+)=0.05 mol/L D.c点对应的NaOH溶液体积为20.0 mL |
|
| 13. 选择题 | 详细信息 |
|
下列事实对应的化学用语表达错误的是 A.自然界中正常的雨水呈酸性:H2O+CO2 B.“NO2球”浸入冷水中颜色变浅:2NO2(g)(红棕色) C.硫代硫酸钠溶液与稀硫酸混合出现浑浊:S2O32-+2H+==S↓+SO2↑+H2O D.甲烷的燃烧热为ΔH=-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式为:CH4(g)+2O2(g)==CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
|
| 14. 选择题 | 详细信息 |
氧化锂(Li2O)是离子晶体,其晶格能可以通过图所示循环进行计算。下列说法错误的是 A.O=O键键能为ΔH3 B.Li原子的第一电离能为0.5ΔH2 C.Li2O的晶格能为ΔH6取正值 D.ΔH1+ΔH2+ΔH3+ΔH4+ΔH6=ΔH5 |
|
| 15. 选择题 | 详细信息 |
|
1909年,丹麦生理学家索仑生提出用pH表示水溶液的酸度:pH=-lg[H+],后来又定义pOH=-lg[OH-],pKW=-lgKW。对某水溶液的下列说法中错误的是 A.pH+pOH=pKW B.若为酸性溶液则pH>pOH C.常温下pH+pOH=14 D.溶液pH=7时未必呈中性 |
|
| 16. 选择题 | 详细信息 | |||||||||||||||
在试管中进行下列实验,现象与实验操作不相匹配的是
|
||||||||||||||||
| 17. 选择题 | 详细信息 |
常温下,甲酸和乙酸的电离常数分别为1.8×10-4和1.8×10-5。将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。两种酸用通式HY表示,下列叙述正确的是 A.曲线Ⅱ代表乙酸 B.酸的电离程度:c点>d点 C.溶液中水的电离程度:b点>c点 D.从c点到d点,溶液中 |
|
| 18. 选择题 | 详细信息 |
温度为T0时,X(g)和Y(g)在2 L的密闭容器中发生反应生成Z(g),各物质的物质的量随时间变化的关系如图a所示。其他条件相同,温度分别为T1、T2时发生反应,X的物质的量随时间变化的关系如图b所示。下列叙述中错误的是 A.反应的方程式为X(g)+Y(g) B.X(g)与Y(g)生成Z(g)的反应是放热反应 C.图a中反应达到平衡时,Y的转化率为62.5% D.T1时,若该反应的平衡常数K的值为50,则T1>T0 |
|
| 19. 综合题 | 详细信息 |
|
在建国70周年阅兵仪式上,“歼20”“东风-41核导弹”等国之重器亮相,它们采用了大量合金材料。回答下列问题: (1)早期战斗机主要采用铝合金,其中超硬铝属Al-Cu-Mg-Zn系。Cu在元素周期表中的位置是_____________,比较第一电离能Al______Mg(填“>”“<”“=”)。 (2)查阅资料显示第二电离能Cu大于Zn,理由是_______________。 (3)中期战斗机主要采用钛合金,Ti的价电子排布图为___________________。钛晶体在882 ℃以上为体心立方的β钛,其中钛原子的配位数为_______。 (4)钛镍合金可用于战斗机的油压系统,该合金溶于热的硫酸生成Ti(SO4)2、NiSO4,其中阴离子的立体构型为___________,S的_______杂化轨道与O的2p轨道形成_____键(填“π”或“σ”)。 (5)一种钛镍合金的立方晶胞结构如图所示,若晶胞的边长为a pm,则晶胞的密度为________g/cm3(用含a、NA的计算式表示)。  (6)隐形战机采用Fe(CO)5(羰基铁)作为吸波材料,羰基铁在常温下为红棕色液体,固体羰基铁属于_________晶体,CO与Fe之间的化学键称为________。与CO互为等电子体的分子或离子是______(只写一种)。 |
|
| 20. 实验题 | 详细信息 |
|
某学习小组欲测定市售橙汁饮料中维生素C的含量。每100克鲜榨橙汁中含有大约37.5毫克的维生素C。实验室可用碘量法测定橙汁饮料中维生素C的含量,反应的方程式为C6H8O6+I2==C6H6O6+2HI(维生素C化学式为C6H8O6,相对分子质量为176),其实验步骤及相关数据如下: ①标准溶液的稀释:移取浓度为0.0080 mol/L的碘标准溶液25.00 mL于250 mL容量瓶中,定容,摇匀备用。 ②移取10.00 mL饮料样品(设密度为1.0 g/cm3)于250 mL锥形瓶中,加入50 mL蒸馏水,2 mL指示剂。 ③在滴定管中装入稀释后的标准溶液,滴定至终点,读取并记录相关数据。 ④重复测定3次,数据记录如下表。  回答下列问题: (1)实验中盛装标准溶液应选择______(填“酸式”或“碱式”)滴定管。 (2)步骤2中加入的指示剂是___________,判断滴定达到终点的现象是__________。 (3)实验中下列操作可能导致测定结果偏低的是_______(填标号)。 A.稀释标准溶液定容时俯视刻度线 B.滴定结束时俯视读 C.在锥形瓶中加入样品后放置较长时间才开始滴定 D.滴定管尖嘴部分有气泡,滴定后消失 (4)计算该饮料样品中维生素C含量为________mg/100 g。该含量______(填“高于”或“低于”)鲜榨橙汁。 |
|
| 21. 填空题 | 详细信息 |
常温下 0.1 mol/L的H2A溶液中H2A、HA-、A2- 在三者中所占物质的量分数(分布系数)随pH变化的关系如图所示。回答下列问题: (1)H2A的电离方程式是__________________,二级电离常数K2=_________。 (2)已知25 ℃时HF的Ka=10-3.45,将少量H2A的溶液加入足量NaF溶液中,发生反应的离子方程式为_______________________。 |
|
| 22. 实验题 | 详细信息 | |||||||||
某化学实验小组用酸性KMnO4溶液与草酸(H2C2O4)溶液反应,研究外界条件对反应速率的影响,实验操作及现象如下:
|
||||||||||
| 23. 计算题 | 详细信息 |
在某温度(T ℃)的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L,x与y关系如图所示。 (1)该温度下,水的离子积为________,T ℃_____25 ℃(填“大于”“小于”或“等于”)。 (2)将此温度下pH=11的NaOH溶液与pH=1的HCl溶液等体积混合,混合后溶液的pH约为________。(已知lg2=0.3) (3)在此温度下,将pH=13的NaOH溶液Va L与pH=1的硫酸溶液Vb L混合。若所得混合液的pH=2,则Va:Vb =_______。 |
|
| 24. 综合题 | 详细信息 |
|
甲醇是重要的化工原料,利用合成气(CO、H2、CO2)在催化剂的作用下合成甲醇,可能发生的反应如下: ① CO2(g)+3H2(g) ② CO(g)+2H2(g) ③ CO2(g)+H2(g) (1)反应③的ΔH3=________,化学平衡常数K3与K1、K2的代数关系是K3=_____。 (2)要使反应②的速率和转化率都增大,需要改变的条件是___________。在5 MPa下,要提高反应②的转化率,可采取的措施有__________、_________(答两条)。 (3)若反应①在恒容密闭容器中进行,下列可以判断该反应达到平衡的是_______(填标号)。 A.v正(H2)=v逆(CH3OH) B.混合气压强不变 C.c(H2)与c(H2O)比值不变 D.混合气密度不变 (4)在一定温度和催化剂存在下,向1 L密闭容器中充入1 mol CO2和3 mol H2发生反应①。当CO2的平衡转化率为50%时,产物甲醇的体积分数为________,该温度下,正反应的平衡常数K=__________。若向容器中再充入0.5 mol H2和0.5 mol H2O(g),其他条件不变时平衡_______移动(填“正向”“逆向”“不”)。 |
|




