2019年湖南省岳阳市中考化学模拟试卷带参考答案和解析
| 1. | 详细信息 |
|
下列变化属于化学变化的是( ) A.冰雪融化 B.纸张燃烧 C.水果榨汁 D.海水晒盐 |
|
| 2. | 详细信息 |
|
下列实验操作正确的是( )。 A.蒸发溶液时,在蒸发皿下必须垫石棉网 B.用天平称量时左盘放砝码、右盘放药品 C.点燃可燃性气体前,一定要验纯 D.CO还原CuO结束时,先停气、后熄酒精灯 |
|
| 3. | 详细信息 |
|
某果园中的绿橙因缺氮生长不良,叶色泛黄,应施用下列化肥中的( ) A. KCl B. CO(NH2)2 C. Ca(H2P04)2 D. K2CO3 |
|
| 4. | 详细信息 |
|
2018年3月22日是第二十六届“世界水日”,3月22日至3月28日是第三十一届“中国水周”。下列有关水的认识中错误的是( ) A. 大量使用农药、化肥,会造成水体污染 B. 水通过三态变化实现天然循环,其主要是通过化学变化完成的 C. 水是生命之源,保护水资源包括防治水体污染和节约用水两方面 D. 电解水的实验装置中,正极和负极产生的气体体积比为1∶2 |
|
| 5. | 详细信息 |
某反应前后分子变化的微观示意图如图所示,下列说法错误的是( )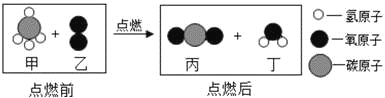 A. 生成物均为氧化物 B. 甲是有机物,乙、丙、丁是无机物 C. 点燃前,要先检验甲的纯度,防止爆炸 D. 参加反应的甲、乙微粒个数比为1:2 |
|
| 6. | 详细信息 |
|
今年全国“两会”代表委员们使用的“石头纸”,是以碳酸钙为主要材料,经特殊工艺处理后制成的。碳酸钙属于 A. 氧化物 B. 酸 C. 碱 D. 盐 |
|
| 7. | 详细信息 |
|
制造汽车要用到含铜、铁、铝等金属材料。对金属材料的说法正确的是( ) A.车体多用钢材制造,其表面喷漆只是为了美观 B.工业上用二氧化碳还原赤铁矿冶炼金属铁 C.铜、铁、铝在一定条件下都能发生置换反应 D.在实验室中探究铝、铜的金属活动性顺序,除铝、铜外,还要用到的试剂是浓硫酸 |
|
| 8. | 详细信息 |
|
将下列物质同时加入到水中,能大量共存且得到无色透明溶液的是( ) A.K2CO3、BaCl2、NaOH B.CaC12、HCl、KNO3 C.KOH、HCl、(NH4)2SO4 D.Fe2O3、KCl、NaNO3 |
|
| 9. | 详细信息 |
|
下列家庭实验不会成功的是 A. 用缝衣针淬火处理后制钓鱼钩 B. 用6B铅笔芯做导电性实验 C. 用等质量的同种白糖加入等量热水与冷水中,比较溶解速率 D. 用冷碟子放在蜡烛火焰上制取炭黑 |
|
| 10. | 详细信息 |
|
写出下列反应的文字表达式,注明反应类型: (1)电解水______(反应类型______) (2)氢气与氧气点燃______(反应类型______) |
|
| 11. | 详细信息 |
|
2016年3月22日是第二十四届“世界水日”,今年的宣传主题是“水与就业”,请你回答下列问题: (1)淡水资源有限,我们需要节约用水,如图1中表示节水标志的是_____(填字母);  (2)自然界中的淡水需要净化才能成为我们使用的自来水,净化过程中可以通过_____操作去除水中的不溶物;利用活性炭,不仅可以除去水中的不溶性杂质,还可以_____; (3)水的硬度过大会影响生产和生活,生活中我们可以利用_____来鉴别硬水和软水,然后利用_____的方法来降低水的硬度; (4)爱护水资源从我做起,下列做法不可行的是_____(填序号) A洗脸、刷牙时随手关闭水龙头 B用洗过衣服的水冲马桶 C用洗衣机洗一件衬衫 D使用节水型马桶 (5)图2是电解水的实验装置图,请你回答:试管A中收集到的气体是_____,若该气体的体积为8mL,则试管B中收集到的气体体积为_____mL,该反应的文字表达式为_____。 |
|
| 12. | 详细信息 |
甲、乙、丙三种固体的溶解度曲线如图所示,据图回答: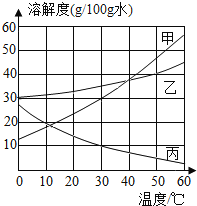 (1)30℃时,丙的溶解度是________; (2)50℃时,在100g水中放入50g乙物质,充分搅拌后所得溶液的溶质质量分数为________。(计算结果保留至0.1%); (3)若将20℃时甲、乙、丙三种物质的饱和溶液升温至40℃(不考虑水的蒸发),可析出晶体的是________; (4)将50℃时甲、乙、丙三种物质的饱和溶液均降温至10℃,所得溶液的溶质质量分数从大到小的顺序是________。 |
|
| 13. | 详细信息 |
化学是一门以实验为基础的科学,根据下图所示装置回答有关问题: (1)仪器①的名称是__________。 (2)李丽同学设计了实验室制取并收集二氧化碳的装置(如图C所示),装置中出现了一处错误,你的纠正方法是__________。该装置的发生装置具有的优点是__________。锥形瓶中发生反应的化学方程式为__________。 (3)实验室利用图A所示装置制取氧气的化学方程式为__________。 (4)实验室可以用加热氯化镁和熟石灰固体混合物的方法制取氨气。已知氨气是一种无色有刺激性气味的气体,密度比空气小,极易溶于水。为了制取并收集一瓶干燥的氨气,且减少对空气的污染。在上述装置中选出最佳的实验装置组合是__________(填字母编号)。 |
|
| 14. | 详细信息 | |
|
叠氮化钠(NaN3)被广泛应用于汽车安全气囊,某兴趣小组对其进行下列研究. (应用研究) (1)汽车经撞击后,30毫秒内引发NaN3,迅速分解为Na、N2,反应方程式为_______。 (制备研究) (2)将金属钠与液态氨反应得NaNH2,再将NaNH2与N2O反应可生成NaN3、NaOH和 气体X,该反应的化学方程式为2NaNH3+N2O = NaN3+NaOH+X,实验室检验X 气体使用的试纸是湿润________。 (Na2CO3质量分数测定) 工业级NaN3中常含有少量的Na2CO3,为测定样品中Na2CO3的质量分数设计如图装置(已知H2SO4溶液与NaN3,反应不生成气体)。 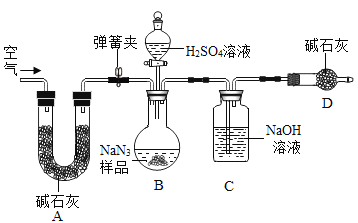 (3)装置A的作用是_____。设计的实验步骤为:①精确称量样品,检查装置气密性;②打开弹簧夹,鼓入空气,称量装置C;③关闭弹簧夹,打开分液漏斗活塞;④再打开弹簧夹,_______;⑤再次称量装置C。计算碳酸钠含量至少需要测定______(填数字)个数据。根据制备反应,分析工业级NaN3中含有Na2CO3的可能原因_______。
|
||
| 15. | 详细信息 |
|
三亚硝酸氮的化学式为N(NO2)3,是科学家2011年发现的一种新型火箭燃料。试计算: (1)亚硝酸根NO2-的化合价为-1,则化学式中加黑点的氮元素化合价为____________; (2)三亚硝酸氮分子中氮、氧原子的个数比为_________; (3)三亚硝酸氮的相对分子质量为___________; (4)三亚硝酸氮中氮元素和氧元素的质量比为__________; (5)三亚硝酸氮中氮元素的质量分数为_______(精确到0.1%); (6)100g三亚硝酸氮中氮元素的质量为______(保留一位小数)。 |
|
| 16. | 详细信息 |
| 我校实践活动小组的同学,对某一工厂排放的废水进行检测,发现主要污染物是氢氧化钠,为了测定废水中氢氧化钠的含量,他们取 160g 废水于烧杯中,逐渐加入溶 质质量分数为 5%的稀盐酸至 146g 时恰好完全反应(废水中的其他成分不与盐酸反应)。求: (1)所用稀盐酸中溶质的质量为____g。 (2)废水中氢氧化钠溶质的质量分数____(写计算过程)。 | |
最近更新




