江苏省淮安市洪泽区、金湖县2020-2021年九年级上期期末化学免费试卷带答案和解析
| 1. 选择题 | 详细信息 |
|
下列过程中,一定发生化学变化的是() A.蜡烛燃烧 B.矿石粉碎 C.冰雪融化 D.酒精挥发 |
|
| 2. 选择题 | 详细信息 |
|
组成人体的元素中含量最多的是 ( ) A. 碳 B. 氢 C. 氧 D. 氟 |
|
| 3. 选择题 | 详细信息 |
|
下列化学用语的表述正确的是 A.5个氮原子:5N B.2个钙离子:2Ca+2 C.铝元素的元素符号:Ag D.氯化镁的化学式:mgCL2 |
|
| 4. 选择题 | 详细信息 |
|
规范的实验操作是化学实验成功的关键,下列实验操作规范的是 A.气体验满  B.量筒读数 B.量筒读数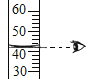 C.点燃酒精灯  D.移开蒸发皿 D.移开蒸发皿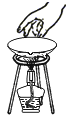 |
|
| 5. 选择题 | 详细信息 | ||||||||||||||||||||
下列对溶液中溶质、溶剂的判断正确的是
|
|||||||||||||||||||||
| 6. 选择题 | 详细信息 |
|
2019年5月12日是我国第11个“防灾减灾日”,了解防灾减灾的相关知识,有利于保护人们的生命、财产安全。下列关于火灾、灭火与逃生的说法错误的是 A.炒菜时油锅着火,用锅盖盖灭是为了隔绝空气 B.家中天燃气泄漏着火,应先关闭天燃气阀门再实施灭火 C.房屋失火,用水浇灭是为了降低可燃物的着火点 D.逃离火灾现场时,可用湿毛巾捂住口鼻,并尽量贴近地面逃离 |
|
| 7. 选择题 | 详细信息 |
|
瑞德西韦( Remdesivir,化学式为C27H35N6O8P)是一种治疗新冠病毒肺炎的临床试验药物。下列关于瑞德西韦的描述不正确的是 A.由碳、氢、氧、氮、磷五种元素组成 B.相对分子质量为602g C.一个分子中含有77个原子 D.碳、氧两种元素的原子个数比为27:8 |
|
| 8. 选择题 | 详细信息 |
|
为了防止钢铁制品锈蚀,下列做法不当的是 A.在铁制品表面镀上一层锌 B.在脸盘、杯子等表面烧涂搪瓷等 C.将使用后的刀具用布擦干 D.用洗涤剂除去铁制品表面的油膜 |
|
| 9. 选择题 | 详细信息 |
某反应前后分子变化的微观示意图如下。 “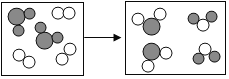 A.反应物中没有单质 B.图中共表示了9种物质 C.有反应物过量未参加反应 D.该反应可表示为: |
|
| 10. 选择题 | 详细信息 |
化学兴趣小组同学采用图1装置对可燃性粉尘爆炸进行探究,并用传感器测定容器内爆炸时压强与可燃性粉尘直径、可燃性粉尘浓度的关系如图2、图3所示。下列说法正确的是  A.该实验中若容器无盖,鼓入的可燃性粉尘也会爆炸 B.该实验中用打气筒鼓入空气的速度对实验结果没有影响 C.根据图2可知,可燃性粉尘颗粒直径越小,爆炸威力越大 D.根据图3可知,容器中可燃物粉尘的浓度越大,爆炸威力越大 |
|
| 11. 填空题 | 详细信息 |
|
用符合要求的物质的序号填空。 ①石墨 ②硬铝 ③金刚石 ④半导体硅晶片 (1)可用于玻璃切割的是_____。 (2)可用于飞机制造的是_____。 (3)可用于制造计算机芯片的是_____。 (4)可用于制作电池电极材料的是_____。 |
|
| 12. 填空题 | 详细信息 |
|
生活中处处有化学。 (1)为了全民健康,卫生部推广使用“强化加铁酱油”。这里的“铁”是指_____(填“单质”或“元素”)。 (2)厨房中,用洗洁精除餐具表面的残留食用油,利用了洗净精的_____作用。 (3)用肥皂洗衣服时发现泡沫很少,且有浮渣产生,这一现象说明当地的水为_____(填“硬水”或“软水”);长期使用硬水不利于身体健康,生活中常用煮沸将其软化。 |
|
| 13. 填空题 | 详细信息 |
甲和乙(氯化钠)两种物质的溶解度曲线如图所示。 (1)20℃时,乙物质的溶解度是_____。 (2)氯化钠是由Cl-和_____构成的(填写微粒符号)。 (3)在40℃时,在保持溶质质量分数不变的情况下,若把接近饱和的甲溶液变成饱和溶液,除了降温之外还可以可采取的方法为_____。 (4)下列说法正确的是_____。 A 甲、乙两物质的溶解度随温度的升高而增大 B 20℃时,向125g溶质质量分效为20%的乙溶液中加入15g乙固体并振荡,有固体不溶解 C 40℃时,使乙的饱和溶液析出晶体可用加热升温、冷却降温和蒸发溶剂三种方法 D 将相同质量的甲和乙的饱和溶液分别从40℃降温至10℃,甲析出晶体的质量多 |
|
| 14. 流程题 | 详细信息 |
生命离不开水,生活中也离不开水。水可以用来洗涤,这说明水具有溶解性质。我们一般用到的水往往都是自来水,下图是某地自来水厂生产的一般流程: (1)利用了活性炭的_____(填“物理”或“化学”)性质,除掉水中的一些可溶的有色和有臭味的物质。 (2)“投药”过程一般是加入适量氯气,所起的作用是_____。 (3)该图中有一处标注不尽合理,请指出并说出你的理由是_____。 |
|
| 15. 流程题 | 详细信息 |
已知氧化铜可以和稀硫酸反应生成硫酸铜和水,某工厂处理回收含铜废料的生产流程如下: 请回答: (1)流程①中“灼烧”目的是_____便于硫酸溶解、除去可燃、易分解的杂质。 (2)流程②中加入足量稀硫酸生成蓝色溶液的化学方程式是_____;不选用盐酸主要是因为盐酸具有_____性,对环境污染更多些。 (3)流程②过滤后所得蓝色溶液仍有少量悬浮物,解决的方法是_____。 (4)流程③加入铁屑后发生反应的化学方程式是_____,该反应所属的基本反应类型是_____。 |
|
| 16. 实验探究题 | 详细信息 |
根据下列实验装置图,回答有关问题。 (1)写出装置图中标号①的仪器名称_____。 (2)实验室用高锰酸钾制取氧气的化学方程式为_____。选用装置A与D制取氧气,实验步骤如下: ①先检验装置的气密性,再加入药品; ②先让试管均匀受热,再对药品所在的部位加热; ③导管口开始有气泡放出后,立即收集; ④停止加热时,先熄灭酒精灯,再把导管移出水面。 以上实验步骤的叙述中,正确的是_____(填序号)。 (3)若用装满水的F装置收集氧气,则气体从_____处导管进入(填“b”或“c”),若要用水将瓶中氧气排出使用,水应从_____处导管进入。 |
|
| 17. 实验探究题 | 详细信息 |
实验室配制一定溶质质量分数的氯化钠溶液的流程如下图所示:  (1)应称量_____g氯化钠固体,需加水_____mL(水的密度为1g·mL-1)。 (2)若称量氯化钠固体时指针向左偏转,则应_____直到天平平衡。 〔3)实验中发现氯化钠固体已结块,为了较快地溶解,合理的方法有_____(填序号)。 A 用玻璃棒搅拌 B 用玻璃棒将固体捣碎 C 适当地加热 (4)下列操作中可能导致配制氯化钠溶液的溶质质量分数偏大的是_____(填序号)。 A 氯化钠中含有杂质 B 量取水时俯视 C 内壁有少量水的烧杯溶解氯化钠 D 转移时,有少量溶液溅出 (5)取上述溶液10g,需加_____g水稀释,可得到5%的氯化钠溶液。 |
|
| 18. 实验探究题 | 详细信息 |
工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4.为了测定铁红中铁的质量分效,某兴趣小组的同学进行了如下实验,请你参与过程分析。 (查阅资料)碱石灰能充分吸收CO2,主要原理是: (问题讨论) (1)铁的矿物中主要成分为Fe2O3的是_____。 A 磁铁矿 B 黄铁矿 C 赤铁矿 D 菱铁矿 (2)写出装置A玻璃管中炭粉的作用是_____。 (3)实验开始时,应先点燃_____(填“A”或“B”)装置中的酒精喷灯。 (实验评价)整套装置存在一些明显的不足之处 (4)甲同学建议在装置A、B之间增加盛有浓NaOH溶液的洗气瓶和盛有澄清石灰水的洗气瓶,NaOH溶液洗气的目的是_____。 (5)乙同学建议在装置D处放置燃着的酒精灯以点燃尾气,同学们认为在点燃之前,应对尾气先_____以确保安全。 (数据计算) (6)实验中所需的CO2可以用碳酸钠(Na2CO3)与稀盐酸快速反应制备,反应的化学方程式为: |
|
最近更新



