四川2019年高三化学下半期月考测验免费试卷
| 1. 选择题 | 详细信息 |
|
化学与生活联系密切, 下列说法错误的是 A. 氯化钠是生活中常用的食品防腐剂 B. 浓香型白酒的香源成分己酸乙酯属于油脂 C. 草木灰中提取的 K2CO3可以去除餐具上的油污 D. 人们已开始试用 ClO2和O3作新的自来水消毒剂 |
|
| 2. 选择题 | 详细信息 |
|
下列关于有机化合物的说法错误的是 A. 纤维素属于天然高分子化合物 B. 可用溴水来鉴别乙苯和苯乙烯 C. 苯只能发生氧化反应和取代反应 D. 葡萄糖和果糖互为同分异构体 |
|
| 3. 选择题 | 详细信息 |
|
NA表示阿伏加德罗常数的值, 下列叙述正确的是 A. 1mol H2O中含有的极性共价键数目为2NA B. 16 g16O2和18O2混合物中含有的质子数目为8NA C. Zn和浓硫酸反应得到22.4LSO2和 H2混合气体时, 转移的电子数为4NA D. 标准状况下2 mol NO与1 mol O2充分反应后分子数共2NA |
|
| 4. 选择题 | 详细信息 | |||||||||||||||
下列实验操作不能实现对应实验目的的是
|
||||||||||||||||
| 5. 选择题 | 详细信息 |
|
W、 X、 Y、 Z均为短周期元素且原子序数依次增大, W和 X形成的气态化合物的水溶液显碱性,Y的 M层电子数与 K层电子数之和为 L层电子数的一半, Z的低价氧化物和其气态氢化物可以反应得到 Z的淡黄色单质。下列说法正确的是 A. Y与 Z的单质混合加热能反应 B. X、 Y、 Z的简单离子半径: X<Y<Z C. Z的含氧酸酸性强于 X的含氧酸 D. 单质的还原性: W >Y |
|
| 6. 选择题 | 详细信息 |
如图所示阴阳膜组合电解装置用于循环脱硫,用NaOH溶液在反应池中吸收尾气中的二氧化硫,将得到的Na2SO3溶液进行电解又制得NaOH。其中a、b离子交换膜将电解槽分为三个区域,电极材料为石墨,产品C为H2SO4溶液。下列说法正确的是( ) A. b为只允许阳离子通过的离子交换膜 B. 阴极区中B最初充入稀NaOH溶液,产品E为氧气 C. 反应池采用气、液逆流方式,目的是使反应更充分 D. 阳极的电极反应式为SO32-+2e-+H2O===2H++SO42- |
|
| 7. 选择题 | 详细信息 |
常温下, 将稀 HCl溶液滴加到等浓度的弱碱 AOH溶液中, 测得混合液的 pH和lg[C(AOH)/C(A+)] 的关系如图所示, 其中 a点表示未加盐酸时的数据, e点表示 HCl和 AOH恰好完全反应时的数据。下列说法错误的是 A. 常温下, A+的水解平衡常数为 1.0×10-10 B. 点e溶液中水电离出的H+浓度为 10-6.23mol/L C. 点c 溶液中的 n(A+)+n(AOH)等于点 e溶液中的 n(Cl-) D. 点d溶液中: c(Cl-)> c(AOH)>c(A+) |
|
| 8. 实验题 | 详细信息 |
|
锌锰干电池的负极是作为电池壳体的金属锌,正极是被二氧化锰和碳粉包围的石墨电极,电解质是氯化锌和氯化铵的糊状物,该电池放电过程中产生 MnOOH。废旧电池中的Zn、Mn元素的回收,对环境保护有重要的意义。 Ⅰ. 回收锌元素,制备ZnCl2 步骤一:向除去壳体及石墨电极的黑色糊状物中加水,搅拌,充分溶解,经过滤分离得固体和滤液。 步骤二:处理滤液,得到ZnCl2·xH2O晶体。 步骤三:将SOCl2与ZnCl2·xH2O晶体混合制取无水ZnCl2。 制取无水ZnCl2,回收剩余的SOCl2并验证生成物中含有SO2(夹持及加热装置略) 的装置如下:  (已知: SOCl2是一种常用的脱水剂,熔点-105℃,沸点79℃,140℃以上时易分解,与水剧烈水解生成两种气体。) (1)写出SOCl2与水反应的化学方程式:______________________。 (2)接口的连接顺序为a→___→___→ h → h →___→___→___→e。______________ Ⅱ. 回收锰元素,制备MnO2 (3)洗涤步骤一得到的固体,判断固体洗涤干净的方法:_________________________。 (4)洗涤后的固体经初步蒸干后进行灼烧,灼烧的目的__________________________。 Ⅲ. 二氧化锰纯度的测定 称取1.40g灼烧后的产品,加入2.68g草酸钠(Na2C2O4)固体,再加入足量的稀硫酸并加热(杂质不参与反应),充分反应后冷却,将所得溶液转移到100mL容量瓶中用蒸馏水稀释至刻线,从中取出20.00mL,用0.0200mol/L高锰酸钾溶液进行滴定,滴定三次,消耗高锰酸钾溶液体积的平均值为17.30mL。 (5)写出MnO2溶解反应的离子方程__________________________________________。 (6)产品的纯度为______________________ 。 (7)若灼烧不充分,滴定时消耗高锰酸钾溶液体积_____(填“偏大”、“ 偏小”、“ 不变”)。 |
|
| 9. 综合题 | 详细信息 | |||||||||||||||
|
当发动机工作时,反应产生的NO尾气是主要污染物之一,NO的脱除方法和转化机理是当前研究的热点。请回答下列问题: (1)已知:2NO(g)+O2 (g) =2NO2(g) △H1= -113kJ/mol 6NO2(g)+O3(g)=3N2O5(g) △H2= -227 kJ/mol 4NO2 (g)+O2(g)=2N2O5(g) △H3= -57 kJ/mol 则 2O3(g)= 3O2(g)是_________反应(填“放热”或“吸热”),以上 O3氧化脱除氮氧化物的总反应是NO(g)+O3(g)=NO2(g)+O2(g) △H4=_______kJ/mol,最后将NO2与_________剂反应转化为无污染的气体而脱除。
|
||||||||||||||||
| 10. | 详细信息 |
钛酸锂电池应用广泛, 电池放电后负极材料主要含有Li4Ti5O12、 铝箔及少量Fe, 可通过下列工艺流程回收钛、 锂。回答下列问题: (1) Li4Ti5O12中, Ti元素的化合价为___, 滤液1中含金属的阴离子是___(填离子符号)。 (2) 酸浸时 Li4Ti5O12发生的反应是: Li4Ti5O12+7H2SO4+5H2O2=2Li2SO4+5[TiO(H2O2)]SO4+7H2O, 该反应是否属于氧化还原反应?___(填 “是” 或 “否”); 滤渣1是___。 (3) 向[TiO(H2O2)]SO4溶液中加入Na2SO3溶液发生反应的离子方程式为___。 (4) 向TiOSO4溶液中通入NH3发生反应的离子方程式为___。 (5) 沉淀TiO(OH)2用蒸馏水洗涤的目的是___。 (6) 萃取时, 温度对萃取率的影响如图所示。由图分析知实验时选择在常温下进行即可, 理由是__。  (7)“萃取” 和 “反萃取” 可简单表示为:[TiO(H2O2)]2++2(HA)2 |
|
| 11. 综合题 | 详细信息 |
|
钴、 铜及其化合物在工业上有重要用途, 回答下列问题: (1) 请补充完基态Co的简化电子排布式: [Ar]_________, Co2+有_______个未成对电子。 (2) Na3[Co(NO2)6]常用作检验K+的试剂, 配位体NO2-的中心原子的杂化形式为________, 空间构型为_____。大π键可用符号 (3) 配合物[Cu(En)2]SO4的名称是硫酸二乙二胺合铜(Ⅱ), 是铜的一种重要化合物。其中 En 是乙二胺(H2NCH2CH2NH2)的简写。 ①该配合物[Cu(En)2]SO4中N、 O、 Cu的第一电离能由小到大的顺序是______________。 ②乙二胺和三甲胺[N(CH3)3]均属于胺, 且相对分子质量相近, 但乙二胺比三甲胺的沸点高得多, 原因是______________________________________________________。  (4) 金属Cu晶体中的原子堆积方式如图所示, 其配位数为______, 铜的原子半径为a nm, 阿伏加德罗常数的值为NA, Cu的密度为_________g/cm3(列出计算式即可)。 |
|
| 12. 综合题 | 详细信息 |
盐酸普鲁卡因 (  ) 是一种良好的局部麻醉药, 具有毒性小, 无成瘾性等特点。其合成路线如下图所示: ) 是一种良好的局部麻醉药, 具有毒性小, 无成瘾性等特点。其合成路线如下图所示: 回答下列问题: (1) 3molA可以合成1molB, 且B是平面正六边形结构, 则B的结构简式为_________。 (2) 有机物C的名称为____________, B→C的反应类型为_____________。 (3) 反应C→D的化学方程式为________________________________________。 (4) F和E发生酯化反应生成G, 则F的结构简式为___________________。 (5) H的分子式为____。 (6) 分子式为C9H12且是C的同系物的同分异构体共有__________种。 (7) 请结合上述流程信息, 设计由苯、 乙炔为原料合成 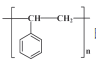 的路线_______________ 。(其他无机试剂任选) 的路线_______________ 。(其他无机试剂任选) |
|