临夏回族自治州永靖县移民中学高三化学上册期中考试考试完整版
| 1. 选择题 | 详细信息 |
|
用NA代表阿伏加德罗常数的值,下列叙述正确的是 ( ) A.78g过氧化钠晶体中,含2NA个阴离子 B.常温常压下,22.4L氦气含有NA个氦原子 C.在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定是4NA D.常温下16g O2与O3的混合气体中含氧原子数为NA |
|
| 2. 选择题 | 详细信息 |
|
下列关于胶体的叙述正确的是 A.胶体粒子不能透过滤纸 B.胶体和溶液的本质区别是胶体能发生丁达尔现象 C.胶体带电,故在电场作用下会产生电泳现象 D.用渗析的方法净化胶体时,使用半透膜只能让小分子和离子通过 |
|
| 3. 选择题 | 详细信息 |
|
常温下,下列各组离子在指定溶液中能大量共存的是 A.pH=1的溶液中: Fe2+、NO3-、SO42-、Na+ B.由水电离的c(H+)=1×10-14 mol·L-1的溶液中:Ca2+、K+、Cl-、HCO3- C.c(H+)/c(OH-)=1012的溶液中: NH4+、Al3+、NO3-、Cl- D.加入苯酚显紫色的溶液: K+、ClO-、SO42-、SCN- |
|
| 4. 选择题 | 详细信息 |
|
分类是化学学习与研究的常用方法,下列分类正确的是 A.Na2O、MgO、Al2O3均属于碱性氧化物 B.石灰石、生石灰、熟石灰均属于碱 C.酸、碱、盐之间发生的反应均属于复分解反应 D.混合物、分散系、胶体从属关系如右图所示  |
|
| 5. 选择题 | 详细信息 |
|
2011年9 月29日,“长征-2F”运载火箭成功将“天宫一号”目标飞行器送上太空,火箭中使用的燃料是偏二甲肼(CH3-NH-NH-CH3)和四氧化二氮(N2O4)。在火箭升空过程中,燃料发生反应:CH3-NH-NH-CH3+2N2O4→2CO2+3N2+4H2O提供能量。下列叙述正确的是 A.该燃料绿色环保,在燃烧过程中不会造成任何环境污染 B.该反应中N2O4是氧化剂,偏二甲肼是还原剂 C.CO2是氧化产物,N2是还原产物 D.每有0.6 mol N2生成,转移电子数目为2.4NA |
|
| 6. 选择题 | 详细信息 |
工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下: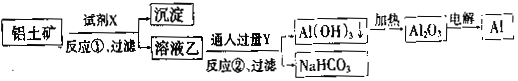 下列叙述正确的是( ) A.反应②的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3 B.反应①、过滤后所得沉淀为氢氧化铁 C.图中所示转化反应都不是氧化还原反应 D.试剂X可以是氢氧化钠溶液,也可以是盐酸 |
|
| 7. 选择题 | 详细信息 |
|
下列说法中正确的是 ( ) A. 1 L水中溶解了58.5gNaCl,该溶液的物质的量浓度为1 mol/L B. 从1L2mol/L的H2SO4溶液中取出0.5L,该溶液的浓度为1mol/L C. 配制500mL0.1 mol·L-1的CuSO4溶液,需8.0g 无水CuSO4 D. 中和100mL1mol/L的H2SO4溶液,需NaOH为4.0 g |
|
| 8. 选择题 | 详细信息 |
|
0.6mol·L-1Fe2(SO4)3和1.2mol·L-1CuSO4的混合溶液200mL,加入一定量铁粉充分反应后,测得溶液中Fe2+与Cu2+物质的量之比为2:1,则加入铁粉的物质的量为( ) A.0.30mol B.0.22mol C.0.16mol D.0.48mol |
|
| 9. 选择题 | 详细信息 | ||||||||||||||||||||
向四支试管中分别加入少量不同的无色溶液并进行如下操作,其中结论正确的是
|
|||||||||||||||||||||
| 10. 选择题 | 详细信息 |
对 的表述不正确的是 的表述不正确的是A.该物质能发生缩聚反应 B.该物质的核磁共振氢谱上共有7个峰 C.该物质遇FeCl3溶液显色,1mol该物质最多能与含1mol Br2的溴水发生取代反应 D.1 mol该物质最多消耗Na、NaOH、NaHCO3的物质的量之比为2:2:1 |
|
| 11. 选择题 | 详细信息 |
|
有一真空储气瓶,净重500g。在相同条件下,装满氧气后重508g,装满另一种气体X 时重511g,则X的相对分子质量为( ) A.44 B.48 C.64 D.71 |
|
| 12. 选择题 | 详细信息 |
|
甲酸甲酯、乙酸丁酯、丙酸甲酯组成的混合脂中,若氧元素的质量分数为30%,那么氢元素的质量分数为 A. 10% B. 15% C. 20% D. 无法确定 |
|
| 13. 选择题 | 详细信息 |
|
由两分子乙炔聚合得到CH2=CH—C≡CH ,继续和氯化氢发生加成反应得到CH2=CH—CCl=CH2,所得产物加成聚合后得到354g A.624g B.416g C.312g D.208g |
|
| 14. 选择题 | 详细信息 |
|
能正确表示下列反应的离子方程式是( ) A.醋酸钠的水解反应 B.碳酸氢钙与过量的NaOH溶液反应Ca2++2 C.苯酚钠溶液与二氧化碳反应 C6H5O—+ CO2+ H2O=C6H5OH+ D.稀硝酸与过量的铁屑反应 3Fe+8H++2 |
|
| 15. 选择题 | 详细信息 |
|
甲、乙、丙、丁分别是Al2(SO4)3、FeSO4、NaOH、BaCl2四种物质中的一种,若将丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加则沉淀消失,丁溶液滴入甲溶液时,无明显现象发生,据此可判断丙物质是( ) A.Al2(SO4)3 B.NaOH C.BaCl2 D.FeSO4 |
|
| 16. 选择题 | 详细信息 |
|
下列有关NaHCO3和Na2CO3性质的比较中,正确的是 ( ) A. 热稳定性:Na2CO3<NaHCO3 B. 常温时在水中的溶解度:Na2CO3<NaHCO3 C. 等物质的量的NaHCO3和Na2CO3与足量稀盐酸反应,NaHCO3放出的CO2多 D. 等质量的NaHCO3和Na2CO3与足量稀盐酸反应产生CO2的量:Na2CO3<NaHCO3 |
|
| 17. 选择题 | 详细信息 |
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(v)与时间(t)关系如右图。反应中镁和铝的 A. 物质的量之比为3:2 B. 质量之比为3:2 C. 摩尔质量之比为2:3 D. 反应速率之比为2:3 |
|
| 18. 实验题 | 详细信息 | ||||||||
(10分)市场销售的某种食用精制盐包装袋上有如下说明:
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处) KIO3+ KI+ H2SO4= K2SO4+ I2+ H2O |
|||||||||
| 19. 推断题 | 详细信息 |
|
下图是中学常见物质间的转化关系。已知: ①A为淡黄色固体,B为导致“温室效应”的主要物质; ②E为常见金属,J为红褐色沉淀; ③G在实验室中常用于检验B的存在;④L是一种重要的工业原料,常用于制造炸药,浓溶液常呈黄色,储存在棕色瓶中。  回答下列问题: (1)A的电子式____________________________________________________。 (2)反应①的化学方程式为__________,反应②的离子方程式为_________________, (3)若参加反应的A的质量为39g,则消耗CO2的体积(标况下)为__________L。 (4)L的化学式__________,G的化学式__________________________。 |
|
| 20. 综合题 | 详细信息 | ||||||||||||
[2012·南通二调](12分)碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下: 已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表: 已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
|
|||||||||||||
| 21. 推断题 | 详细信息 |
|
已知: ①在稀碱溶液中,溴苯难发生水解 ② 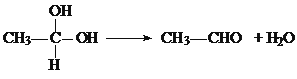 现有分子式为C10H10O2Br2的芳香族化合物X,其苯环上的一溴代物只有一种,其核磁共振氢谱图中有四个吸收峰,吸收峰的面积比为1:2:6:1,在一定条件下可发生下述一系列反应,其中C能发生银镜反应,E遇FeCl3溶液显色且能与浓溴水反应。  请回答下列问题: (1)X中官能的名称是______________。 (2)F→H的反应类型是_________________。 (3)I的结构简式为___________________; (4)E不具有的化学性质________(选填序号) a.取代反应 b.消去反应 c.氧化反应 d.1molE最多能与2molNaHCO3反应 (5)写出下列反应的化学方程式: ①X与足量稀NaOH溶液共热的化学方程式:________________ ; ②F→G的化学方程式:____________________; (6)同时符合下列条件的E的同分异构体共有_____ 种,其中一种的结构简式为________。 a.苯环上核磁共振氢谱有两种 b.不能发生水解反应 c.遇FeCl3溶液不显色 d.1molE最多能分别与1molNaOH和2molNa反应 |
|



