洛阳市2019年高二化学下学期月考测验同步练习
| 1. 选择题 | 详细信息 |
|
把下列四种X溶液分别加入四个盛有10mL 2molL﹣1盐酸的烧杯中,均加水稀释到50mL,此时,X和盐酸缓慢地进行反应,其中反应速率最快的是( ) A. 10℃20mL3 molL﹣1的X溶液 B. 20℃30 mL 2 molL﹣1的X溶液 C. 20℃10 mL 4 molL﹣1的X溶液 D. 10℃10 mL 2 molL﹣1的X溶液 |
|
| 2. 选择题 | 详细信息 |
某温度时,在2 L容器中三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式和反应开始至2 min末Z的平均反应速率分别为( )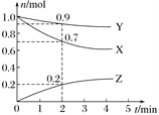 A. X+3Y C. X+2Y |
|
| 3. 选择题 | 详细信息 |
|
反应4A(g)+5B(g) A. A的平均反应速率是0.010 mol•L﹣1•s﹣1 B. 容器中含D物质的量至少为0.45 mol C. 容器中A、B、C、D的物质的量的比一定是4∶5∶4∶6 D. 容器中A的物质的量一定增加了0.30 mol |
|
| 4. 选择题 | 详细信息 |
|
在密闭容器中充入4 mol X,在一定的温度下4X(g) A. 3.4 mol B. 4 mol C. 2.8 mol D. 1.2 mol |
|
| 5. 选择题 | 详细信息 |
|
下列关于碰撞的说法正确的是( ) A. 活化分子之间的碰撞一定能引发化学反应,即活化分子之间的碰撞为有效碰撞 B. 发生有效碰撞的分子必为活化分子 C. 反应物分子之间的碰撞一定会引发化学键的断裂 D. 反应物分子之间只要有合适的取向的碰撞必为有效碰撞 |
|
| 6. 选择题 | 详细信息 |
参照反应Br+H2→HBr+H的能量—反应历程的示意图,下列叙述中正确的是( ) A. 正反应为放热反应 B. 加入催化剂,该化学反应的反应热不变 C. 反应物总能量高于生成物总能量 D. 升高温度可增大正反应速率,降低逆反应速率 |
|
| 7. 选择题 | 详细信息 |
|
对于反应C(s)+H2O(g) A. 增大C(s)的量 B. 增大H2O(g)的浓度 C. 增大CO(g)或H2(g)的浓度 D. 减小H2O(g)的浓度 |
|
| 8. 选择题 | 详细信息 |
|
在恒温恒容条件下,能使A(g)+B(g) A. 减少C或D的物质的量 B. 增大D的物质的量 C. 减少B的物质的量 D. 增大A或B的物质的量 |
|
| 9. 选择题 | 详细信息 |
|
对于反应:N2+O2 A. 缩小体积使压强增大 B. 增大体积使压强减小 C. 体积不变充入He使气体压强增大 D. 保证压强不变条件下充入Ne |
|
| 10. 选择题 | 详细信息 |
|
将等质量的两份锌粉a、b分别加入过量的稀硫酸中,同时向a中加少量CuSO4溶液组成原电池,下列各图中产生H2的体积V(L)与时间t(min)的关系如图所示,其中正确的是( ) A. 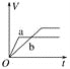 B. B. 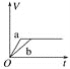 C. 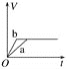 D. D. 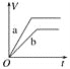 |
|
| 11. 选择题 | 详细信息 |
把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由图表示。在下列因素中对产生H2速率有影响的是 ①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度 A. ①④ B. ③④ C. ①②③ D. ①②③④ |
|
| 12. 选择题 | 详细信息 |
|
在一个定容的密闭容器中进行如下反应:2SO2(g)+O2(g) A. c(SO2)=0.25 mol·L-1 B. c(O2)=0.12 mol·L-1 C. c(SO2)+c(SO3)=0.15 mol·L-1 D. c(SO3)+c(O2)=0.3 mol·L-1 |
|
| 13. 选择题 | 详细信息 |
|
一定条件下,将A、B、C三种物质各1 mol通入一个密闭容器中发生反应: 2A+ B A. 1.5 mol B. 1 mol C. 0.5 mol D. 0 |
|
| 14. 选择题 | 详细信息 |
|
一定温度下,向某容积恒定的密闭容器中充入1 mol N2、3 mol H2,经充分反应后达到如下平衡:N2(g)+3H2(g) A. 达平衡后再加入一定量的N2,体系内各物质含量不变 B. N2、H2、NH3的浓度一定相等 C. 反应没有达到平衡时,NH3会不断地分解,达到平衡时则不会再分解 D. 平衡时,N2、H2物质的量之比为1∶3 |
|
| 15. 选择题 | 详细信息 |
在一定温度下,容器内某一反应中两种气态物质M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( ) A. 反应的化学方程式为:2M B. t2时,正逆反应速率相等,反应达到平衡状态 C. t3时,M上a点正反应速率等于N上b点的逆反应速率 D. t3后的单位时间段内,无论是用M表示还是用N表示,反应速率均为0 |
|
| 16. 选择题 | 详细信息 |
|
下列说法中,可以证明反应N2(g)+3H2(g)2NH3(g)已达到平衡状态的是 A. 1个N≡N键断裂的同时,有3个H—H键形成 B. 1个N≡N键断裂的同时,有3个H—H键断裂 C. 3个H—H键形成的同时,有6个N—H键断裂 D. 1个N≡N键断裂的同时,有6个N—H键形成 |
|
| 17. 选择题 | 详细信息 |
|
在一定温度下的恒容密闭容器中,当下列哪些物理量不再发生变化时,表明下述反应:A(s) + 2B(g) ①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④气体的总物质的量 ⑤混合气体总质量 A. ②③⑤ B. ①②③ C. ②③④ D. ①③④⑤ |
|
| 18. 选择题 | 详细信息 |
|
在一密闭容器中进行反应:X2(g)+Y2(g) A、Z的浓度可能为0.3mol/L B、平衡时X2、Y2的转化率相等 C.平衡时,Y2和Z的生成速率之比为2:1 D、若平衡后再改变外界条件,升高温度,则反应的平衡常数将变大 |
|
| 19. 选择题 | 详细信息 |
|
在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g) A.加催化剂同时升高温度 B.加催化剂同时增大压强 C.升高温度同时充入N2 D.降低温度同时增大压强 |
|
| 20. 选择题 | 详细信息 |
|
下列措施或事实能用勒夏特列原理解释的是( ) A. 在合成氨(正反应是放热)的反应中,升温有利于氨的合成 B. H2、I2、HI三者的平衡混合气加压后颜色变深 C. 钢铁在潮湿的空气中更容易生锈 D. 含有酚酞的氨水中加入少量的氯化铵溶液的颜色变浅 |
|
| 21. 选择题 | 详细信息 |
|
高温下,某反应达到平衡,平衡常数K= A. 该反应是焓变为正值 B. 恒温恒容下,增大压强,H2浓度一定减小 C. 升高温度,逆反应速率减小 D. 该反应化学方程式为CO+H2O |
|
| 22. 选择题 | 详细信息 |
|
可逆反应A+B(s) A、A为固体,C为气体,正反应为放热反应 B、A为气体,C为固体,正反应为吸热反应 C、A为气体,C为固体,正反应为放热反应 D、A、C均为气体,正反应为吸热反应 |
|
| 23. 选择题 | 详细信息 |
|
纯水在25 ℃和80 ℃时,c(H+)前后大小关系及酸碱性分别是( ) A. 大于 弱酸性 B. 等于 都显中性 C. 小于 弱酸性 D. 小于 都显中性 |
|
| 24. 选择题 | 详细信息 |
|
已知25 ℃时水的离子积为Kw=1.0×10-14,35 ℃时水的离子积为Kw=2.1×10-14。下列说法中正确的是 ( ) A. 水中的c(H+)随温度的升高而降低 B. 25 ℃时水呈中性,35 ℃时水呈酸性 C. 水的电离过程是吸热过程 D. 一定温度下,向水中加入酸或碱时,水的离子积将发生变化 |
|
| 25. 选择题 | 详细信息 |
|
用标准浓度的NaOH溶液滴定未知浓度的盐酸时下列情况会使盐酸物质的量浓度偏低的是( ) A. 碱式滴定管用蒸馏水洗净后,直接注入标准浓度的NaOH溶液 B. 碱式滴定管尖端有气泡,滴定后气泡消失 C. 记录消耗的碱液,滴定前平视,滴定后俯视凹液面 D. 锥形瓶用蒸馏水洗净后,直接装入未知浓度的盐酸 |
|
| 26. 填空题 | 详细信息 |
某温度时,在2L容器中,某一反应中A、B的物质的量随时间变化的曲线如图所示,由图中数据分析得: (1)从反应开始至4 min时,A的平均反应速率为___。 (2)该反应的化学方程式为___。 |
|
| 27. 填空题 | 详细信息 |
|
现有反应:mA(g)+nB(g) (1)该反应的逆反应为__(填“吸热”或“放热”)反应,且m+n_(填“>”“=”或“<”)p。 (2)减压使容器体积增大时,A的质量分数__。(填“增大”“减小”或“不变”,下同) (3)若升高温度,则平衡时B、C的浓度之比 (4)若加入催化剂,平衡时气体混合物的总物质的量____。 |
|
| 28. 填空题 | 详细信息 |
煤化工中常需研究不同温度下平衡常数、投料比及产率等问题。已知:CO(g)+H2O(g)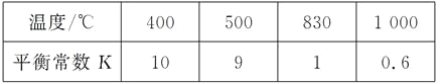 某温度下,平衡浓度符合下式:c(CO2)·c(H2)===c(CO)·c(H2O),试判断此时的温度为__℃。该反应正方向为__(填“放热反应”、“吸热反应”) |
|
| 29. 填空题 | 详细信息 |
|
在容积为2 L的密闭容器中进行如下反应:A(g)+2B(g) (1)5 min末B的物质的量浓度为________。 (2)前5 min内化学反应速率v(A)为_______。 (3)化学方程式中n值为________。 (4)该反应在此温度下的平衡常数K=______(填数值)。 |
|
| 30. 填空题 | 详细信息 |
|
25℃时,50mL0.10 mol·L-1醋酸中存在电离平衡:CH3COOH (1)加入少量醋酸钠,上述平衡向___移动(填“左”、“右”、“不”,下同)。 (2)加入少量0.1 mol·L-1盐酸,上述平衡向___移动,c(H+)___(填“增大”、“减小”、“不变”,下同)。 (3)加入碳酸钠固体,上述平衡向___移动,c(H+)___。 |
|
| 31. 填空题 | 详细信息 |
已知某温度下CH3COOH的电离常数K=1.6×10-5,该温度下向20 mL 0.01 mol·L-1CH3COOH溶液中逐滴加入0.01 mol·L-1KOH溶液,其pH变化曲线如图所示(忽略温度变化),请回答有关问题: (1)a点溶液中c(H+)为____mol·L-1。 (2)b点溶液中溶质__,CH3COOH的电离常数___1.6×10-5(“>”、“<”或“=”)。 |
|
| 32. 填空题 | 详细信息 |
|
(1)某温度(T℃)时,水的Kw=1×10-12,则该温度___(填“>”、“<”或“=”)25℃,其理由是___。 (2)该温度下,c(H+)=1×10-7mol·L-1的溶液呈___(填“酸性”、“碱性”或“中性”);若该溶液中只存在NaOH溶质,则由H2O电离出来的c(OH-)=____mol·L-1。 |
|
最近更新



