еұұдёң2020е№ҙй«ҳдёүеҢ–еӯҰдёҠеҚҠе№ҙйҷ„зӯ”жЎҲдёҺи§Јжһҗ
| 1. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
еҢ–еӯҰдёҺз”ҹжҙ»гҖҒзӨҫдјҡеҸ‘еұ•жҒҜжҒҜзӣёе…іпјҢдёӢеҲ—жңүе…іиҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜ A.вҖңж—¶ж°”й”ҷйҖҶпјҢйңҫйӣҫи”Ҫж—ҘвҖқпјҢйӣҫжүҖеҪўжҲҗзҡ„ж°”жә¶иғ¶иғҪдә§з”ҹдёҒиҫҫе°”ж•Ҳеә” B.вҖңйқ’и’ҝдёҖжҸЎпјҢд»Ҙж°ҙдәҢеҚҮжёҚпјҢз»һеҸ–жұҒвҖқпјӣеұ е‘Ұе‘Ұж”№иҝӣжҸҗеҸ–йқ’и’ҝзҙ зҡ„ж–№жі•пјҢжҸҗеҸ–иҝҮзЁӢдёӯеҸ‘з”ҹдәҶеҢ–еӯҰеҸҳеҢ– C.еҲҳзҰ№й”Ўзҡ„вҖңеҚғж·ҳдёҮжјүиҷҪиҫӣиӢҰпјҢеҗ№е°ҪзӢӮжІҷе§ӢеҲ°йҮ‘вҖқеҸҜд»ҘзңӢеҮәйҮ‘жҖ§иҙЁзЁіе®ҡпјҢеҸҜйҖҡиҝҮзү©зҗҶж–№жі•еҫ—еҲ° D.вҖңеӨ–и§ӮеҰӮйӣӘпјҢејәзғ§д№ӢпјҢзҙ«йқ’зғҹиө·вҖқгҖӮеҜ№зЎқй…ёй’ҫзҡ„йүҙе®ҡиҝҮзЁӢдёӯеҲ©з”ЁдәҶз„°иүІеҸҚеә” |
|
| 2. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
жҹҘйҳ…иө„ж–ҷеҸҜзҹҘпјҢиӢҜеҸҜиў«иҮӯж°§ж°§еҢ–пјҢеҸ‘з”ҹеҢ–еӯҰеҸҚеә”дёәпјҡ A.5з§Қ B.4з§Қ C.3з§Қ D.2з§Қ |
|
| 3. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҗ„з»„дёӯзҡ„Xе’ҢYдёӨз§ҚеҺҹеӯҗпјҢеҢ–еӯҰжҖ§иҙЁдёҖе®ҡзӣёдјјзҡ„жҳҜ (гҖҖгҖҖ) A. XеҺҹеӯҗе’ҢYеҺҹеӯҗжңҖеӨ–еұӮйғҪеҸӘжңү1дёӘз”өеӯҗ B. XеҺҹеӯҗзҡ„ж ёеӨ–з”өеӯҗжҺ’еёғејҸдёә1s2пјҢYеҺҹеӯҗзҡ„ж ёеӨ–з”өеӯҗжҺ’еёғејҸдёә1s22s2 C. XеҺҹеӯҗзҡ„2pиғҪзә§дёҠжңү3дёӘз”өеӯҗпјҢYеҺҹеӯҗзҡ„3pиғҪзә§дёҠжңү3дёӘз”өеӯҗ D. XеҺҹеӯҗж ёеӨ–MеұӮдёҠд»…жңү2дёӘз”өеӯҗпјҢYеҺҹеӯҗж ёеӨ–NеұӮдёҠд»…жңү2дёӘз”өеӯҗ |
|
| 4. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
е…ідәҺдёӢеҲ—еҗ„е®һйӘҢиЈ…зҪ®зҡ„еҸҷиҝ°дёӯпјҢдёҚжӯЈзЎ®зҡ„жҳҜпјҲ пјү A. 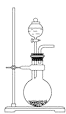 еҸҜз”ЁдәҺе®һйӘҢе®ӨеҲ¶еҸ–е°‘йҮҸNH3жҲ–O2 еҸҜз”ЁдәҺе®һйӘҢе®ӨеҲ¶еҸ–е°‘йҮҸNH3жҲ–O2B.  еҸҜз”Ёд»ҺaеӨ„еҠ ж°ҙзҡ„ж–№жі•жЈҖйӘҢиЈ…зҪ®в‘Ўзҡ„ж°”еҜҶжҖ§ еҸҜз”Ёд»ҺaеӨ„еҠ ж°ҙзҡ„ж–№жі•жЈҖйӘҢиЈ…зҪ®в‘Ўзҡ„ж°”еҜҶжҖ§C.  е®һйӘҢе®ӨеҸҜз”ЁиЈ…зҪ®в‘ўж”¶йӣҶH2гҖҒNH3 е®һйӘҢе®ӨеҸҜз”ЁиЈ…зҪ®в‘ўж”¶йӣҶH2гҖҒNH3D. 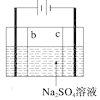 еҲ¶зЎ«й…ёе’Ңж°ўж°§еҢ–й’ пјҢе…¶дёӯbдёәйҳізҰ»еӯҗдәӨжҚўиҶңгҖҒcдёәйҳҙзҰ»еӯҗдәӨжҚўиҶң еҲ¶зЎ«й…ёе’Ңж°ўж°§еҢ–й’ пјҢе…¶дёӯbдёәйҳізҰ»еӯҗдәӨжҚўиҶңгҖҒcдёәйҳҙзҰ»еӯҗдәӨжҚўиҶң |
|
| 5. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
дәәдҪ“е°ҝж¶ІдёӯеҸҜд»ҘеҲҶзҰ»еҮәе…·жңүз”ҹй•ҝзҙ ж•Ҳеә”зҡ„еҢ–еӯҰзү©иҙЁвҖ”вҖ”еҗІе“ҡд№ҷй…ёпјҢеҗІе“ҡд№ҷй…ёзҡ„з»“жһ„з®ҖејҸеҰӮеӣҫжүҖзӨәгҖӮдёӢеҲ—жңүе…іиҜҙжі•жӯЈзЎ®зҡ„жҳҜ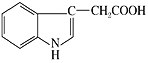 A.еҲҶеӯҗдёӯеҗ«жңү2з§Қе®ҳиғҪеӣў B.еҗІе“ҡд№ҷй…ёиӢҜзҺҜдёҠзҡ„дәҢж°Ҝд»Јзү©е…ұжңүеӣӣз§Қ C.1 molеҗІе“ҡд№ҷй…ёдёҺи¶ійҮҸж°ўж°”еҸ‘з”ҹеҸҚеә”пјҢжңҖеӨҡж¶ҲиҖ—5 mol H2 D.еҲҶеӯҗдёӯдёҚеҗ«жүӢжҖ§зўіеҺҹеӯҗ |
|
| 6. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
зҹӯе‘Ёжңҹдё»ж—Ҹе…ғзҙ aгҖҒbгҖҒcгҖҒdгҖҒeзҡ„еҺҹеӯҗеәҸж•°дҫқж¬ЎеўһеӨ§пјҢAгҖҒBгҖҒCгҖҒDгҖҒEгҖҒFеқҮжҳҜз”ұдёҠиҝ°е…ғзҙ з»„жҲҗзҡ„дёӯеӯҰеҢ–еӯҰеёёи§Ғзү©иҙЁпјҢе…¶дёӯAжҳҜеӣӣе…ғеҢ–еҗҲзү©пјҢCжҳҜиғҪдҪҝж№ҝж¶ҰзәўиүІзҹіи•ҠиҜ•зәёеҸҳи“қзҡ„ж°”дҪ“пјҢDжҳҜж·Ўй»„иүІеӣәдҪ“еҢ–еҗҲзү©пјҢEжҳҜеҚ•иҙЁгҖӮеҗ„зү©иҙЁд№Ӣй—ҙеӯҳеңЁеҰӮеӣҫиҪ¬еҢ–е…ізі»(йғЁеҲҶдә§зү©жңӘж ҮеҮә)гҖӮдёӢеҲ—иҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜ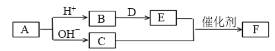 A.з®ҖеҚ•зҰ»еӯҗеҚҠеҫ„еӨ§е°Ҹе…ізі»пјҡcпјһdпјһe B.з®ҖеҚ•йҳҙзҰ»еӯҗзҡ„иҝҳеҺҹжҖ§пјҡaпјһcпјһd C.ж°ўеҢ–зү©зҡ„жІёзӮ№пјҡcпјһd D.Cе’ҢEеҸҚеә”з”ҹжҲҗFжҳҜе·ҘдёҡеҲ¶зЎқй…ёзҡ„йҮҚиҰҒеҸҚеә”д№ӢдёҖ |
|
| 7. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
жңҖиҝ‘科еӯҰ家еҸ‘зҺ°йғҪз”ұзЈ·еҺҹеӯҗжһ„жҲҗзҡ„й»‘зЈ·(й»‘зЈ·зҡ„зЈ·еҺҹеӯҗдәҢз»ҙз»“жһ„еҰӮеӣҫ)жҳҜжҜ”зҹіеўЁзғҜжӣҙеҘҪзҡ„ж–°еһӢдәҢз»ҙеҚҠеҜјдҪ“жқҗж–ҷ.дёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜ A.зҹіеўЁзғҜеұһдәҺзғҜзғғ B.зҹіеўЁзғҜдёӯзўіеҺҹеӯҗйҮҮз”Ёsp3жқӮеҢ– C.й»‘зЈ·дёҺзҷҪзЈ·дә’дёәеҗҢзҙ ејӮеҪўдҪ“ D.й»‘зЈ·й«ҳжё©дёӢеңЁз©әж°”дёӯеҸҜд»ҘзЁіе®ҡеӯҳеңЁ |
|
| 8. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
SBPз”өи§Јжі•иғҪеӨ§е№…еәҰжҸҗй«ҳз”өи§Јж§Ҫзҡ„з”ҹдә§иғҪеҠӣпјҢеҰӮеӣҫдёәSBPз”өи§Јжі•еҲ¶еӨҮMoO3зҡ„зӨәж„ҸеӣҫпјҢдёӢеҲ—иҜҙжі•й”ҷиҜҜзҡ„жҳҜ(гҖҖгҖҖ) A.aжһҒдёәз”өжәҗзҡ„иҙҹжһҒпјҢеҸ‘з”ҹж°§еҢ–еҸҚеә” B.з”өи·ҜдёӯиҪ¬з§»4molз”өеӯҗпјҢеҲҷзҹіеўЁз”өжһҒдёҠдә§з”ҹж ҮеҮҶзҠ¶еҶөдёӢ22.4LO2 C.й’ӣеҹәй’ӣй”°еҗҲйҮ‘з”өжһҒеҸ‘з”ҹзҡ„з”өжһҒеҸҚеә”дёәпјҡ3H2O+Mo4+-2e-=MoO3+6H+ D.з”өи·Ҝдёӯз”өеӯҗжөҒеҗ‘дёәпјҡaжһҒ |
|
| 9. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||||||||
дёӢеҲ—жңүе…іе®һйӘҢж“ҚдҪңгҖҒзҺ°иұЎгҖҒи§ЈйҮҠе’Ңз»“и®әйғҪжӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ)
|
|||||||||||||||||||||
| 10. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
жҹҗйҮ‘еұһжңүжңәеӨҡеӯ”жқҗж–ҷFJI-H14еңЁеёёжё©еёёеҺӢдёӢеҜ№CO2е…·жңүи¶…й«ҳзҡ„еҗёйҷ„иғҪеҠӣпјҢ并иғҪй«ҳж•ҲеӮ¬еҢ–CO2дёҺзҺҜж°§д№ҷзғ·иЎҚз”ҹзү©зҡ„еҸҚеә”пјҢе…¶е·ҘдҪңеҺҹзҗҶеҰӮеӣҫжүҖзӨәгҖӮдёӢеҲ—иҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜпјҲ пјү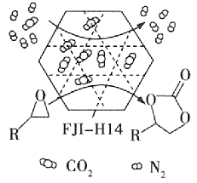 A.иҜҘжқҗж–ҷзҡ„еҗёйҷ„дҪңз”Ёе…·жңүйҖүжӢ©жҖ§ B.иҜҘж–№жі•зҡ„е№ҝжіӣдҪҝз”ЁжңүеҠ©дәҺеҮҸе°‘CO2жҺ’ж”ҫ C.еңЁз”ҹжҲҗ  зҡ„иҝҮзЁӢдёӯпјҢжңүжһҒжҖ§е…ұд»·й”®еҪўжҲҗ зҡ„иҝҮзЁӢдёӯпјҢжңүжһҒжҖ§е…ұд»·й”®еҪўжҲҗD.е…¶е·ҘдҪңеҺҹзҗҶеҸӘж¶үеҸҠеҢ–еӯҰеҸҳеҢ– |
|
| 11. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
йҮ‘еұһ(M)пјҚз©әж°”з”өжұ (еҰӮеӣҫ)е…·жңүеҺҹж–ҷжҳ“еҫ—гҖҒиғҪйҮҸеҜҶеәҰй«ҳзӯүдјҳзӮ№пјҢжңүжңӣжҲҗдёәж–°иғҪжәҗжұҪиҪҰе’Ң移еҠЁи®ҫеӨҮзҡ„з”өжәҗгҖӮиҜҘзұ»з”өжұ ж”ҫз”өзҡ„жҖ»еҸҚеә”дёәпјҡ4M + nO2 + 2nH2O = 4M(OH)nгҖӮе·ІзҹҘпјҡз”өжұ зҡ„вҖңзҗҶи®әжҜ”иғҪйҮҸвҖқжҢҮеҚ•дҪҚиҙЁйҮҸзҡ„з”өжһҒжқҗж–ҷзҗҶи®әдёҠиғҪйҮҠж”ҫеҮәзҡ„жңҖеӨ§з”өиғҪгҖӮдёӢеҲ—иҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜ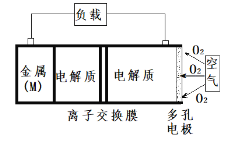 A.еӨҡеӯ”з”өжһҒжңүеҲ©дәҺж°§ж°”жү©ж•ЈиҮіз”өжһҒиЎЁйқўпјҢеҸҜжҸҗй«ҳеҸҚеә”йҖҹзҺҮ B.з”өжұ ж”ҫз”өиҝҮзЁӢзҡ„жӯЈжһҒеҸҚеә”ејҸпјҡ O2 + 2H2O + 4eпјҚ = 4OHпјҚ C.жҜ”иҫғMgгҖҒAlдәҢз§ҚйҮ‘еұһпјҚз©әж°”з”өжұ пјҢвҖңзҗҶи®әжҜ”иғҪйҮҸвҖқд№ӢжҜ”жҳҜ8вҲ¶9 D.дёәйҳІжӯўиҙҹжһҒеҢәжІүз§ҜMg(OH)2пјҢе®ңйҮҮз”ЁдёӯжҖ§з”өи§ЈиҙЁеҸҠйҳізҰ»еӯҗдәӨжҚўиҶң |
|
| 12. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ | ||||||||
й“Ӣ(Bi)дҪҚдәҺе…ғзҙ е‘ЁжңҹиЎЁдёӯ第VAж—ҸпјҢе…¶д»·жҖҒдёә+3ж—¶иҫғзЁіе®ҡпјҢй“Ӣй…ёй’ (NaBiO3)жә¶ж¶Іе‘Ҳж— иүІгҖӮзҺ°еҸ–дёҖе®ҡйҮҸзҡ„зЎ«й…ёй”°MnSO4жә¶ж¶ІпјҢеҗ‘е…¶дёӯдҫқж¬Ўж»ҙеҠ дёӢеҲ—жә¶ж¶ІпјҢеҜ№еә”зҺ°иұЎеҰӮиЎЁжүҖзӨәпјҡ
|
|||||||||
| 13. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
е®Өжё©дёӢпјҢе°Ҷ0.1000molВ·LпјҚ1зӣҗй…ёж»ҙе…Ҙ20.00 mLжңӘзҹҘжө“еәҰзҡ„жҹҗдёҖе…ғзўұMOHжә¶ж¶ІдёӯпјҢжә¶ж¶ІpHйҡҸеҠ е…Ҙзӣҗй…ёдҪ“з§ҜеҸҳеҢ–жӣІзәҝеҰӮеӣҫжүҖзӨәгҖӮдёӢеҲ—жңүе…іиҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜ A.иҜҘдёҖе…ғзўұжә¶ж¶Іжө“еәҰдёә0.1000molВ·LпјҚ1 B.aзӮ№пјҡc(MпјӢ)>c(ClпјҚ)>c(OH-)>c(H+) C.bзӮ№пјҡc(MпјӢ)пјӢc(MOH)пјқc(ClпјҚ) D.е®Өжё©дёӢпјҢMOHзҡ„з”өзҰ»еёёж•°Kbпјқ1Г—10пјҚ5 |
|
| 14. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
жҹҗй»„иүІжә¶ж¶ІдёӯеҸҜиғҪеҗ«жңүNa+гҖҒNH4+гҖҒFe2+гҖҒFe3+гҖҒClп№ЈгҖҒSO42п№ЈгҖҒCO32п№ЈзӯүзҰ»еӯҗ(дёҚиҖғиҷ‘ж°ҙзҡ„з”өзҰ»е’ҢзҰ»еӯҗзҡ„ж°ҙи§Ј)гҖӮжҹҗеҗҢеӯҰдёәдәҶзЎ®е®ҡе…¶з»„еҲҶпјҢи®ҫ计并е®ҢжҲҗдәҶеҰӮдёӢе®һйӘҢпјҡ дёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜ( ) A.c(Fe3+)дёҖе®ҡдёә0.2molвҖўLп№Ј1 B.Clп№ЈдёҖе®ҡеӯҳеңЁ C.Na+гҖҒSO42п№ЈдёҖе®ҡеӯҳеңЁпјҢNH4+дёҖе®ҡдёҚеӯҳеңЁ D.Na+гҖҒFe2+еҸҜиғҪеӯҳеңЁпјҢCO32п№ЈдёҖе®ҡдёҚеӯҳеңЁ |
|
| 15. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
PbCl2жҳҜдёҖз§ҚйҮҚиҰҒзҡ„еҢ–е·Ҙжқҗж–ҷпјҢеёёз”ЁдҪңеҠ©жә¶еүӮгҖҒеҲ¶еӨҮй“…й»„зӯүжҹ“ж–ҷгҖӮе·Ҙдёҡз”ҹдә§дёӯеҲ©з”Ёж–№й“…зҹҝзІҫзҹҝ(дё»иҰҒжҲҗеҲҶдёәPbSпјҢеҗ«жңүFeS2зӯүжқӮиҙЁ)е’ҢиҪҜй”°зҹҝ(дё»иҰҒжҲҗеҲҶдёәMnO2)еҲ¶еӨҮPbCl2зҡ„е·ҘиүәжөҒзЁӢеҰӮеӣҫжүҖзӨәгҖӮ е·ІзҹҘпјҡi.PbCl2еҫ®жә¶дәҺж°ҙ ii.PbCl2(s) + 2ClпјҚ(aq)вҮҢPbCl42-(aq) О”H>0 дёӢеҲ—иҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜ( ) A.жөёеҸ–иҝҮзЁӢдёӯMnO2дёҺPbSеҸ‘з”ҹеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸдёәпјҡ8H++2ClпјҚ+PbS + 4MnO2=PbCl2 +4Mn2++SO42-+4H2O B.PbCl2еҫ®жә¶дәҺж°ҙпјҢжөёеҸ–еүӮдёӯеҠ е…ҘйҘұе’ҢNaClжә¶ж¶ІдјҡеўһеӨ§е…¶жә¶и§ЈжҖ§ C.и°ғpHзҡ„зӣ®зҡ„жҳҜйҷӨеҺ»Fe3+пјҢеӣ жӯӨpHи¶ҠеӨ§и¶ҠеҘҪ D.жІүйҷҚжұ дёӯиҺ·еҫ—PbCl2йҮҮеҸ–зҡ„жҺӘж–ҪжңүеҠ ж°ҙзЁҖйҮҠгҖҒйҷҚжё© |
|
| 16. з»јеҗҲйўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
иө„жәҗеҢ–еҲ©з”ЁCO2пјҢеҸҜд»ҘеҮҸе°‘жё©е®Өж°”дҪ“жҺ’ж”ҫпјҢиҝҳеҸҜд»ҘиҺ·еҫ—зҮғж–ҷжҲ–йҮҚиҰҒзҡ„еҢ–е·Ҙдә§е“ҒгҖӮеӣһзӯ”дёӢеҲ—й—®йўҳпјҡ (1)CO2зҡ„жҚ•йӣҶ в‘ з”ЁйҘұе’ҢNa2CO3жә¶ж¶ІеҒҡеҗёж”¶еүӮеҸҜвҖңжҚ•йӣҶвҖқCO2гҖӮеҶҷеҮәвҖңжҚ•йӣҶвҖқCO2еҸҚеә”зҡ„зҰ»еӯҗж–№ејҸ_____________гҖӮ в‘ЎиҒҡеҗҲзҰ»еӯҗж¶ІдҪ“жҳҜзӣ®еүҚе№ҝжіӣз ”з©¶зҡ„CO2еҗёйҷ„еүӮгҖӮз»“еҗҲеӣҫеғҸеҲҶжһҗиҒҡеҗҲзҰ»еӯҗж¶ІдҪ“еҗёйҷ„CO2зҡ„жңүеҲ©жқЎд»¶жҳҜ_________________________гҖӮ 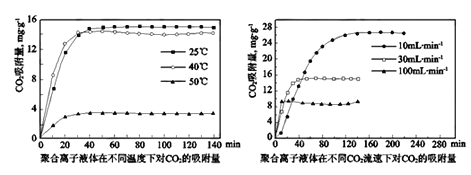 (2)з”ҹдә§е°ҝзҙ пјҡ е·ҘдёҡдёҠд»ҘCO2гҖҒNH3дёәеҺҹж–ҷз”ҹдә§е°ҝзҙ [CO(NH2)2]пјҢиҜҘеҸҚеә”еҲҶдёәдәҢжӯҘиҝӣиЎҢпјҡ 第дёҖжӯҘпјҡ2NH3(g)+CO2(g)вҮҢH2NCOONH4(s) в–іH = - 159.5 kJВ·mol-1 第дәҢжӯҘпјҡH2NCOONH4(s)вҮҢCO(NH2)2(s)+ H2O(g) в–іH = +116.5 kJВ·mol-1 в‘ еҶҷеҮәдёҠиҝ°еҗҲжҲҗе°ҝзҙ зҡ„зғӯеҢ–еӯҰж–№зЁӢејҸ___________________________гҖӮиҜҘеҸҚеә”еҢ–еӯҰе№іиЎЎеёёж•°Kзҡ„иЎЁиҫҫејҸпјҡ_________________________гҖӮ в‘Ўжҹҗе®һйӘҢе°Ҹз»„жЁЎжӢҹе·ҘдёҡдёҠеҗҲжҲҗе°ҝзҙ пјҢеңЁдёҖе®ҡдҪ“з§Ҝзҡ„еҜҶй—ӯе®№еҷЁдёӯжҠ•е…Ҙ4mol NH3е’Ң1mol CO2пјҢе®һйӘҢжөӢеҫ—еҸҚеә”дёӯеҗ„з»„еҲҶзү©иҙЁзҡ„йҮҸйҡҸж—¶й—ҙзҡ„еҸҳеҢ–еҰӮеӣҫжүҖзӨәпјҡ  е·ІзҹҘжҖ»еҸҚеә”зҡ„еҝ«ж…ўз”ұж…ўзҡ„дёҖжӯҘеҸҚеә”еҶіе®ҡпјҢеҲҷеҗҲжҲҗе°ҝзҙ жҖ»еҸҚеә”зҡ„еҝ«ж…ўз”ұ第__________жӯҘеҸҚеә”еҶіе®ҡпјҢжҖ»еҸҚеә”иҝӣиЎҢеҲ°___________minж—¶еҲ°иҫҫе№іиЎЎ (3)еҗҲжҲҗд№ҷй…ёпјҡдёӯеӣҪ科еӯҰ家йҰ–ж¬Ўд»ҘCH3OHгҖҒCO2е’ҢH2дёәеҺҹж–ҷй«ҳж•ҲеҗҲжҲҗд№ҷй…ёпјҢе…¶еҸҚеә”и·Ҝеҫ„еҰӮеӣҫжүҖзӨәпјҡ  в‘ еҺҹж–ҷдёӯзҡ„CH3OHеҸҜйҖҡиҝҮз”өи§Јжі•з”ұCO2еҲ¶еҸ–пјҢз”ЁзЁҖзЎ«й…ёдҪңз”өи§ЈиҙЁжә¶ж¶ІпјҢеҶҷеҮәз”ҹжҲҗCH3OHзҡ„з”өжһҒеҸҚеә”ејҸ_______________________гҖӮ в‘Ўж №жҚ®еӣҫзӨәпјҢеҶҷеҮәжҖ»еҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢ___________гҖӮ |
|
| 17. з»јеҗҲйўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
жңүAгҖҒBгҖҒCгҖҒDеӣӣз§Қе…ғзҙ пјҢе…¶дёӯAе…ғзҙ е’ҢBе…ғзҙ зҡ„еҺҹеӯҗйғҪжңү1дёӘжңӘжҲҗеҜ№з”өеӯҗпјҢAпјӢжҜ”BпјҚе°‘дёҖдёӘз”өеӯҗеұӮпјҢBеҺҹеӯҗеҫ—дёҖдёӘз”өеӯҗеЎ«е…Ҙ3pиҪЁйҒ“еҗҺпјҢ3pиҪЁйҒ“е·Іе……ж»ЎпјӣCеҺҹеӯҗзҡ„pиҪЁйҒ“дёӯжңү3дёӘжңӘжҲҗеҜ№з”өеӯҗпјҢе…¶ж°”жҖҒж°ўеҢ–зү©еңЁж°ҙдёӯзҡ„жә¶и§ЈеәҰеңЁеҗҢж—Ҹе…ғзҙ жүҖеҪўжҲҗзҡ„ж°ўеҢ–зү©дёӯжңҖеӨ§пјӣDзҡ„жңҖй«ҳеҢ–еҗҲд»·е’ҢжңҖдҪҺеҢ–еҗҲд»·зҡ„д»Јж•°е’Ңдёә4пјҢе…¶жңҖй«ҳд»·ж°§еҢ–зү©дёӯеҗ«Dзҡ„иҙЁйҮҸеҲҶж•°дёә 40пј…пјҢдё”е…¶ж ёеҶ…иҙЁеӯҗж•°зӯүдәҺдёӯеӯҗж•°гҖӮRжҳҜз”ұAгҖҒDдёӨе…ғзҙ еҪўжҲҗзҡ„зҰ»еӯҗеҢ–еҗҲзү©пјҢе…¶дёӯAпјӢдёҺD2пјҚзҰ»еӯҗж•°д№ӢжҜ”дёә2вҲ¶1гҖӮеӣһзӯ”дёӢеҲ—й—®йўҳпјҡ (1)Aе…ғзҙ еҪўжҲҗзҡ„жҷ¶дҪ“еұһдәҺA2еҜҶе Ҷз§ҜеһӢејҸпјҢеҲҷе…¶жҷ¶дҪ“еҶ…жҷ¶иғһзұ»еһӢеә”еұһдәҺ______(еЎ«еҶҷвҖңе…ӯж–№вҖқгҖҒвҖңйқўеҝғз«Ӣж–№вҖқжҲ–вҖңдҪ“еҝғз«Ӣж–№вҖқ)гҖӮ (2)BпјҚзҡ„з”өеӯҗжҺ’еёғејҸдёә____________пјҢеңЁCB3еҲҶеӯҗдёӯCе…ғзҙ еҺҹеӯҗзҡ„еҺҹеӯҗиҪЁйҒ“еҸ‘з”ҹзҡ„жҳҜ___________жқӮеҢ–гҖӮ (3)Cзҡ„ж°ўеҢ–зү©зҡ„з©әй—ҙжһ„еһӢдёә____________________пјҢе…¶ж°ўеҢ–зү©еңЁеҗҢж—Ҹе…ғзҙ жүҖеҪўжҲҗзҡ„ж°ўеҢ–зү©дёӯжІёзӮ№жңҖй«ҳзҡ„еҺҹеӣ жҳҜ________________________гҖӮ (4)Bе…ғзҙ зҡ„з”өиҙҹжҖ§_______Dе…ғзҙ зҡ„з”өиҙҹжҖ§(еЎ«вҖңпјһвҖқгҖҒвҖңпјңвҖқжҲ–вҖңпјқвҖқ)пјӣз”ЁдёҖдёӘеҢ–еӯҰж–№зЁӢејҸиҜҙжҳҺ___________гҖӮ (5)еҰӮеӣҫжүҖзӨәжҳҜRеҪўжҲҗзҡ„жҷ¶дҪ“зҡ„жҷ¶иғһпјҢи®ҫжҷ¶иғһзҡ„жЈұй•ҝдёәa cmгҖӮиҜ•и®Ўз®—Rжҷ¶дҪ“зҡ„еҜҶеәҰдёә_______гҖӮ(йҳҝдјҸеҠ еҫ·зҪ—еёёж•°з”ЁNAиЎЁзӨә)  |
|
| 18. е®һйӘҢйўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
зЎ«й…ёеӣӣж°ЁеҗҲй“ңжҷ¶дҪ“([Cu(NH3)4]SO4В·H2O)еёёз”ЁдҪңжқҖиҷ«еүӮпјҢеӘ’жҹ“еүӮпјҢеңЁзўұжҖ§й•Җй“ңдёӯд№ҹеёёз”ЁдҪңз”өй•Җж¶Ізҡ„дё»иҰҒжҲҗеҲҶпјҢеңЁе·ҘдёҡдёҠз”ЁйҖ”е№ҝжіӣгҖӮеёёжё©дёӢиҜҘзү©иҙЁжә¶дәҺж°ҙпјҢдёҚжә¶дәҺд№ҷйҶҮгҖҒд№ҷйҶҡпјҢеңЁз©әж°”дёӯдёҚзЁіе®ҡпјҢеҸ—зғӯж—¶жҳ“еҸ‘з”ҹеҲҶи§ЈгҖӮжҹҗеҢ–еӯҰе…ҙи¶Је°Ҹз»„д»ҘCuзІүгҖҒ3mol/Lзҡ„зЎ«й…ёгҖҒжө“ж°Ёж°ҙгҖҒ10% NaOHжә¶ж¶ІгҖҒ95%зҡ„д№ҷйҶҮжә¶ж¶ІгҖҒ0.500 mol/LзЁҖзӣҗй…ёгҖҒ0.500 mol/Lзҡ„NaOHжә¶ж¶ІжқҘеҗҲжҲҗзЎ«й…ёеӣӣж°ЁеҗҲй“ңжҷ¶дҪ“并жөӢе®ҡе…¶зәҜеәҰгҖӮ I.CuSO4жә¶ж¶Ізҡ„еҲ¶еӨҮ в‘ з§°еҸ–4gй“ңзІүпјҢеңЁAд»ӘеҷЁдёӯзҒјзғ§10еҲҶй’ҹ并дёҚж–ӯжҗ…жӢҢпјҢж”ҫзҪ®еҶ·еҚҙгҖӮ в‘ЎеңЁи’ёеҸ‘зҡҝдёӯеҠ е…Ҙ30mL 3mol/Lзҡ„зЎ«й…ёпјҢе°ҶAдёӯеӣәдҪ“ж…ўж…ўж”ҫе…Ҙе…¶дёӯпјҢеҠ зғӯ并дёҚж–ӯжҗ…жӢҢгҖӮ в‘ўи¶ҒзғӯиҝҮж»Өеҫ—и“қиүІжә¶ж¶ІгҖӮ (1)Aд»ӘеҷЁзҡ„еҗҚз§°дёә_____________гҖӮ (2)жҹҗеҗҢеӯҰеңЁе®һйӘҢдёӯжңү1.5gзҡ„й“ңзІүеү©дҪҷпјҢиҜҘеҗҢеӯҰе°ҶеҲ¶еҫ—зҡ„CuSO4жә¶ж¶ІеҖ’е…ҘеҸҰдёҖи’ёеҸ‘зҡҝдёӯеҠ зғӯжө“зј©иҮіжңүжҷ¶иҶңеҮәзҺ°пјҢеҶ·еҚҙжһҗеҮәзҡ„жҷ¶дҪ“дёӯеҗ«жңүзҷҪиүІзІүжң«пјҢиҜ•и§ЈйҮҠе…¶еҺҹеӣ _____гҖӮ II.жҷ¶дҪ“зҡ„еҲ¶еӨҮгҖӮе°ҶдёҠиҝ°еҲ¶еӨҮзҡ„CuSO4жә¶ж¶ІжҢүеҰӮеӣҫжүҖзӨәиҝӣиЎҢж“ҚдҪң  (3)е·ІзҹҘжө…и“қиүІжІүж·Җзҡ„жҲҗеҲҶдёәCu2(OH)2SO4пјҢиҜ•еҶҷеҮәз”ҹжҲҗжӯӨжІүж·Җзҡ„зҰ»еӯҗеҸҚеә”ж–№зЁӢејҸ___________гҖӮ (4)жһҗеҮәжҷ¶дҪ“ж—¶йҮҮз”ЁеҠ е…Ҙд№ҷйҶҮзҡ„ж–№жі•пјҢиҖҢдёҚжҳҜжө“зј©з»“жҷ¶зҡ„еҺҹеӣ жҳҜ_______________гҖӮ III.ж°Ёеҗ«йҮҸзҡ„жөӢе®ҡгҖӮзІҫзЎ®з§°еҸ–mgжҷ¶дҪ“пјҢеҠ йҖӮйҮҸж°ҙжә¶и§ЈпјҢжіЁе…ҘеҰӮеӣҫжүҖзӨәзҡ„дёүйўҲ瓶дёӯпјҢ然еҗҺйҖҗж»ҙеҠ е…ҘVmL10%NaOHжә¶ж¶ІпјҢйҖҡе…Ҙж°ҙи’ёж°”пјҢе°Ҷж ·е“Ғж¶Ідёӯзҡ„ж°Ёе…ЁйғЁи’ёеҮәпјҢ并用蒸йҰҸж°ҙеҶІжҙ—еҜјз®ЎеҶ…еЈҒпјҢз”ЁV1mLClmol/Lзҡ„зӣҗй…ёж ҮеҮҶжә¶ж¶Іе®Ңе…Ёеҗёж”¶гҖӮеҸ–дёӢжҺҘ收瓶пјҢз”ЁC2mol/L NaOHж ҮеҮҶжә¶ж¶Іж»ҙе®ҡиҝҮеү©зҡ„HCl(йҖүз”Ёз”Іеҹәж©ҷдҪңжҢҮзӨәеүӮ)пјҢеҲ°з»ҲзӮ№ж—¶ж¶ҲиҖ—V2mLNaOHжә¶ж¶ІгҖӮ  (5)зҺ»з’ғз®Ў2зҡ„дҪңз”Ё_________________пјҢж ·е“Ғдёӯж°Ёзҡ„иҙЁйҮҸеҲҶж•°зҡ„иЎЁиҫҫејҸ_______гҖӮ (6)дёӢеҲ—е®һйӘҢж“ҚдҪңеҸҜиғҪдҪҝж°Ёеҗ«йҮҸжөӢе®ҡз»“жһңеҒҸдҪҺзҡ„еҺҹеӣ жҳҜ______________гҖӮ A.ж»ҙе®ҡж—¶жңӘз”ЁNaOHж ҮеҮҶжә¶ж¶Іж¶Ұжҙ—ж»ҙе®ҡз®Ў B.иҜ»ж•°ж—¶пјҢж»ҙе®ҡеүҚе№іи§ҶпјҢж»ҙе®ҡеҗҺдҝҜи§Ҷ C.ж»ҙе®ҡиҝҮзЁӢдёӯйҖүз”Ёй…ҡй…һдҪңжҢҮзӨәеүӮ D.еҸ–дёӢжҺҘ收瓶еүҚпјҢжңӘз”Ёи’ёйҰҸж°ҙеҶІжҙ—жҸ’е…ҘжҺҘ收瓶дёӯзҡ„еҜјз®ЎеӨ–еЈҒ |
|
| 19. | иҜҰз»ҶдҝЎжҒҜ | |||||||||
д»Ҙеәҹж—§й”Ңй”°з”өжұ дёӯзҡ„й»‘й”°зІүпјҲMnO2гҖҒMnO(OH)гҖҒNH4ClгҖҒе°‘йҮҸZnCl2еҸҠзӮӯй»‘гҖҒж°§еҢ–й“ҒзӯүпјүдёәеҺҹж–ҷеҲ¶еӨҮMnCl2пјҢе®һзҺ°й”°зҡ„еҶҚеҲ©з”ЁгҖӮе…¶е·ҘдҪңжөҒзЁӢеҰӮдёӢпјҡ пјҲ1пјүиҝҮзЁӢв… пјҢеңЁз©әж°”дёӯеҠ зғӯй»‘й”°зІүзҡ„зӣ®зҡ„жҳҜйҷӨзӮӯгҖҒж°§еҢ–MnO(OH)зӯүгҖӮO2ж°§еҢ–MnO(OH)зҡ„еҢ–еӯҰж–№зЁӢејҸжҳҜ_______гҖӮ пјҲ2пјүжә¶ж¶Іaзҡ„дё»иҰҒжҲҗеҲҶдёәNH4ClпјҢеҸҰеӨ–иҝҳеҗ«жңүе°‘йҮҸZnCl2зӯүгҖӮ 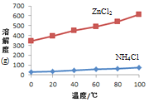 в‘ жә¶ж¶Іaе‘Ҳй…ёжҖ§пјҢеҺҹеӣ жҳҜ______гҖӮ в‘Ў ж №жҚ®еҰӮеӣҫжүҖзӨәзҡ„жә¶и§ЈеәҰжӣІзәҝпјҢе°Ҷжә¶ж¶Іa______пјҲеЎ«ж“ҚдҪңпјүпјҢеҸҜеҫ—NH4ClзІ—е“ҒгҖӮ в‘ў жҸҗзәҜNH4ClзІ—е“ҒпјҢжңүе…іжҖ§иҙЁж•°жҚ®еҰӮдёӢпјҡ
|
||||||||||
| 20. жҺЁж–ӯйўҳ | иҜҰз»ҶдҝЎжҒҜ |
жҹҗжҠ—з»“иӮ зӮҺиҚҜзү©жңүж•ҲжҲҗеҲҶзҡ„еҗҲжҲҗи·ҜзәҝеҰӮеӣҫ(йғЁеҲҶеҸҚеә”з•ҘеҺ»иҜ•еүӮе’ҢжқЎд»¶)пјҡ е·ІзҹҘпјҡa. b. ж №жҚ®д»ҘдёҠдҝЎжҒҜеӣһзӯ”дёӢеҲ—й—®йўҳпјҡ (1)зғғAзҡ„з»“жһ„з®ҖејҸжҳҜ__________гҖӮ (2)в‘ зҡ„еҸҚеә”жқЎд»¶жҳҜ__________пјӣв‘Ўзҡ„еҸҚеә”зұ»еһӢжҳҜ____________гҖӮ (3)дёӢеҲ—еҜ№жҠ—з»“иӮ зӮҺиҚҜзү©жңүж•ҲжҲҗеҲҶеҸҜиғҪе…·жңүзҡ„жҖ§иҙЁжҺЁжөӢжӯЈзЎ®зҡ„жҳҜ__________гҖӮ A.ж°ҙжә¶жҖ§жҜ”иӢҜй…ҡеҘҪпјҢеҜҶеәҰжҜ”иӢҜй…ҡзҡ„еӨ§ B.иғҪеҸ‘з”ҹж¶ҲеҺ»еҸҚеә” C.иғҪеҸ‘з”ҹиҒҡеҗҲеҸҚеә” D.ж—ўжңүй…ёжҖ§еҸҲжңүзўұжҖ§ (4)EдёҺи¶ійҮҸNaOHжә¶ж¶ІеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸжҳҜ________________________________. (5)з¬ҰеҗҲдёӢеҲ—жқЎд»¶зҡ„Eзҡ„еҗҢеҲҶејӮжһ„дҪ“жңү________________з§ҚпјҢе…¶дёӯж ёзЈҒе…ұжҢҜж°ўи°ұжңүеӣӣз»„еі°пјҢеі°йқўз§Ҝд№ӢжҜ”3вҲ¶1вҲ¶1вҲ¶1зҡ„ејӮжһ„дҪ“зҡ„з»“жһ„з®ҖејҸдёә___________________гҖӮ a.дёҺEе…·жңүзӣёеҗҢзҡ„е®ҳиғҪеӣў b.иӢҜзҺҜдёҠзҡ„дёҖзЎқеҹәеҸ–д»Јдә§зү©жңүдёӨз§Қ (6)е·ІзҹҘ  зҡ„еҗҲжҲҗи·Ҝзәҝ______гҖӮ(ж— жңәиҜ•еүӮд»»йҖү) зҡ„еҗҲжҲҗи·Ҝзәҝ______гҖӮ(ж— жңәиҜ•еүӮд»»йҖү) |
|
- е…ЁеӣҪ2019е№ҙй«ҳдёҖеҢ–еӯҰдёҠеӯҰжңҹиҜҫж—¶з»ғд№ е…Қиҙ№жЈҖжөӢиҜ•еҚ·
- жІіеҚ—2019е№ҙй«ҳдәҢеҢ–еӯҰдёҠеҚҠжңҹжңҲиҖғжөӢйӘҢе…Қиҙ№жЈҖжөӢиҜ•еҚ·
- ж№–еҢ—й«ҳдёүеҢ–еӯҰй«ҳиҖғжЁЎжӢҹпјҲ2019е№ҙдёҠеҶҢпјүе…Қиҙ№иҜ•еҚ·
- й«ҳдёӯеҢ–еӯҰдәәж•ҷзүҲ еҝ…дҝ®2 第дёҖз« зү©иҙЁз»“жһ„ е…ғзҙ е‘ЁжңҹеҫӢ 第дёҖиҠӮ е…ғзҙ е‘ЁжңҹиЎЁ ж ёзҙ
- 2017-2018е№ҙй«ҳдәҢдёҠеӯҰжңҹ第дәҢж¬ЎжңҲиҖғеҢ–еӯҰиҖғйўҳеёҰзӯ”жЎҲе’Ңи§ЈжһҗпјҲжІіеҚ—зңҒеҚ—йҳіеёӮзңҒзӨәиҢғжҖ§й«ҳдёӯиҒ”и°ҠеӯҰж Ўпјү
- й«ҳдёӯеҢ–еӯҰдәәж•ҷзүҲ йҖүдҝ®дә” 第дёүз« з¬¬дёүиҠӮ й…Ҝ
- 2017-2018е№ҙй«ҳдёҖдёҠеӯҰжңҹ第дәҢж¬ЎжңҲиҖғеҢ–еӯҰиҖғеҚ·еёҰеҸӮиҖғзӯ”жЎҲе’Ңи§ЈжһҗпјҲжІіеҚ—зңҒеҚ—йҳіеёӮзңҒзӨәиҢғжҖ§й«ҳдёӯиҒ”и°ҠеӯҰж Ўпјү
- жұҫйҳіеёӮ2017е№ҙй«ҳдәҢдёҠеҶҢеҢ–еӯҰй«ҳиҖғжЁЎжӢҹйҷ„зӯ”жЎҲдёҺи§Јжһҗ



