福建2018年高三上学期化学期中考试免费检测试卷
| 1. 选择题 | 详细信息 |
|
厉害了我的国!“中国名片”中航天、军事、天文等领域的发展受到世界瞩目,它们与化学有着密切联系。下列说法正确的是 A. “中国天眼”的“眼眶”是钢铁结成的圈梁,属于新型无机非金属材料 B. “歼−20”飞机上大量使用的碳纤维是一种新型有机高分子材料 C. “神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷是新型无机非金属材料 D. “天宫二号”空间实验室的太阳能电池板的主要材料是二氧化硅 |
|
| 2. 选择题 | 详细信息 |
|
《本草衍义》中对精制砒霜过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如针,尖长者为胜,平短者次之”,文中涉及的操作方法是 A. 萃取 B. 蒸馏 C. 干馏 D. 升华 |
|
| 3. 选择题 | 详细信息 |
|
下列有关物质性质与用途具有对应关系的是 A. SO2具有氧化性,常用于漂白秸秆、织物 B. 明矾水解形成Al(OH)3胶体,可用作水处理中的净水剂 C. 石英坩埚耐高温,可用来加热熔化烧碱、纯碱等固体 D. 次氯酸有酸性,可用于自来水的杀菌消毒 |
|
| 4. 选择题 | 详细信息 |
|
下列家庭化学实验不能达到预期目的的是 A. 用灼烧并闻气味的方法区别纯棉织物和纯羊毛织物 B. 用湿润的淀粉-KI 试纸检验 HCl气体中是否混有 Cl2 C. 向 Ca(ClO)2 溶液中加入硫酸溶液,来证明 S、Cl 的非金属性强弱 D. 将一片铝箔用火灼烧,铝箔熔化但不滴落,证明铝箔表面致密Al2O3薄膜熔点高于Al |
|
| 5. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数的值,下列有关叙述正确的是 A. 常温常压下, 30 g乙烷中所含的极性共价键数为6NA B. 0.2mol N2和0.6mol H2混合充分反应后,转移的电子数目为1.2 NA C. 0.1 mol9038Sr原子中含中子数为3.8NA D. 0.1 mol·L-1的NH4NO3溶液中含有的氮原子数为0.2 NA |
|
| 6. 选择题 | 详细信息 |
|
下列表示对应化学反应的离子方程式正确的是( ) A. 氢氧化铁胶体中加入HI溶液:Fe(OH)3+3H+═Fe3++3H2O B. 用氨水溶解氢氧化铜沉淀:Cu2++4NH3•H2O═[Cu(NH3)4]2++4H2O C. 用稀硝酸除去试管内壁银:3Ag+4H++NO3﹣═3Ag++NO↑+2H2O D. 向NaClO溶液中通入过量的SO2:SO2+NaClO+H2O=HClO+NaHSO3 |
|
| 7. 选择题 | 详细信息 |
如图是金属镁和卤素单质(X2)反应的能量变化示意图。下列说法正确的是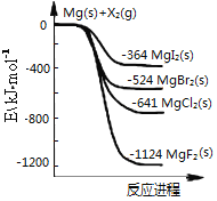 A. 卤素单质(X2)与水反应均可生成两种酸 B. MgF2的电子式为: C. 热稳定性:MgI2>MgBr2>MgCl2>MgF2 D. 由图可知此温度下MgI2(s)与Cl2(g)反应的热化学方程式为:MgI2(s)+Cl2(g)=MgCl2(s)+I2(g) ΔH=-277 kJ·mol-1 |
|
| 8. 选择题 | 详细信息 |
|
常温下,下列各组离子在指定溶液中可能大量共存的是 A. c(OH−)/c(H+)=1×1014的溶液中:K+、Na+、I−、SiO32- B. 水电离出的c( H+)= 1× 10-13 mol·L-1的溶液中:Ca2+、Ba2+、Cl-、HCO3- C. 加入铝粉能放出氢气的溶液中:Ba2+、Cl-、Fe3+、NO3- D. c(SO32-)=0.1 mol·L-1的溶液中:Ca2+、MnO4-、SO42-、H+ |
|
| 9. 选择题 | 详细信息 |
|
下列实验操作正确的是 A. 制备无水氯化铁  B. 配制一定浓度的硫酸溶液 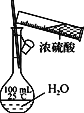 C. 制取少量NH3 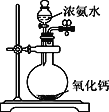 D. 比较NaHCO3和Na2CO3的热稳定性 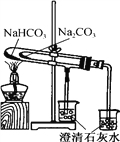 |
|
| 10. 选择题 | 详细信息 |
|
四种短周期元素W、X、Y、Z的原子序数依次增大,W元素的最外层电子数是其电子层数的二倍;X的原子半径是短周期主族元素原子中最大的;Y是地壳中含量最多的金属元素;X与Z形成的离子化合物的水溶液呈中性。下列叙述中,不正确的是 A. 将W的最高价氧化物通入到Na2SiO3溶液中,生成白色沉淀,得出非金属性:W>Si B. 将X单质投入到CuSO4溶液中,生成紫红色固体 C. 工业上用电解熔融Y的氧化物的方法冶炼金属Y D. Z的气态氢化物的沸点在同主族中最低 |
|
| 11. 选择题 | 详细信息 |
向铜屑、稀盐酸和铁盐的混合溶液中持续通入空气可制备氯化铜。其反应过程如图所示。 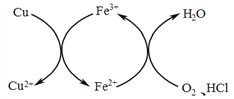 下列说法不正确的是 A. Fe3+对该反应有催化作用 B. 该过程中的Fe3+可由Fe(NO3)3提供 C. 可用K3[Fe(CN)6]溶液区分Fe3+与Fe2+ D. 制备CuCl2的总反应为2Cu + O2 + 4HCl = 2CuCl2 + 2H2O |
|
| 12. 选择题 | 详细信息 |
某同学为测定Na2CO3固体(含少量NaC1)的纯度,设计如下装置(含试剂)进行实验。 下列说法不正确的是 A. 必须在②③间添加吸收HC1的装置 B. ④的作用是防止空气中的气体影响实验的精确度 C. 反应后通入空气的作用是保证②中产生的气体完全转移到③中 D. 根据称取样品和③中产生的沉淀的质量即可求算Na2CO3固体的纯度 |
|
| 13. 选择题 | 详细信息 |
|
下列实验叙述错误的是 A. 用洁净铂丝蘸取溶液进行焰色反应,火焰呈黄色,说明原溶液中有Na+而无法判断是否有K+ B. 配制硫酸铁溶液时,将硫酸铁溶解在硫酸中,再加水稀释 C. 中和滴定时,滴定管用蒸馏水洗涤2~3次后即可加入标准溶液进行滴定 D. 向某钠盐 X 的溶液中先滴加稀盐酸,无现象,再滴加 BaCl2 溶液,出现白色沉淀,X 不一定是Na2SO4 |
|
| 14. 选择题 | 详细信息 |
在好氧菌和厌氧菌作用下废液中NH4+能转化为N2(g)和H2O(l),示意图如下: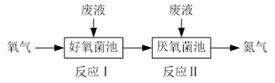 反应I:NH4+(aq)+2O2(g)=NO3-(aq)+2H+(aq)+H2O(l) ΔH1=a kJ·mol-1 反应II:5NH4+(aq)+3NO3-(aq)=4N2(g)+9H2O(l)+2H+(aq) ΔH2=b kJ·mol-1 下列说法正确的是 A. 两池发生的反应中氮元素只被氧化 B. 两池中投放的废液体积相等时NH4+能完全转化为N2 C. 常温常压下,反应II中生成22.4 L N2转移的电子数为3.75×6.02×1023 D. 4NH4+(aq)+3O2(g)=2N2(g)+4H+(aq)+6H2O(l) ΔH= |
|
| 15. 选择题 | 详细信息 |
锂—铜空气燃料电池是低成本高效电池。该电池通过一种复杂的铜“腐蚀”现象产生电能,其中放电过程为2Li+Cu2O+H2O===2Cu+2Li++2OH-。下列说法不正确的是 A. 放电时,Li+透过固体电解质向Cu极移动 B. 通空气时,铜被腐蚀,产生Cu2O C. 放电时,正极的电极反应式为:Cu2O+2H+ +2 e- ===2Cu+H2O D. 整个反应过程中,氧化剂为O2 |
|
| 16. 选择题 | 详细信息 |
研究金属桥墩腐蚀及防护是跨海建桥的重要课题。下列判断中正确的是 A. 用装置①模拟研究时未见a上有气泡产生,说明铁棒没有被腐蚀 B. ②中桥墩与外加电源正极连接能确保桥墩不被腐蚀 C. ③中采用了牺牲阳极的阴极保护法保护桥墩 D. ①②③中海水均是实现化学能转化为电能的电解质 |
|
| 17. 选择题 | 详细信息 | ||||||||||||||||||||
下列根据实验操作和现象所得出的结论正确的是
|
|||||||||||||||||||||
| 18. 选择题 | 详细信息 |
全钒氧化还原电池是一种新型可充电电池,不同价态的含钒离子作为正极和负极的活性物质,分别储存在各自的酸性电解液储罐中。其结构原理如图所示,该电池放电时,右槽中的电极反应为:V2+- e-=V3+,下列说法正确的是 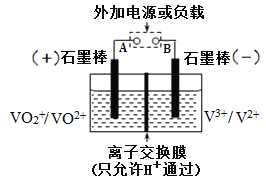 A. 放电时,右槽发生还原反应 B. 放电时,左槽的电极反应式:VO2++2H++e-=VO2++H2O C. 充电时,每转移1mol电子,n(H+)的变化量为1mol D. 充电时,阴极电解液pH升高 |
|
| 19. 选择题 | 详细信息 | |||||||||
已知常温下碳酸、亚硫酸、次氯酸的电离平衡常数如下表:
|
||||||||||
| 20. 选择题 | 详细信息 |
实验小组进行如下实验: 已知:Cr2(SO4)3稀溶液为蓝紫色;Cr(OH)3为灰绿色固体,难溶于水。 下列关于该实验的结论或叙述不正确的是 A. ①中生成蓝紫色溶液说明K2Cr2O7在反应中表现了氧化性 B. 若继续向③中加入稀硫酸,溶液有可能重新变成蓝紫色 C. 将①与③溶液等体积混合会产生灰绿色浑浊,该现象与Cr3+的水解平衡移动有关 D. 操作I中产生的无色气体是CO |
|
| 21. 选择题 | 详细信息 |
硼酸( H3BO3) 为一元弱酸,H3BO3可以通过电解的方法制备。其工作原理如右图所示( 阳膜和阴膜分别只允许阳离子、阴离子通过)。下列说法错误的是 A. a 与电源的正极相连接 B. 阳极的电极反应式为:2H2O-4e-=O2↑+4H+ C. [B(OH)4]-穿过阴膜进入产品室,Na+穿过阳膜进入阴极室 D. 当电路中通过3mol 电子时,可得到1molH3BO3 |
|
| 22. 实验题 | 详细信息 | ||||||||||||
|
硫酰氯(SO2Cl2)和亚硫酰氯(SOCl2)常用作氯化剂,都可用于医药、农药、染料工业及有机合成工业。亚硫酰氯还用于制锂亚硫酰氯(Li/SOCl2)电池。 有关物质的部分性质如下表:
|
|||||||||||||
| 23. 实验题 | 详细信息 |
|
硫代硫酸钠晶体(Na2S2O3·5H2O)又称海波,呈无色透明状,易溶于水,不溶于乙醇,常用作棉织物漂白后的脱氯剂、定量分析中的还原剂。 Ⅰ. Na2S2O3·5H2O的制备 Na2S2O3·5H2O的制备方法有多种,其中亚硫酸钠法是工业和实验室中的主要方法:Na2SO3 + S + 5H2O 制备过程如下: ①称取12.6g Na2SO3于100mL烧杯中,加50 mL去离子水搅拌溶解。 ②另取4.0 g硫粉于200mL烧杯中,加6 mL乙醇充分搅拌均匀将其润湿,再加入Na2SO3溶液,隔石棉小火加热煮沸,不断搅拌至硫粉几乎全部反应。 ③停止加热,待溶液稍冷却后加2 g活性炭,加热煮沸2分钟(脱色)。 ④趁热过滤,得滤液至蒸发皿中, ______________、____________________。 ⑤过滤、洗涤,用滤纸吸干后,称重,计算产率。 (1)加入的硫粉用乙醇润湿的目的是____________________________。 (2)步骤④趁热过滤的原因_____________________,空格处应采取的操作是_________________、____________________。 (3)步骤⑤洗涤过程中,为防止有部分产品损失,应选用的试剂为___________。 (4)滤液中除Na2S2O3和未反应完全的Na2SO3外,最可能存在的无机杂质是________________,生成该杂质的原因可能是____________________________。 Ⅱ.产品纯度的测定 准确称取1.00 g产品(硫代硫酸钠晶体的摩尔质量为248 g/mol),用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 mol/L碘标准溶液滴定至终点,消耗21.00 mL。反应的离子方程式为:2S2O32-+I2=S4O62-+2I-。 (5)计算所得产品的纯度为___________(保留三位有效数字),该数据的合理解释可能是__________(不考虑实验操作引起的误差)。 Ⅲ.产品的应用 (6)Na2S2O3常用于脱氯剂,在溶液中易被Cl2氧化为SO42-,该反应的离子方程式为 ____________________________________。 |
|
| 24. 实验题 | 详细信息 |
|
从古至今,铁及其化合物在人类生产生活中的作用发生了巨大变化。 (1)古代中国四大发明之一的指南针是由天然磁石制成的,其主要成分是______(填字母序号)。 a.Fe b.FeO c.Fe3O4 d.Fe2O3 (2)硫酸渣的主要化学成分为:SiO2约45%,Fe2O3约40%,Al2O3约10%,MgO约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如下(部分操作和条件略):  回答下列问题: ①在步骤i中产生的有毒气体可能有__________________。 ②在步骤iii操作中,要除去的离子之一为Al3+。若常温时Ksp[Al(OH)3]=1.0×10-32,此时理论上使Al3+恰好沉淀完全即溶液中c(Al3+)=1×10-5mol/L,则溶液的pH为____________。 ③步骤iv中,生成FeCO3的离子方程式是_________________。 (3)氯化铁溶液称为化学试剂中的“多面手”,向氯化铜和氯化铁的混合溶液中加入适量氧化铜粉末会产生沉淀,写出该沉淀的化学式______________。这一过程的总反应的离子方程式______。 (4)古老而神奇的蓝色染料普鲁士蓝的合成方法如下:  复分解反应ii的离子方程式是________________。 |
|
| 25. 综合题 | 详细信息 |
|
过二硫酸钾(K2S2O8)在科研与工业上有重要用途。 (1)S2O82-的结构式为[ (2)某厂采用湿法K2S2O8氧化脱硝和氨法脱硫工艺综合处理燃煤锅炉烟气,提高了烟气处理效率,处理液还可以作为城市植被绿化的肥料。 ①脱硫过程中,当吸收液pH=6时,n(SO32-)﹕n(HSO3-)=____。[已知:25℃时,Ka1(H2SO3)=1.5×10-2;Ka2(H2SO3)=1.0×10-7] ②脱硝过程中依次发生两步反应:第1步K2S2O8将NO氧化成HNO2,第2步K2S2O8继续氧化HNO2,第2步反应的化学方程式为________________________________;一定条件下,NO去除率随温度变化的关系如图所示。80℃时,若NO初始浓度为450 mg·m-3,t min达到最大去除率,NO去除的平均反应速率:v(NO) =_______mol.L-1·min-1(列代数式)。  (3)过二硫酸钾可通过“电解→转化→提纯”方法制得,电解装置如下图所示。 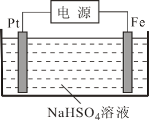 ①电解时,铁电极连接电源的______极。 ②常温下,电解液中含硫微粒主要存在形式与pH的关系如下图所示。已知,硫酸的二级电离常数1.02×10-2,在阳极放电的离子主要是HSO4-,阳极区电解质溶液的pH范围为________,阳极的电极反应式为________。 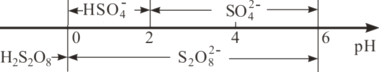 ③往电解产品中加入硫酸钾,使其转化为过二硫酸钾粗产品,提纯粗产品的方法是____________。 |
|
- 2017-2018年高二上学期期中考试化学考卷带参考答案和解析(辽宁省沈阳市东北育才学校)
- 2017-2018年高二上学期第三次月考化学考试(河南省南阳市第一中学)
- 2017-2018年高一上学期期中考试化学考试(北京市第四中学)
- 2018年高考化学二轮专题复习 专题15:无机化工流程题(备考)
- 2015-2016年高三上册化学期末考试题免费试卷(辽宁省葫芦岛市)
- 2015-2016年高二上学期文科化学期末考试带参考答案和解析(山西省太原市)
- 2017-2018年高一上半年期中考试化学考试题(内蒙古巴彦淖尔市第一中学)
- 2017-2018年高二上学期第三次联考化学考卷带参考答案和解析(河南省中原名校)




