2017-2018年高二上学期期中考试化学考卷带参考答案和解析(辽宁省沈阳市东北育才学校)
| 1. | 详细信息 |
|
下列事实不能用勒夏特列原理解释的是 (? ) A.合成氨工业上增大压强以提高反应物的转化率 B.黄绿色的氯水光照后颜色变浅 C.由H2、I2蒸气、HI组成的平衡体系加压后颜色变深 D.在含有Fe(SCN)2+的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去 |
|
| 2. | 详细信息 |
|
下列说法正确的是( ) A. 反应物分子的每次碰撞都能发生化学反应 B. 活化分子之间的碰撞一定是有效碰撞 C. 能够发生化学反应的碰撞是有效碰撞 D. 增大反应物浓度时,活化分子百分数增大 |
|
| 3. | 详细信息 | ||||||||||||||||||||
下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
|
|||||||||||||||||||||
| 4. | 详细信息 |
|
下列有关物质的性质或该物质性质的应用均正确的是( ) A. 醋酸溶液与醋酸钠溶液中的醋酸根均可以水解,同浓度时前者的水解程度比后者低一些 B. 明矾净水与自来水的杀菌清毒原理是一样的 C. MgO和Al2O3在工业上用于制作耐高温材料,可用电解此两种物质冶炼镁、铝金属 D. 氯化亚铁溶液加热蒸干并灼烧得到三氧化二铁 |
|
| 5. | 详细信息 |
|
常温下,下列有关电解质溶液的叙述正确的是? ( ) A. 等浓度等体积的强酸与强碱溶液混合后,溶液的pH=7 B. pH=2的盐酸与pH=12的氨水等体积混合后所得溶液显中性 C. pH=10的Ba(OH)2溶液和pH=13的NaOH溶液等体积混合后溶液的pH=10.7(已知lg 2=0.3) D. 将10 mL pH=a的盐酸与100 mL pH=b的Ba(OH)2溶液混合后恰好中和,则a+b=13 |
|
| 6. | 详细信息 | |||||||||||||||||||||||
一定温度下,在三个体积均为 1.0L的恒容密闭容器中发生反应:2CH3OH(g) ?CH3OCH3(g) + H2O(g)? 下列说法正确的是( )
|
||||||||||||||||||||||||
| 7. | 详细信息 |
|
下列有关说法中不正确的是 A. 某温度时的混合溶液中c(H+)= B. 常温下,由水电离出的c(H+)=10-12mol?L-1的溶液的pH可能为2或12 C. 已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12,向含有Cl-、CrO42-且浓度均为0.010 mol?L-1溶液中逐滴加入0.010 mol?L-1的AgNO3溶液时,CrO42-先产生沉淀 D. 常温下pH=7的CH3COOH和CH3COONa混合溶液中,c(Na+)=c(CH3COO-) |
|
| 8. | 详细信息 |
|
下列叙述正确的是 (? ) A. 25℃时 Cu(OH)2在水中的溶解度大于其在Cu(NO3)2溶液中的溶解度 B. 常温下,NaClO溶液显碱性的原因:ClO?+ H2O =" HClO" + OH? C. 2NO(g) + 2CO(g) = N2(g) + 2CO2(g),在常温下能自发进行,则该反应的△H >0 D. 25℃时向水中加入少量NaOH后,由水电离出的c(H+)?c(OH?)不变 |
|
| 9. | 详细信息 |
|
对于常温下pH=1的硝酸溶液,有关叙述: ①该溶液1mL稀释至100mL后,pH=3 ②向该溶液中加入等体积、pH=13的氢氧化钡溶液恰好完全中和 ③该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为1×10?12 ④向该溶液中加入等体积、等浓度的氨水,所得溶液pH=7 其中正确的是 A. ①② B. ①③ C. ②④ D. ③④ |
|
| 10. | 详细信息 |
|
已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀溶解平衡,测得pH=13,则下列说法不正确的是( ) A. 所得溶液中的c(H+)=1.0×10-13mol?L-1 B. 加入Na2CO3固体,可能生成沉淀 C. 所加的烧碱溶液的pH=13 D. 所得溶液中的c(Mg2+)=5.6×10-10mol?L-1 |
|
| 11. | 详细信息 |
|
用物质的量都是0.1mol的CH3COOH和CH3COONa配制成1L混合溶液,已知其中c(CH3COO-)大于c(Na+)。对该混合溶液的下列判断正确的是( ) A、c(OH-)> c(H+) ? B、c(CH3COOH)+c(CH3COO-)=0.2mol/L C、c(CH3COOH)>c(CH3COO-) D、c(CH3COO-)+c(OH-)=0.2mol/L |
|
| 12. | 详细信息 |
|
已知反应BeCl2+NaBeO2+H2O=2NaCl+2Be(OH)2↓能完全进行,则对下列推断中正确的是( ) A. BeCl2溶液的PH<7,将其蒸干灼烧后,得到的残留物可能为BeO B. Na2BeO2溶液的PH>7,将其蒸干灼烧后,得到的残留物可能为BeO C. Be(OH)2不具有两性 D. BeCl2水溶液的导电性强,因此BeCl2一定是离子化合物 |
|
| 13. | 详细信息 |
|
已知浓度的下列溶液,当温度升高时pH不变的是 A. NaCl B. NaHSO4 C. NaOH D. CH3COONa |
|
| 14. | 详细信息 |
|
下列室温下的溶液中,有关溶液中各粒子的浓度关系判断正确有 ①0.1 mol?L-1CH3COOH溶液中:c(CH3COO-)=c(H+) - c(OH-) ②0.1 mol?L-1CuSO4?(NH4)2SO4?6H2O的溶液中: c(NH ③等体积、等物质的量浓度的弱酸HX和NaX混合后的溶液中: c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) ④pH=2的HA溶液与pH=12的MOH溶液以任意比混合:c(H+)+c(M+) >c(OH-) ⑤0.1 mol/L Na2CO3溶液中:c(OH-)=c(HCO ⑥向醋酸钠溶液中加入醋酸,得到的酸性混合溶液中: c(Na+)>c(CH3COO-)>c(H+)>c(OH-) ⑦pH=7的NH3?NH4Cl混合溶液中:c(NH ⑧0.1 mol?L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) A. 3个 B. 4个 C. 5个 D. 6个 |
|
| 15. | 详细信息 |
|
常温下,下列溶液中的粒子浓度关系正确的是( ) A. 一定物质的量浓度的Na2S溶液中:c(OH-)=c(H+)+2c(H2S)+c(HS-) B. 新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) C. pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) D. 25℃时,浓度均为0.1mol?L-1的CH3COOH、CH3COONa混合溶液pH=4.75,c( |
|
| 16. | 详细信息 |
|
已知25℃时:①HF(aq)+OH-(aq)=F-(aq)+H2O(1)ΔH=-67.7kJ?mol-1, ② H+(aq)+OH-(aq)=H2O(1) ΔH=-57.3kJ?mol-1。在20mL0.1mol?L-1氢氟酸中加入VmL0.1mol?L-1NaOH溶液,下列有关说法不正确的是( ) A. 氢氟酸的电离方程式及热效应可表示为:HF(aq) B. 当V=20时,溶液中:c(OH-)=c(HF)+c(H+) C. 当V=20时,溶液中:c(F-)<c(Na+)=0.1mol?L-1 D. 当V>0时,溶液中可能存在:c(Na+)>c(F-)>c(OH-)>c(H+) |
|
| 17. | 详细信息 |
|
某化学研究性学习小组对电解质溶液作如下的归纳总结(均在常温下),其中正确的是 ( ) ① pH=1的强酸溶液,加水稀释后,溶液中各离子浓度都会降低 ② 1 L 0.50 mol?L-1NH4Cl 溶液与2 L 0.25 mol?L-1NH4Cl 溶液含NH4+ 物质的量完全相等 ③ pH相等的四种溶液:a.CH3COONa b.NaClO c.NaHCO3 d.NaOH,则四种溶液的溶质的物质的量浓度由小到大顺序为:d < b < c < a ④ pH=8.3的NaHCO3溶液:c(Na+) > c(HCO3-) > c(CO32-)> c(H2CO3) ⑤ pH=2的一元酸和pH=12的二元强碱等体积混合:c(OH-) ≤ c(H+) ⑥ pH=4浓度均为0.1 mol?L-1的CH3COOH、CH3COONa混合溶液中:c(CH3COO-)+c(OH-) > c(CH3COOH)+c(H+) A. ③⑤⑥ B. ①③⑤ C. ①②④ D. ②④⑥ |
|
| 18. | 详细信息 |
25℃时,部分含Fe元素的徽粒在溶液中的物质的量分数与溶液pH的关系如图所示,下列说法正确的是 A. HFeO4-在水中的电离程度小于水解程度 B. B、C两点对应溶液中水的电离程度:B > C C. B点溶液加适里水稀释,溶液中所有离子浓度均减小 D. 由A点数据可知,H2FeO4的第一步电离平衡常数Ka1=4.15×l0-4 |
|
| 19. | 详细信息 |
常温下将NaOH溶液添加到己二酸(H2X)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是 A. Ka2(H2X)的数量级为10-6 B. 曲线N表示pH与 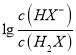 的变化关系 的变化关系C. NaHX溶液中c(H+)>c(OH-) D. 当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(H+)=c(OH-) |
|
| 20. | 详细信息 |
|
常温下,Ka (HCOOH)=1.77×10-4,Ka (CH3COOH)=1.75×10-5,Kb (NH3?H2O) =1.76×10-5,下列说法正确的是 A. 浓度均为0.1 mol?L-1的 HCOONa和NH4Cl 溶液中阳离子的物质的量浓度之和: 前者大于后者 B. 用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和CH3COOH溶液至终点,消耗NaOH溶液的体积相等 C. 0.2 mol?L-1 HCOOH 与 0.1 mol?L-1 NaOH 等体积混合后的溶液中: c(HCOO-) + c(OH-) = c(HCOOH) + c(H+) D. 0.2 mol?L-1 CH3COONa 与 0.1 mol?L-1盐酸等体积混合后的溶液中(pH<7): c(CH3COO-) > c(Cl- ) > c(CH3COOH) > c(H+) |
|
| 21. | 详细信息 | ||||||||
|
(1)Al2(SO4)3溶液加热蒸干并灼烧最终得到物质是________________(填化学式),将NaHCO3与Al2(SO4)3两者溶液混合后可做泡沫灭火剂,其原理是_____________________(用离子方程式表示) (2)实验室溶液中常用NaOH来进行洗气和提纯。当100mL 1mol?L-1的NaOH溶液吸收标准状况下2.24LSO2时,所得溶液中各离子浓度由大到小的顺序为____________________________ (3)25℃时,几种离子开始沉淀时的pH如下表:
|
|||||||||
| 22. | 详细信息 | ||||||||
25℃时,有关物质的电离平衡常数如下:
|
|||||||||
| 23. | 详细信息 | ||||
A、B、C、D、E均为易溶于水的化合物,其离子组成如下表。(各化合物中离子组成不重复)
|
|||||
| 24. | 详细信息 |
(1)甲醇(CH3OH)是重要的溶剂和替代燃料,工业上用CO和H2在一定条件下制备CH3OH的反应为:CO(g)+2H2(g)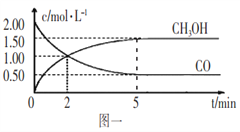 ①从反应开始到5min,用一氧化碳表示的平均反应速率v(CO)=____________。 ②下列说法正确的是____________(填字母序号)。 A.达到平衡时,H2的转化率为65% B.5min后容器中混合气体的平均相对分子质量不再改变 C.达到平衡后,再充入氩气,反应速率减小 D.2min前v(正)>v(逆),2min后v(正) (2)碳与水蒸气反应制取H2的相关反应如下: Ⅰ:C(s)+H2O(g)=CO(g)+H2(g) △H=+131.0kJ/mol Ⅱ:CO(g)+H2O(g)=CO2(g)+H2(g)? △H= - 43kJ/mol Ⅲ:CaO(s)+CO2(g)=CaCO3(S) △H= - 178.3kJ/mol 计算反应C(s)+2H2O(g)+CaO(s) 若K1、K2、K3分别为反应Ⅰ、Ⅱ、Ⅲ的平衡常数,该平衡常数K=__________(用K1、K2、K3表示)。 ②对于可逆反应C(s)+2H2O(g)+CaO(s) A.降低体系的温度 B.压缩容器的体积 C.增加CaO的量 D.选用适当的催化剂 |
|
| 25. | 详细信息 | ||||||||
|
用沉淀滴定法快速测定NaI等碘化物溶液中c(I?),实验过程包括准备标准溶液和滴定待测溶液。 Ⅰ.准备标准溶液 a.准确称取AgNO3基准物4.2468 g(0.0250 mol)后,配制成250 mL标准溶液,放在棕色试剂瓶中避光保存,备用。 b.配制并标定100 mL 0.1000 mol?L?1 NH4SCN标准溶液,备用。 Ⅱ.滴定的主要步骤 a.取待测NaI溶液25.00 mL于锥形瓶中。 b.加入25.00 mL 0.1000 mol?L?1 AgNO3溶液(过量),使I?完全转化为AgI沉淀。 c.加入NH4Fe(SO4)2溶液作指示剂。 d.用0.1000 mol?L?1NH4SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。 e.重复上述操作两次。三次测定数据如下表:
|
|||||||||



