湖南省五市十校2021届高三上册第二次大联考化学试卷带参考答案和解析
| 1. 选择题 | 详细信息 |
2020年7月23日我国首个火星探测器“天问一号”发射成功。火星车所涉及的下列材料中属于金属材料的是( ) A.用石墨纤维和硅制成的太阳能电池复合材料 B.温控涂层材料的成分聚酰胺 C.用钛合金做的车轮材料 D.探测仪镜头材料用的二氧化硅 |
|
| 2. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数的值,下列说法正确的是( ) A. B.含 C. D.标准状况下, |
|
| 3. 选择题 | 详细信息 |
|
下列对化学用语的描述中,正确的是( ) A.羟基与氢氧根离子的电子式都可表示为: B.  C.由 D. |
|
| 4. 选择题 | 详细信息 |
|
下列对实验现象解释的方程式中,正确的是( ) A.向醋酸中加入小苏打溶液,产生无色气体: B.向 C.向 D.向铬酸钾溶液中滴入少量浓硫酸,溶液变橙色: |
|
| 5. 选择题 | 详细信息 |
实验室提纯含少量氯化钠杂质的硝酸钾的过程如图所示,下列分析错误的是( ) A.操作Ⅰ是溶解,操作Ⅱ是蒸发浓缩 B.若从分离出固体的滤液中获得 C.操作Ⅲ是降温结晶→过滤→洗涤→干燥,使硝酸钾晶体从溶液中分离出来 D.除去 |
|
| 6. 选择题 | 详细信息 |
已知某有机物X的结构简式如图所示,下列说法正确的是( )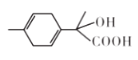 A.X属于芳香烃的含氧衍生物 B.X的分子式为 C.X分子只含有两种官能团 D.X分子可发生取代、消去、加成、氧化、缩聚反应 |
|
| 7. 选择题 | 详细信息 |
二氧化硫—空气质子交换膜燃料电池将化学能转变成电能的同时,实现了制硫酸、发电、环保三位一体的结合,降低了成本提高了效益,其原理如图所示(注:质子指 A. B. C.相同条件下,放电过程中消耗的 D. |
|
| 8. 选择题 | 详细信息 |
 A.在“反应”步骤中参加反应的 B.在“反应”步骤中氧化性: C.“电解”中阴极反应的主要产物是 D.氯元素的化合价为 |
|
| 9. 选择题 | 详细信息 |
某研究小组以AgZSM为催化剂,在容积为1 L的容器中,相同时间下测得0.1 mol NO转化为 A.达到平衡后,其他条件不变,使 B.反应 C. D.Y点再通入 |
|
| 10. 选择题 | 详细信息 |
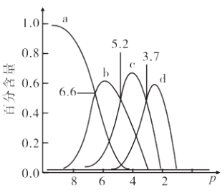 A.常温下,电离方程式: B.曲线c表示 C. D.常温下,向  变小 变小 |
|
| 11. 选择题 | 详细信息 |
|
类比学习是一种认知思维与推测的方法。通过把两个或两类事物或情形进行比较,找出它们在某一抽象层上的相似关系,并以此为依据适当整理对应到另一事物或情况,从而获得有效的认知。下列说法合理的是( ) A.向 B. C. D.向 |
|
| 12. 选择题 | 详细信息 |
|
硫酸亚铁铵隔绝空气加热到500℃发生的反应为: A.该反应的还原产物为 B.X是 C.每生成 D.分别氧化铁元素、氮元素所需的硫酸根离子的物质的量之比为1∶1 |
|
| 13. 选择题 | 详细信息 |
海洋生物参与氮循环过程如图所示: 下列说法不正确的是( ) A.反应①~⑤中包含3个氧化还原反应 B.反应②中有极性键断裂和非极性键生成 C.反应③中可能有氧气参与反应 D.等量 |
|
| 14. 选择题 | 详细信息 |
某同学欲从苯与溴反应后的混合物中分离出溴苯和无水 A.装置甲中 B.反应后向反应混合物中加入蒸馏水,用乙装置分离有机层和水层,可观察到图中所示的现象 C.用装置丙将分液后的水层蒸发至干燥,再灼烧制得无水 D.将经水洗、碱洗、水洗后的粗溴苯蒸馏后可以得到纯溴苯 |
|
| 15. 选择题 | 详细信息 |
一定条件下可发生反应 有人提出利用电化学处理,可提高能量的利用率,下列说法不正确的是( ) A.若设计为原电池,则通入甲烷的电极为负极 B.由图像可知①→②放出能量并形成了 C.使用催化剂,可降低活化能和焓变,加快反应速率 D.若设计为原电池,用稀硫酸作电解质溶液,正极反应为: |
|
| 16. | 详细信息 |
|
A、B、D、E、F是原子序数依次增大的五种短周期元素。A是周期表中相对原子质量最小的元素,A、B能形成两种液态化合物 (1)E在周期表中的位置是___________。 (2)如下图所示,将F单质的水溶液分别滴入盛有不同试剂的试管中。  ①试管a中发生反应的离子方程式为___________,该反应可用于制备漂白液。 ②试管b中的实验现象为___________,说明F的非金属性强于碘,从原子结构的角度解释其原因是___________。 (3)镓( a. b. c. (4) |
|
| 17. | 详细信息 |
我国科学家潘锦功发明了碲化镉薄膜太阳能电池,又称为“发电玻璃”,被誉为“挂在墙上的油田”,使得碲元素重新走进人们的视野。以锡碲渣(主要含 已知:Ⅰ.锡酸钠( Ⅱ. (1)在生产过程中,要将锡碲渣粉碎,其目的是___________。 (2)“碱浸”过程中,锡碲浸出率与溶液中碱的质量浓度关系如图所示,最理想的碱的质量浓度为  (3)“氧化”时,反应的离子方程式为___________。 (4)“沉碲”时加入硫酸控制溶液的 (5)以石墨为电极对浸出液电解可获得 (6)碲产品中碲质量分数的测定,步骤如下: ①取 ②往锥形瓶中加入 ③用 |
|
| 18. 实验题 | 详细信息 |
氨基甲酸铵( (1)仪器A的名称是___________,需往其中加入的固体可能是___________(填名称)。 (2)按气流方向连接各仪器: (3)装置Ⅵ中,采用冰水浴的原因为___________;当 A.蒸馏 B.高压加热烘干 C.真空微热烘干 某同学认为这套装置制得的氨基甲酸铵易变质,同时不符合绿色化学理念,改进了装置,具体做法是___________。 |
|
| 19. | 详细信息 |
|
二甲醚( ① ② ③ (1)一种新合成二甲醚的方法为一定条件下: 判断该反应在一定温度下、体积恒定的密闭容器中,下列不能作为达到化学平衡状态的依据是___________。 A.平均摩尔质量保持不变 B.容器的密度不变 C.容器内压强保持不变 D.单位时间内消耗 (2)可采用 反应①: 反应②: a.压强为  b.温度对平衡体系中乙酸甲酯的含量和乙醇的影响如图乙所示,在 c.若压强为 |
|
| 20. | 详细信息 |
新型冠状病毒引起了全世界的关注。各国科学工作者日夜研究各种药物来治疗新型冠状病毒( 已知:Ⅰ. Ⅱ.  回答下列问题: (1)C中含氧官能团的名称为___________。 (2)G到H的反应类型为___________。 (3)由B生成C的化学反应方程式为___________。 (4)E中含两个Cl原子,则E的结构简式为___________。 (5)X是C的同分异构体,写出满足下列条件的X的结构简式___________。 ①苯环上含有硝基且苯环上的一氯取代产物只有二种; ②能发生水解反应; ③能发生银镜反应。 (6)设计由苯甲醇为原料制备化合物  的合成路线(无机试剂任选)___________。 的合成路线(无机试剂任选)___________。 |
|
最近更新



