жұҹиӢҸиӢҸе·һеёӮ2021еұҠй«ҳдёүдёӢжңҹжңҹеҲқеӯҰдёҡиҙЁйҮҸйҳіе…үжҢҮж Үи°ғз ”еҢ–еӯҰйўҳе…Қиҙ№иҜ•еҚ·
| 1. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
еҠ ејәж°ҙиө„жәҗдҝқжҠӨжҳҜе®һзҺ°з”ҹжҖҒж–ҮжҳҺзҡ„ж ёеҝғгҖӮдёӢеҲ—еҒҡжі•дёҚеә”иҜҘжҸҗеҖЎзҡ„жҳҜ( ) A.е°Ҷжңүе®іжұЎжҹ“зү©ж·ұеәҰеЎ«еҹӢ B.еҹ№е…»иҠӮзәҰз”Ёж°ҙзҡ„ж„ҸиҜҶ C.еҮҸе°‘еҶңдёҡз”ҹдә§дёӯеҢ–иӮҘе’ҢеҶңиҚҜзҡ„дҪҝз”Ё D.еҗҲзҗҶдҪҝз”Ёж— е®іеҢ–еӨ„зҗҶеҗҺзҡ„з”ҹжҙ»жұЎж°ҙ |
|
| 2. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
еҸҚеә”Cl2+Na2SO3+H2O=Na2SO4+2HClеҸҜз”ЁдәҺжұЎж°ҙи„ұж°ҜгҖӮдёӢеҲ—зӣёе…іеҫ®зІ’зҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜ( ) A.дёӯеӯҗж•°дёә20зҡ„ж°ҜеҺҹеӯҗпјҡ C.Na+зҡ„з»“жһ„зӨәж„Ҹеӣҫпјҡ |
|
| 3. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—з”ЁдәҺжұЎж°ҙеӨ„зҗҶзҡ„зү©иҙЁпјҢе…¶жҖ§иҙЁдёҺз”ЁйҖ”е…·жңүеҜ№еә”е…ізі»зҡ„жҳҜ( ) A.Ca(ClO)2жңүејәж°§еҢ–жҖ§пјҢеҸҜз”ЁдәҺж¶ҲжҜ’жқҖиҸҢ B.жҳҺзҹҫзҡ„з„°иүІе‘Ҳзҙ«иүІпјҢеҸҜз”ЁдәҺжІүйҷҚжіҘжІҷ C.жңЁзӮӯе…·жңүиҝҳеҺҹжҖ§пјҢеҸҜз”ЁдәҺеҗёйҷ„иӢҜзӯүжңүжңәзү© D.CaOе…·жңүеҗёж°ҙжҖ§пјҢеҸҜз”ЁдәҺжІүж·ҖйҮҚйҮ‘еұһзҰ»еӯҗ |
|
| 4. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
з”ЁзҹізҒ°д№іеҗёж”¶зЎқй…ёе·Ҙдёҡзҡ„е°ҫж°”(еҗ«NOгҖҒNO2)еҸҜиҺ·еҫ—Ca(NO2)2пјҢе…¶йғЁеҲҶе·ҘиүәжөҒзЁӢеҰӮдёӢпјҡ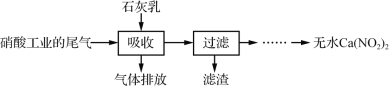 дёӢеҲ—иҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜ( ) A.еҗёж”¶ж—¶дё»иҰҒеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёәNO+NO2+Ca(OH)2=Ca(NO2)2+H2O B.е°ҶзҹізҒ°д№іж”№дёәжҫ„жё…зҹізҒ°ж°ҙеҗёж”¶ж•ҲзҺҮе°ҶдјҡеўһеӨ§ C.йҮҮз”Ёж°”ж¶ІйҖҶжөҒжҺҘи§ҰжңүеҲ©дәҺе°ҫж°”дёӯNOгҖҒNO2зҡ„е……еҲҶеҗёж”¶ D.иӢҘе°ҫж°”дёӯn(NO2)вҲ¶n(NO)пјң1вҲ¶1пјҢеҗёж”¶еҗҺжҺ’ж”ҫзҡ„ж°”дҪ“дёӯNOеҗ«йҮҸеҚҮй«ҳ |
|
| 5. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
зҹӯе‘Ёжңҹдё»ж—Ҹе…ғзҙ XгҖҒYгҖҒZгҖҒWеҺҹеӯҗеәҸж•°дҫқж¬ЎеўһеӨ§пјҢXеҺҹеӯҗж ёеӨ–жңү7дёӘз”өеӯҗпјҢYеңЁе‘ЁжңҹиЎЁдёӯдҪҚдәҺв…ЎAж—ҸпјҢZдёҺXеұһдәҺеҗҢдёҖдё»ж—ҸпјҢеҹәжҖҒWеҺҹеӯҗзҡ„ж ёеӨ–жңү2дёӘжңӘжҲҗеҜ№з”өеӯҗгҖӮдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜ( ) A.еҺҹеӯҗеҚҠеҫ„пјҡr(X)<r(Y)<r(Z)<r(W) B.第дёҖз”өзҰ»иғҪпјҡI1(Y)<I1 (W)<I1 (Z) C.Zзҡ„жңҖй«ҳд»·ж°§еҢ–зү©еҜ№еә”ж°ҙеҢ–зү©зҡ„й…ёжҖ§жҜ”Xзҡ„ејә D.е…ғзҙ YгҖҒWзҡ„з®ҖеҚ•зҰ»еӯҗе…·жңүзӣёеҗҢзҡ„з”өеӯҗеұӮз»“жһ„ |
|
| 6. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
дҫҜж°ҸеҲ¶зўұжі•д»Ҙж°ҜеҢ–й’ гҖҒдәҢж°§еҢ–зўігҖҒж°Ёе’Ңж°ҙдёәеҺҹж–ҷпјҢ еҸ‘з”ҹеҸҚеә”NaCl+NH3+CO2+H2O=NaHCO3вҶ“+NH4ClгҖӮе°ҶжһҗеҮәзҡ„еӣәдҪ“зҒјзғ§иҺ·еҸ–зәҜзўұпјҢеҗ‘жһҗеҮәеӣәдҪ“еҗҺзҡ„жҜҚж¶ІдёӯеҠ е…ҘйЈҹзӣҗеҸҜиҺ·еҫ—еүҜдә§е“Ғж°ҜеҢ–й“өгҖӮдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜ( ) A.CO B.NaHCO3зҡ„зғӯзЁіе®ҡжҖ§жҜ”Na2CO3ејә C.з”Ёжҫ„жё…зҹізҒ°ж°ҙеҸҜд»ҘйүҙеҲ«Na2CO3дёҺNaHCO3 D.зӣёеҗҢжё©еәҰдёӢпјҢNH4ClеңЁж°ҙдёӯзҡ„жә¶и§ЈеәҰеӨ§дәҺеңЁNaClжә¶ж¶Ідёӯзҡ„жә¶и§ЈеәҰ |
|
| 7. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||
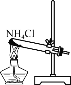
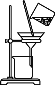
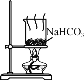
дҫҜж°ҸеҲ¶зўұжі•д»Ҙж°ҜеҢ–й’ гҖҒдәҢж°§еҢ–зўігҖҒж°Ёе’Ңж°ҙдёәеҺҹж–ҷпјҢеҸ‘з”ҹеҸҚеә”NaCl+NH3+CO2+H2O=NaHCO3вҶ“+NH4ClгҖӮе°ҶжһҗеҮәзҡ„еӣәдҪ“зҒјзғ§иҺ·еҸ–зәҜзўұпјҢеҗ‘жһҗеҮәеӣәдҪ“еҗҺзҡ„жҜҚж¶ІдёӯеҠ е…ҘйЈҹзӣҗеҸҜиҺ·еҫ—еүҜдә§е“Ғж°ҜеҢ–й“өгҖӮдёӢеҲ—жңүе…іжЁЎжӢҹдҫҜж°ҸеҲ¶зўұжі•зҡ„е®һйӘҢеҺҹзҗҶе’ҢиЈ…зҪ®иғҪиҫҫеҲ°е®һйӘҢзӣ®зҡ„зҡ„жҳҜ( )
|
|||||||||||||
| 8. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
йҖҡиҝҮд»ҘдёӢдёӨжӯҘеҸҚеә”еҸҜе®һзҺ°NH4ClеҲҶи§Јдә§зү©зҡ„еҲҶзҰ»гҖӮ NH4Cl(s)+MgO(s) Mg(OH)Cl(s) дёӢеҲ—иҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜ( ) A.еҸҚеә”NH4Cl(s)=NH3(g)+HCl(g)зҡ„О”H=+158.84 kJВ·mol -1 B.дёӨжӯҘеҸҚеә”зҡ„О”SеқҮеӨ§дәҺ0 C.MgOжҳҜNH4ClеҲҶи§ЈеҸҚеә”зҡ„еӮ¬еҢ–еүӮ D.5.35 g NH4Clе®Ңе…ЁеҲҶи§ЈзҗҶи®әдёҠеҸҜиҺ·еҫ—ж ҮеҮҶзҠ¶еҶөдёӢзҡ„HClзәҰ2.24 L |
|
| 9. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
зЎ«й…ёдәҡй“ҒжҳҜдёҖз§ҚйҮҚиҰҒзҡ„еҢ–е·ҘеҺҹж–ҷпјҢйғЁеҲҶиҪ¬еҢ–еҰӮдёӢеӣҫжүҖзӨәгҖӮдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜ( )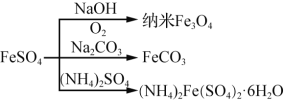 A.з”Ёй…ёжҖ§KMnO4жә¶ж¶ІеҸҜд»ҘжЈҖйӘҢFeSO4жҳҜеҗҰеҸҳиҙЁ B.еҲ¶зәізұіFe3O4ж—¶йҖҡе…Ҙзҡ„O2йңҖиҝҮйҮҸ C.еҲ¶FeCO3ж—¶еә”е°ҶNa2CO3жә¶ж¶ІеҠ е…ҘFeSO4жә¶ж¶Ідёӯ D.з”ҹжҲҗ(NH4)2Fe(SO4)2В·6H2Oзҡ„еҸҚеә”дёәж°§еҢ–иҝҳеҺҹеҸҚеә” |
|
| 10. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
з”Ёжө·ж°ҙжҷ’зӣҗеҗҺзҡ„иӢҰеҚӨж°ҙз”ҹдә§йҮ‘еұһMgзҡ„иҝҮзЁӢеҸҜиЎЁзӨәеҰӮдёӢпјҡиӢҰеҚӨж°ҙ A.еҸҚеә”Mg2+(aq)+Ca(OH)2(s) 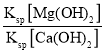 B.еёёжё©дёӢпјҢMg(OH)2жә¶дәҺзӣҗй…ёжүҖеҫ—MgCl2жә¶ж¶Ідёӯc(H+)В·c(OH-)пјң10-14 C.е°ҶMgCl2жә¶ж¶Іи’ёе№Іеҫ—еҲ°ж— ж°ҙMgCl2 D.з”өи§ЈзҶ”иһҚMgCl2еңЁйҳҙжһҒиҺ·еҫ—йҮ‘еұһMg |
|
| 11. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
еҢ–еҗҲзү©ZжҳҜеҗҲжҲҗжҹҗз§Қж¶ҲзӮҺй•Үз—ӣиҚҜзү©зҡ„йҮҚиҰҒдёӯй—ҙдҪ“пјҢеҸҜз”ұдёӢеҲ—еҸҚеә”еҲ¶еҫ—гҖӮ дёӢеҲ—жңүе…іеҢ–еҗҲзү©XгҖҒYе’ҢZзҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜ( ) A.Xж—ўиғҪдёҺзӣҗй…ёд№ҹиғҪдёҺNaOHжә¶ж¶ІеҸҚеә” B.YиғҪеҸ‘з”ҹзј©иҒҡгҖҒж°§еҢ–гҖҒж¶ҲеҺ»еҸҚеә” C.ZеҲҶеӯҗдёӯеҗ«ж°§е®ҳиғҪеӣўзҡ„еҗҚз§°дёәзҫҹеҹәе’Ңзҫ§еҹә D.XдёҺи¶ійҮҸH2еҠ жҲҗеҗҺзҡ„дә§зү©дёӯеҗ«жңү5дёӘжүӢжҖ§зўіеҺҹеӯҗ |
|
| 12. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
еҗ‘CuSO4жә¶ж¶ІдёӯйҖҗж»ҙж»ҙеҠ ж°Ёж°ҙпјҢе…Ҳз”ҹжҲҗи“қиүІжІүж·ҖпјҢеҗҺи“қиүІжІүж·ҖйҖҗжёҗжә¶и§Јдёәж·ұи“қиүІжә¶ж¶ІпјҢеҗ‘ж·ұи“қиүІжә¶ж¶ІдёӯеҠ е…Ҙ95%д№ҷйҶҮпјҢж·ұи“қиүІжә¶ж¶ІеҸҳжө‘жөҠпјҢйқҷзҪ®еҗҺжңүж·ұи“қиүІзЎ«й…ёеӣӣж°ЁеҗҲй“ңжҷ¶дҪ“жһҗеҮәпјҢдёҠеұӮжә¶ж¶ІйўңиүІеҸҳжө…гҖӮдёӢеҲ—жңүе…іиҜҙжі•жӯЈзЎ®зҡ„жҳҜ( ) A.з”ҹжҲҗи“қиүІжІүж·ҖеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸдёәCu2++2OH-=Cu(OH)2вҶ“ B.NH3жһҒжҳ“жә¶дәҺж°ҙжҳҜеӣ дёәж°ЁеҲҶеӯҗй—ҙжҳ“еҪўжҲҗж°ўй”® C.и“қиүІжІүж·Җжә¶и§Јдёәж·ұи“қиүІжә¶ж¶ІжҳҜеӣ дёәNH D.зЎ«й…ёеӣӣж°ЁеҗҲй“ңеңЁд№ҷйҶҮдёӯзҡ„жә¶и§ЈеәҰе°ҸдәҺеңЁж°ҙдёӯзҡ„жә¶и§ЈеәҰ |
|
й«ҳдёӯеҢ–еӯҰ иҜ•еҚ·жҺЁиҚҗ
- еҶ…и’ҷеҸӨеҢ…еӨҙеёӮй«ҳдәҢеҢ–еӯҰдёӢеҶҢжңҲиҖғиҜ•еҚ·жЁЎжӢҹиҖғиҜ•и®ӯз»ғ
- 2019-2020е№ҙй«ҳдёҖдёҠжңҹ第дёүж¬ЎжңҲиҖғеҢ–еӯҰиҖғиҜ•е®Ңж•ҙзүҲпјҲж№–еҚ—зңҒйӮөдёңеҺҝ第дёҖдёӯеӯҰпјү
- й«ҳдёүеҢ–еӯҰдёӢеҶҢдё“йўҳз»ғд№ еңЁзәҝжөӢйӘҢе®Ңж•ҙзүҲ
- й»‘йҫҷжұҹеҶңеһҰе»әдёүжұҹз®ЎзҗҶеұҖ第дёҖй«ҳзә§дёӯеӯҰ2020-2021е№ҙй«ҳдёҖдёҠеӯҰжңҹ12жңҲжңҲиҖғеҢ–еӯҰе…Қиҙ№иҜ•еҚ·еёҰзӯ”жЎҲе’Ңи§Јжһҗ
- й•ҝжҳҘеёӮ2019е№ҙй«ҳдёҖеҢ–еӯҰдёӢеҚҠе№ҙжңҲиҖғжөӢйӘҢеҗҢжӯҘз»ғд№
- еҢ—дә¬еёӮй«ҳдәҢеҢ–еӯҰдёҠеҶҢжңҹжң«иҖғиҜ•еңЁзәҝжөӢйӘҢе®Ңж•ҙзүҲ
- зҰҸе»әзңҒиҺҶз”°еёӮж¶өжұҹеҢәиҺҶ田第дёғдёӯеӯҰ2020-2021е№ҙй«ҳдәҢдёҠжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰиҜ•еҚ·еңЁзәҝз»ғд№
- ж№–еҚ—2019е№ҙй«ҳдәҢеҢ–еӯҰеүҚеҚҠжңҹжңҹдёӯиҖғиҜ•еңЁзәҝе…Қиҙ№иҖғиҜ•
жңҖиҝ‘жӣҙж–°