2020年黑龙江省哈尔滨市香坊区中考一模化学免费试卷完整版
| 1. | 详细信息 |
3月18日,地铁2号线在建工程在做好疫情防控工作基础上正式复工。地铁2号线距离年底前通车的目标又近一步。下列有关说法不正确的是() A.地铁行驶时的能量转化是电能转化为机械能 B.地铁钢轨是用韧性好、硬度大的锰钢制成的 C.钢的含碳量2%~4.3%,生铁的含碳量0.03%~2% D.修建地铁站使用了塑料,塑料属于合成材料 |
|
| 2. | 详细信息 |
|
下列配制一定质量分数的氯化钠溶液的实验操作错误的是() A.  取用氯化钠 B. 取用氯化钠 B. 称量氯化钠质量 称量氯化钠质量C.  量取水的体积 D. 量取水的体积 D. 溶解氯化钠 溶解氯化钠 |
|
| 3. | 详细信息 |
|
下列做法错误的是() A.酒精灯内的酒精在桌面起火燃烧,立即用湿抹布盖灭 B.为了减轻蚊虫叮咬后的痛痒,在叮咬处涂上一些牙膏 C.家里用热的纯碱溶液代替洗涤剂洗餐具 D.发现天然气泄漏,立即打电话报警 |
|
| 4. | 详细信息 |
|
下列过程没有发生化学变化的是() A.  检验氧气 B. 检验氧气 B.  稀释浓硫酸 稀释浓硫酸C.  二氧化碳溶解性实验 D. 二氧化碳溶解性实验 D. 酸、碱溶液改变花的颜色 酸、碱溶液改变花的颜色 |
|
| 5. | 详细信息 |
|
下列实验现象描述正确的是() A.稀盐酸与氧化铁反应,红棕色固体逐渐减少,溶液由无色变为浅绿色 B.点燃氢气后观察到淡蓝色火焰,火焰上方有水雾生成 C.在酒精灯火焰上加热铜丝,紫红色固体表面变黑 D.镁带在空气中燃烧产生黄白色火焰,放出热量,产生大量白烟 |
|
| 6. | 详细信息 |
|
人体健康离不开化学,下列叙述不正确的是 A.人体中含量较多的四种元素是氧、碳、氢、氮 B.食用铁强化酱油可以预防地方性甲状腺肿大 C.幼儿及青少年缺钙会患佝偻病和发育不良 D.奶制品、豆类、虾皮等食物中含有丰富的钙元素 |
|
| 7. | 详细信息 |
|
石蕊是从地衣植物中提取得到的色素,能部分溶于水而显紫色,是一种常用的酸碱指示剂,石蕊的化学式是C7H7O4N,下列有关石蕊的叙述正确的是() A.石蕊是由四种原子构成的有机化合物 B.一个石蕊分子中含有87个质子 C.石蕊中氮元素与氢元素的质量比为2:1 D.石蕊分子中质子数等于中子数 |
|
| 8. | 详细信息 | |||||||||||||||
对下列事实的解释不正确的是()
|
||||||||||||||||
| 9. | 详细信息 |
|
下列有关资源和能源的叙述不正确的是() A.人们正在利用和开发的其他能源有太阳能、风能、生物质能等 B.回收废旧金属可以节约金属资源和能源 C.地球上可利用的淡水资源很少,不足全球水储量的1% D.空气是一种宝贵的资源,其中氧气约占空气质量的21% |
|
| 10. | 详细信息 | ||||||||||||||||||||||
实验室区分下列各组物质的两种方法都正确的是()
|
|||||||||||||||||||||||
| 11. | 详细信息 |
如图是甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法错误的是() A.甲、乙均属于易溶性物质 B.10°C时,等质量的甲、乙饱和溶液中所含溶质的质量相等 C.10°C时,分别将甲、乙两物质的溶液恒温蒸发等质量的水,析出晶体的质量不一定相等 D.20°C时,乙物质溶液的溶质质量分数约为33.3% |
|
| 12. | 详细信息 | ||||||||||||||||||||
除去下列物质中的少量杂质所选用的试剂或方法正确的是()
|
|||||||||||||||||||||
| 13. | 详细信息 |
|
现有一定质量的碳酸钡和碳酸钾的固体混合物,与100g 质量分数14.6%的稀盐酸恰好完全反应,将反应后的溶液蒸干得到34.2g固体,则原混合物中氧元素的质量分数为( ) A.30% B.8.5% C.15% D.17% |
|
| 14. | 详细信息 |
同学们都比较喜欢吃披萨,披萨是一种以面粉为主要原料,辅以蔬菜、水果、肉类等制成的食物。请回答下列问题: (1)如图这款披萨的辅料有火腿、虾仁、 蓝莓、西红柿等,其中面饼主要为人体提供的营养素是①_____(水除外)。蓝莓富含的营养素的作用是②__________, 预防疾病,③___________。 (2)盛披萨的平底铁锅用完后,需要洗净晾干,原因是①___________。铁锅手柄的最外层使用木头或热固性塑料,目的是②_________。 (3)种植西红柿时发现其抗病虫害能力弱,且叶片发黄,可以施加________(填一种化肥的化学式)来解决。 |
|
| 15. | 详细信息 |
如图所示是全球最大太阳能飞机“阳光动力2号”。 “阳光动力2号”的机身和机翼均采用碳纤维复合材料制成,该机的机翼、机身和水平尾翼上共贴敷了17248 片135pμm厚的单晶硅薄膜太阳能电池。请回答下列问题: (1)碳纤维复合材料是有机纤维经过一系列热处理转化而成,含碳量高于90%,其强度比钢高五倍,重量却不到钢的一半。碳纤维复合材料具有的优良性能是________(填字母)。 A 硬度大、密度大 B 密度小、熔点低 C 密度小、强度高 (2)太阳能电池芯片的常用材料是“单晶硅”。硅的元素符号是①_______,高纯硅常用作半导体材料,这说明硅具有②_________性。 (3)制造该飞机时常用乙炔( C2H2)进行焊接。实验室可以用电石( CaC2 )和水反应制得乙炔气体,同时生成一种碱。该反应的化学方程式为①__________,电石中碳元素的化合价是②________。 (4)太阳能飞机与用航空煤油做燃料的飞机相比,不仅可以节约_______,还可以减少对空气的污染。 |
|
| 16. | 详细信息 |
下图是某化学反应的微观模拟图,请回答问题: (1)请在丙图中将相关粒子图形补充完整_________。 (2)写出乙到丙变化的微观实质_________。 (3)写出该反应的化学方程式_________。 (4)某元素比氮元素多一个周期多两个族,写出该元素的离子符号_________。 |
|
| 17. | 详细信息 | ||||||||
|
比较、归类是学习化学常用的方法。 (1)初中化学实验可以按照实验目的分为:“混合物分离提纯实验”、“探究物质反应条件实验”、“探究物质性质的实验”等。据此我们可以将实验C与实验①____________ (填字母)归为一类,分类依据是②__________。
|
|||||||||
| 18. | 详细信息 |
下图是实验室制取气体的发生装置和收集装置,请回答问题: (1)仪器①的名称是________。 (2)若在实验室用一种固体制取氧气,选用的发生装置是①___(填字母),该反应的化学方程式为②__。 (3)制取氧气时,首先要检查装置气密性:连接好仪器,将导管一端浸入水中,用手紧握容器外壁,如果观察到水中导管口有①_______,说明装置不漏气。产生上述现象的原因是:手紧握容器外壁,容器内②______,大于外界大气压,在压强差的作用下出现上述现象。 (4)在C、D、E、F四个装置中,不能用于收集二氧化碳气体的是①____(填字母),原因是②_______。 |
|
| 19. | 详细信息 |
图中A、B 、C、D、E、F是初中化学常见的物质,且A、B、C、D、E是五种不同类别的物质,己知B是目前世界上年产量最高的金属,A与D反应产生白色沉淀。图中“一”表示相连的物质之间可以在溶液中发生化学反应,“→”表示由某种物质可以转化为另一种物质(部分反应物、生成物及反应条件已略去,所涉及的化学反应均为初中化学学习中常见的反应) 请回答下列问题: (1)写出A物质的化学式①______,E物质的一种用途②________。 (2)写出C与F反应的化学方程式_________。 (3)①②③④⑤五个化学反应中,不属于基本反应类型的是___(填数字序号)。 |
|
| 20. | 详细信息 |
某化学兴趣小组的同学们想测定木炭还原氧化铜实验后所得固体(铜和氧化铜的混合物,以下简称为“混合物”)中氧化铜的含量,进行了如下实验。请回答问题: (1)上述实验过程中发生反应的化学方程式为___________。 (2)样品中氧化铜的含量为_______。 (3)根据已知条件列出求解150g稀盐酸中溶质质量(x)的比例式___________。 (4)若向最终所得滤液中加入46.5g水,所得不饱和溶液的溶质质量分数为___________。 (5)若将400g混合物还原,可得到金属铜的质量为___________。 |
|
| 21. | 详细信息 |
某学习小组的同学们在学习了酸、碱盐的相关性质后,做了如下实验,请与他们一起探究: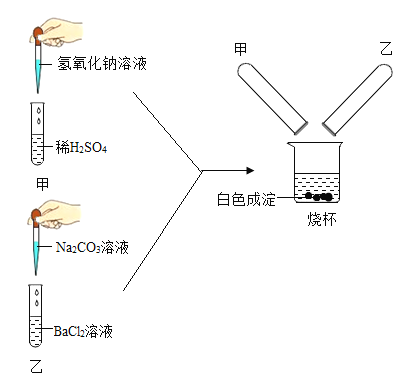 甲同学实验时发生反应的化学方程式为__________。 乙同学观察到的实验现象为____________。 实验结束后,甲、乙同学将试管中清液倒入同一烧杯中,发现产生白色沉淀,由此可知乙同学实验所得溶液中含有的溶质是_________(填化学式)。 [提出问题]烧杯内滤液中含有哪些离子呢? 同学们将烧杯中固液混合物分离,取滤液少许,向其中加入过量的碳酸钠溶液,无明显现象。 [假设与猜想]甲同学:Na+、Cl- 乙同学:Na+、Cl-、OH- 丙同学:Na+、Cl-、SO42-、Ba2+ [表达与交流]大家一致认为___________同学的猜想是错误的。理由是________。 [活动与探究]甲同学为了验证自己的猜想,取烧杯中滤液少许,加入无色酚酞溶液,没有观察到明显实验现象,于是认为自己的猜想正确。大家都认为甲同学的实验结论_______ (填“正确”或“不正确”)。同学们通过实验最终确定了滤液中的离子成分。 [反思与收获]由上述探究活动可知,当溶液中待测离子较多时,可以先加入试剂,根据_______排除一些猜想。当溶质组成只剩两种情况时,加人适当的试剂,证明______即可。 |
|
最近更新







