2019-2020年高二上学期期中考试化学考题同步训练(甘肃省兰州市联片办学)
| 1. 选择题 | 详细信息 |
|
已知反应X+Y=M+N为放热反应,对该反应的下列说法中正确的( ) A.X的能量一定高于M B.Y的能量一定高于N C.X和Y的总能量一定高于M和N的总能量 D.因该反应为放热反应,故不必加热就可发生反应 |
|
| 2. 选择题 | 详细信息 |
|
设C + CO2 A. υ1增大,υ2减小 B. 同时减小 C. 同时增大 D. υ1减小,υ2增大 |
|
| 3. 选择题 | 详细信息 |
|
反应A(g) + 3B(g) = 2C(g) + 2D(g)在四种不同情况下的反应速率分别为① v(A)=0.45 mol⋅L−1⋅s−1 ② v(B)=0.6 mol⋅L−1⋅s−1、③ v(C)=0.4 mol⋅L−1⋅s−1、④ v(D)=0.45 mol⋅L−1⋅s−1,该反应进行的快慢顺序为( ) A.① > ③ = ② > ④ B.① > ② > ③ = ④ C.② > ① = ④ > ③ D.① > ④ > ② = ③ |
|
| 4. 选择题 | 详细信息 |
|
可以充分说明反应P(g)+Q(g) A. 反应容器内的压强不随时间改变 B. 反应容器内P、Q、R、S四者浓度之比为1:1:1:1 C. P的生成速率和S的生成速率相等 D. 反应容器内的气体总物质的量不随时间变化 |
|
| 5. 选择题 | 详细信息 |
|
一定量的锌粉和6 mol/L的过量盐酸反应,当向其中加入少量的下列物质时,能够加快反应速率,又不影响产生H2的总量的是 ( ) ①石墨粉 ②CuO ③铜粉 ④铁粉 ⑤浓盐酸 A.①②⑤ B.①③⑤ C.③④⑤ D.①③ |
|
| 6. 选择题 | 详细信息 |
|
在N2+3H2 A.0.3 mol·L-1·s-1 B.0.4 mol·L-1·s-1 C.0.6 mol·L-1·s-1 D.0.8 mol·L-1·s-1 |
|
| 7. 选择题 | 详细信息 |
|
下列有关热化学方程式的表示及说法正确的是 ( ) A.已知c(石墨,s)=c(金刚石,s);△H>0,则石墨比金刚石稳定 B.若2C(s)+O2(g)=2CO(g) △H=−221.0 kJ/mol,则碳的燃烧热为110.5 kJ/mol C.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ba(OH)2反应的中和热△H=2×(-57.3)kJ/mol D.已知H2(g)+F2(g)=2HF(g);△H=-270kJ/mol,则2L氟化氢气体分解成1L氢气和1L氟气吸收270kJ热量 |
|
| 8. 选择题 | 详细信息 |
|
一定温度下,反应N2(g)+3H2(g) A. 2△H和2K B. -2△H和 K2 C. -2△H和 K-2 D. 2△H和-2K |
|
| 9. 选择题 | 详细信息 |
|
下列各组热化学方程式中ΔH前者大于后者的是 ( ) ①C(s)+O2(g)=CO2(g) ΔH1;C(s)+1/2O2(g)=CO(g) ΔH2。 ②S(s)+O2(g)=SO2(g) ΔH3;S(g)+O2(g)=SO2(g) ΔH4。 ③H2(g)+1/2O2(g)=H2O(g) ΔH5 ;2H2(g)+O2(g)=2H2O(g)ΔH6。 A.① B.② C.②③ D.①②③ |
|
| 10. 选择题 | 详细信息 |
在一定体积的密闭容器中,进行如下的化学反应CO2(g)+H2(g)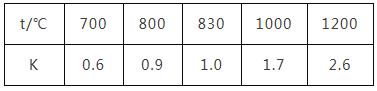 A.此反应为放热反应 B.此反应只有达到平衡时,密闭容器中的压强才不会变化 C.此反应达到1 000 ℃时的反应速率比700 ℃时大 D.该反应的化学平衡常数越大,反应物的转化率越低 |
|
| 11. 选择题 | 详细信息 |
|
在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g) A.加催化剂同时升高温度 B.加催化剂同时增大压强 C.升高温度同时充入N2 D.降低温度同时增大压强 |
|
| 12. 选择题 | 详细信息 |
|
对于可逆反应:2A(g)+B(g) A. 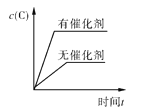 B. 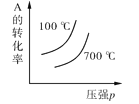 C. 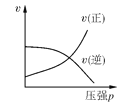 D. 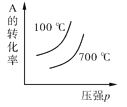 |
|
| 13. 计算题 | 详细信息 |
已知工业制氢气的反应为CO(g)+H2O(g) 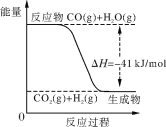 (1)增加H2O(g)的浓度,CO的转化率将________(填“增大”、“减小”或“不变”)。 (2)平衡常数的表达式K=________。400 ℃时平衡常数K______9(填“>”、“<” 或“=”)。 (3)已知2H2(g)+O2(g) |
|
| 14. 解答题 | 详细信息 |
|
将等物质的量的A、B、C、D 4种物质混合,发生如下反应:aA+bB (1)该化学方程式各物质的化学计量数为a=____、b=____、c=_____、d=____。 (2)若只改变压强,反应速率发生变化,但平衡不发生移动,该反应中各物质的聚集状态: A_________、B_______、D________。 (3)若只升高温度,反应一段时间后,测知4种物质其物质的量又达到相等,则该反应为______(填“放热”或“吸热”)反应。 |
|
| 15. 计算题 | 详细信息 |
|
(1)写出符合要求的一个反应: ①吸热的分解反应的化学方程式:______________________。 ②表示一类放热反应的离子方程式:____________________。 (2)化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知: N≡N键的键能是948.9 kJ·mol-1,H—H键的键能是436.0 kJ·mol-1;由N2和H2合成1 mol NH3时可放出46.2 kJ的热量。则N—H键的键能是_______。 (3)根据下列3个热化学反应方程式: Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH=-24.8 kJ·mol-1; 3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH=-47.2 kJ·mol-1; Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH=+640.5 kJ·mol-1。 写出CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式:_______ |
|
| 16. 计算题 | 详细信息 |
|
在一定温度下,10L密闭容器中加入5.0molSO2、4.5molO2,经10min后反应达平衡时O2的浓度为0.30mol/L。请计算(写出计算过程): (1)10min内SO2的转化率; (2)容器内反应前与平衡时的压强之比(最简整数比) ; (3)平衡常数K。 |
|
高中化学 试卷推荐
- 2017-2018年高二上学期期中考试化学在线测验(广东省深圳市高级中学)
- 2018年高考化学二轮专题复习 专题十四:实验综合(备考)
- 高中化学人教版 选修三 第3章 晶体结构与性质 金属键
- 2018届高三上学期第三次诊断考试理科综合-化学考题带答案和解析(山东省实验中学)
- 2017-2018年高一上半期期中考试化学在线测验(重庆市第一中学)
- 高中化学人教版 选修四 第三章 水溶液中的离子反应 第三节 盐类的水解 盐类的水解第二课时
- 2016-2017年高一前半期化学期中考试考试题(江西省南昌市八一中学、洪都中学、麻丘中学等六校联考)
- 2016-2017年高一上学期化学期中考试考试(广东省清远三中)
最近更新



