九年级化学下半年月考试卷附答案与解析(2019年福建)
| 1. 选择题 | 详细信息 |
|
端午节吃粽子是传统习俗,在制作粽子的过程中一定发生了化学变化的是 A. 水洗糯米 B. 刀切肉块 C. 粽叶包粽 D. 烧火煮粽 |
|
| 2. 选择题 | 详细信息 |
|
“水是生命之源、生产之要、生态之基”是2014年“中国水周”的宣传口号之一。下列关于水的认识不正确的是( ) A. 电解水可以得到氢气和氧气 B. 经过自来水厂处理过的水是纯水 C. 我国人均可利用淡水资源十分短缺 D. 水经过“三态”变化实现在自然界中的循环 |
|
| 3. 选择题 | 详细信息 |
|
下列实验方案中,设计合理的是( ) A. 分离木炭粉和氧化铜粉末:在空气中充分灼烧 B. 除去氨气中的水蒸气:通过盛有浓硫酸的洗气瓶 C. 检验氢氧化钠溶液是否变质:取样,滴加酚酞溶液 D. 鉴别双氧水和水:取样,加入少量二氧化锰 |
|
| 4. 选择题 | 详细信息 |
|
某同学制作的试剂标签如下,其中化学式书写不正确的是( ) A.  B. B.  C. C.  D. D.  |
|
| 5. 选择题 | 详细信息 |
|
永春芦柑被国外水果商称之为“东方佳果”。芦柑含有丰富的维生素C,其化学式为C6H8O6, 下列关于维生素C的说法,正确的是( ) A. 维生素C由四种元素组成 B. 一个维生素C分子中含碳、氢原子的个数比为4︰3 C. 维生素C的相对分子质量为186 D. 一个维生素C分子中含有20个原子 |
|
| 6. 选择题 | 详细信息 |
|
在含有Cu(NO3)2和AgNO3的混合溶液中加入一定量的锌粉,充分反应后过滤,滤液为无色,则下列说法中正确的是 ( ) A. 滤渣中一定有银,没有铜和锌 B. 滤渣中一定有银和铜,可能有锌 C. 滤液中一定有硝酸锌、硝酸铜 D. 滤液中一定有硝酸锌、硝酸铜、硝酸银 |
|
| 7. 选择题 | 详细信息 |
下图为甲乙两物质的溶解度曲线,下列说法正确的是( )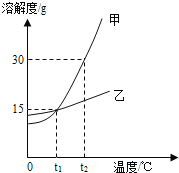 A. 甲的溶解度大于乙的溶解度 B. t1℃时,甲、乙两物质饱和溶液中溶质的质量分数均为15% C. t2℃时,将50克甲物质放入100克水中,得到溶液的质量为150克 D. 要使接近饱和的乙溶液转化为饱和溶液,可以采用降温的方法 |
|
| 8. 填空题 | 详细信息 |
|
生活与化学密切相关,处处充满着化学知识。 (1)化肥对农作物生长很重要,下列属于铵态氮肥的是_______(填标号)。 A NaNO3 B CO(NH2)2 C NH4Cl (2)下列物品中,所使用的主要材料属于复合材料的是_______(填标号)。 A 有机玻璃 B 钢筋混凝土 C 玻璃 D 铝合金 (3)净水器中用活性炭来除去水中的有色物质和异味,这是利用活性炭的_______。 (4)牛奶中含有_________元素(填名称),老年人长期饮用可以有效预防骨质疏松。 (5)生锈的铁钉可用酸洗,清洗后的溶液中含有铁离子____(填离子符号)。 (6) 用水壶烧开水时易产生水垢的水,属于______水。 (7)保险丝(铅锑合金)比组成它的纯金属的熔点______。(填“高”或者“低”)。 (8)用洗洁精除去油污,是由于洗洁精对油污有______作用。 (9)“吃得营养,吃出健康”,青少年宜多吃蔬菜水果,以保证________的摄入量。 (10)近几年,由于汽车数量急剧增加、工业快速发展等因素,致使化石燃料大量使用,对环境的影响也日益凸显。小红查阅资料后获知:科学家在积极寻找洁净的新能源过程中,发现了氨气燃烧能释放出大量的热且产物对环境没有污染,从能量变化角度看,“放出大量的热”是 __________能转化为热能。该反应的微观示意图如下,根据围观示意图写出该反应的化学方程式________________________,该反应中________是还原剂。 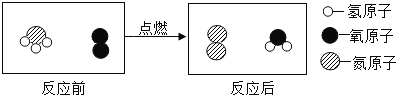 |
|
| 9. 填空题 | 详细信息 |
试依据核电荷数为1~18的元素的原子结构示意图,回答下列问题: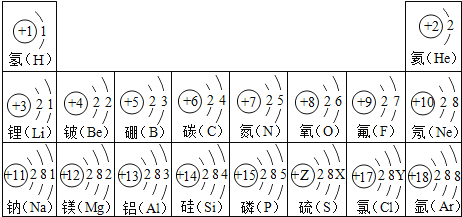 (1)上图中氯元素的最外层电子数Y=____(填数值),则与氯元素化学性质相似的元素是____。 (2)核电荷数为12的元素的原子失去两个电子后,形成的粒子的符号是______,与该粒子具有相同电子数的微粒有____________(填一种微粒符号)。 (3)上图中11、17号元素组成的化合物化学式为_____,该化合物中11号元素的化合价为______。 (4)上图的排列具有一定的规律,如:同一行中,从左到右元素的核电荷数依次增加。你还能找到哪些规律?试写出其中一个:________________________________ |
|
| 10. 推断题 | 详细信息 |
A﹣H都是初中化学常见物质.其中A、B的组成元素相同,且常温下都是无色液体;H是蓝色沉淀.X、Y都是氧化物,其中X是黑色粉末状固体,Y常用作食品干燥剂,Z是红色固体.它们之间有如图转化关系.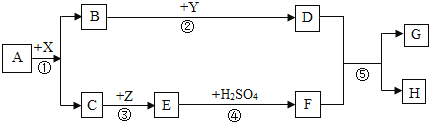 根据上述信息,回答下列问题: (1)写出A的化学式为 __________;H的化学式________;D的水溶液俗称 __________ 。 (2)反应⑤的化学方程式____________________,属于_________反应。(填基本类型) (3)反应①中X起______作用。Z的一种用途是______________________。 |
|
| 11. 实验探究题 | 详细信息 |
|
学习化学离不开实验:(化学方程式每个3分,其余每空1分) (1)写出图1装置中一种仪器的名称________,该仪器的用途有________________。 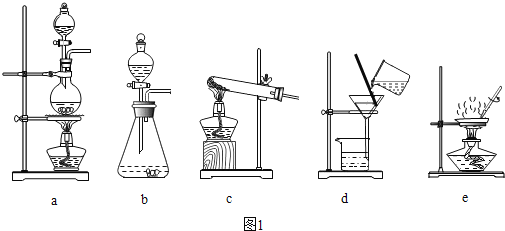 (2)小志同学用的高锰酸钾制氧气,应选用图1中的______装置,该图中的一处错误为________________,反应的化学方程式为_______________________。 (3)图2中用甲制取少量的二氧化碳,该装置的优点是___________,反应的化学方程式________。乙中某调味品可代替甲中某药品,请写出该调味品中能与鸡蛋壳发生反应的主要成分___________(填化学式)。用上述制取二氧化碳实验后的固液残留物进行过滤、蒸发的操作训练。 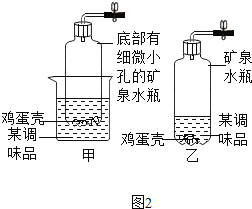 ① 对固液残留物进行过滤,应选择图1中_____(填标号)装置,过滤时玻璃棒的作用是____;② 取上述少量滤液进行蒸发,析出的固体中一定含有的物质是____________。 |
|
| 12. 综合题 | 详细信息 |
|
过碳酸钠(2Na2CO3•3H2O2,相对分子质量为314)是一种很好的消毒剂和供氧剂,常用于洗涤、印染、纺织、造纸、医药卫生等领域。 Ⅰ.制备过碳酸钠(查阅资料)过碳酸钠难溶于异丙醇,可浴于水,易发生反应2Na2CO3•3H2O2 =2Na2CO3+3H2O2;过氧化氢在温度较高时易发生分解。碳酸钠能与盐酸反应放出二氧化碳,也能与氯化钙溶液反应生成白色沉淀。 (制备流程)(图1) 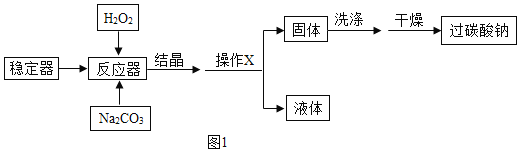 (1)操作X是________;请写出Na2CO3与H2O2化合生成过碳酸钠的化学方程式___________________________; (2)流程中结晶在常温下进行,原因是_______________________________; (3)为提高产品的纯度,碳酸钠和过氧化氢的最佳投料质量比是________,洗涤固体时,选用的最佳试剂是_______________ 。 (4)II.神奇的“氧立得” 小明同学新买了一台氧立得便携式制氧器,其中有A、B两包固体,经查阅资料知A包主要成分为过碳酸钠,B包为黑色固体粉未,将A包、B包药品分别放入机器,就可以制得氧气,在反应前后B的质量和化学性质不变,为探究A包固体的纯度,设计了如图2所示实验装置。 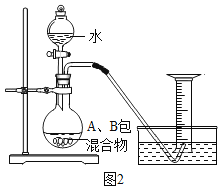 (实验步骤)①检查装置气密性;②称取2.2gA包药品和少许B包药品,并全部装入烧瓶内;③按图搭好装置;④现将橡胶管插入量筒底部;⑤打开分液漏斗;⑥待反应停止后,保持橡胶管口在量筒底部;⑦等试管冷却到室温时将橡胶管移出水槽,读取量筒读数为220mL;⑧数据处理。[氧气在实验条件下密度为1.43g/L] (问题讨论)B固体成分为________(填化学式),实验时烧瓶内可观察到的现象是________ (5)如果将步骤④和⑤对调,实验结果将________(选填“偏大”、“偏小”或“不变”),理由是____________________________; (6)证明反应停止后烧瓶中有碳酸钠的方法是取样加入_______,有白色沉淀产生,反应的化学方程式___________________________; (7)此样品中过碳酸钠的质量分数为_________________。 |
|
| 13. 实验探究题 | 详细信息 |
|
某同学在做“硫在氧气中燃烧”的实验时,为了防止空气污染,用氢氧化钠溶液来吸收二氧化硫。下面是该同学实验与计算过程: (1)配制100g溶质质量分数为10%的氢氧化钠溶液,需用天平称取______g的氢氧化钠;配制上述溶液,可用20%氢氧化钠溶液______g加水稀释。 (2)如下图所示,硫燃烧后,注入所配制的NaOH溶液吸收二氧化硫。若集气瓶中生成0.64g的二氧化硫,将其完全吸收,针筒要吸取的氢氧化钠溶液中含氢氧化钠___克。(假设NaOH溶液吸收SO2 时只发生如下反应:SO2+2NaOH=Na2SO3+H2O) 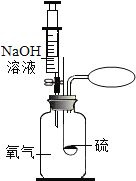 |
|
最近更新



