九年级化学(2018年下册)网上考试练习
| 1. 选择题 | 详细信息 |
|
下列制作过程中的变化属于化学变化的是 A.海水晒盐 B.风力发电 C.煤的干馏 D.纺纱织布 |
|
| 2. 选择题 | 详细信息 |
|
2017年世界环保日的主题是“人人参与,创建绿色家园”。与该主题相符的是 A.鼓励露天焚烧塑料袋减少白色污染 B.鼓励骑共享单车绿色出行 C.鼓励大量使用化肥增加产量 D.鼓励使用一次性筷子干净卫生 |
|
| 3. 选择填空题 | 详细信息 |
|
正确的实验操作是实验成功的关键,下列实验操作错误的是 A. 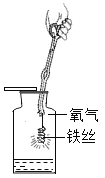 铁丝燃烧 B. 铁丝燃烧 B. 闻气体的气味 C. 闻气体的气味 C. 蒸发食盐水 D. 蒸发食盐水 D.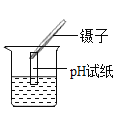 测溶液的pH值 测溶液的pH值 |
|
| 4. 选择题 | 详细信息 |
|
分子、原子、离子都是构成物质的微粒,下列物质都是由原子构成的一组是 A.金刚石、晶体硅 B.硫酸铜、干冰 C.氯化钠、汞 D.水、液氮 |
|
| 5. 选择题 | 详细信息 |
|
开封灌汤包被誉为“中州膳食一绝”,制作灌汤包的原料有瘦肉、面粉、麻油、食盐等,其中富含蛋白质的是 A.瘦肉 B.面粉 C.麻油 D.食盐 |
|
| 6. 选择题 | 详细信息 |
|
下列关于水的说法正确的是 A.过滤能将硬水转化为软水 B.纯净水是指不含任何化学物质的水 C.活性炭可除去水中的异味 D.电解水是一种常用的净水方法 |
|
| 7. 选择题 | 详细信息 |
|
分类法是学习化学的重要方法,下列分类正确的是 A.黄铜和黄金都是合金 B.烧碱和纯碱都是碱 C.酒精和碳酸钠都是有机物 D.塑料和合成橡胶都是合成材料 |
|
| 8. 选择题 | 详细信息 |
|
有化合价升降的反应是氧化还原反应。下列一定不是氧化还原反应的是 ( ) A.化合反应 B.分解反应 C.置换反应 D.复分解反应 |
|
| 9. 选择题 | 详细信息 |
|
某无色溶液中主要含有五种离子,己知其中四种为OH-、SO42-、CO32-、NO3-,则另一种离子可能是 A.NH4+ B.K+ C.Cu2+ D.Cl- |
|
| 10. 选择题 | 详细信息 |
甲、乙、丙三种物质的溶解度曲线如图所示,下列说法正确的是 A.丙的溶解度一定小于乙的溶解度 B.将t2℃甲、乙的饱和溶液降温到t1℃,析出固体的质量甲>乙 C.分离甲中混有的少量的丙可采用降温结晶的方法 D.t3℃时,50g水中加入50g的甲物质充分溶解后可得到100g甲的饱和溶液 |
|
| 11. 选择题 | 详细信息 | |||||||||||||||
密闭容器内有a、b、c、d四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表所示,下列说法正确的是
|
||||||||||||||||
| 12. 填空题 | 详细信息 |
|
钼酸铵((NH4)2MoO4)常用来测定水中磷元素的含量,关于它的说法正确的是 A.钼酸铵是氧化物 B.钼酸铵是由四种元素组成的 C.钼酸铵中含有15个原子 D.钼酸铵中含有两个氧分子 |
|
| 13. 选择题 | 详细信息 | |||||||||||||||
在一定质量的甲溶液中逐渐加入乙至过量,反应过程中溶液的总质量与加入乙的质量关系,能用如图图像表示的是
|
||||||||||||||||
| 14. 选择题 | 详细信息 |
|
将17.6g含有CuO、ZnO、Al2O3、Fe3O4四种氧化物的混合物放入烧杯中,加入足量的稀盐酸,充分反应后生成水的质量为5.4g,则固体混合物中金属元素的总质量为 A.12.8g B.9.6g C.4.8g D.无法确定 |
|
| 15. 填空题 | 详细信息 |
| 保持氦气的化学性质的最小粒子是______________(写化学式),茶壶中的水垢用厨房中的__________(写化学式)来除,人体缺乏维生素A会患________。 | |
| 16. 填空题 | 详细信息 |
| 生活中处处有化学,化学与生活密切相关。米多奇雪米饼包装袋中用生石灰作干燥剂,请用化学方程式表示其原理______________;我们常用__________来鉴别硬水和软水;炒菜时油锅着火用锅盖盖灭,其灭火原理是______________。 | |
| 17. 填空题 | 详细信息 |
如图为溴的原子结构示意图。请回答:溴元素位于元素周期表的第_____周期,溴元素与钙元素形成的化合物的化学式是______。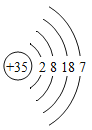 |
|
| 18. 填空题 | 详细信息 |
| 乙醇是一种重要的燃料,它燃烧的化学方程式是______________,与化石燃料相比,乙醇作为燃料的优点是_____________。 | |
| 19. 实验探究题 | 详细信息 |
如图是微型实验常用的“W”型玻璃管,在a处体现了CO的_________性,b处反应的化学方程式_________________,你认为该微型装置的优点是______________。 |
|
| 20. 推断题 | 详细信息 |
A、B、C、D、E是初中化学常见的物质,B是空气中含量第二位的物质,C是年产量最高的金属,D的浓溶液常作某些气体的干燥剂,其相互反应情况如图所示(“—”表示相连的物质能发生反应,“→”表示一种物质能生成另一种物质)。请回答: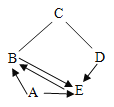 (1)写出A的化学式_______________________; (2)简述把D的浓溶液变成稀溶液的方法_____________________________。 (3)C与D的稀溶液反应的化学方程式是____________________________。 |
|
| 21. 实验探究题 | 详细信息 |
燃烧是生活中常见的一种现象。 (1)如图中能说明温度达到可燃物的着火点是燃烧的条件之一的现象是?__________。 (2)小明在实验结束后发现铜片变黑了,原因是什么?________________。 |
|
| 22. 填空题 | 详细信息 |
|
用所学化学知识解释下列问题。 (1)用微观的观点解释:10mL酒精和10mL水混合后体积小于20mL。____________。 (2)用化学方程式表示:将黑色氧化铜粉末装入试管中加热,通入氨气(NH3),可以得到红色的铜、水和一种气体单质。____________。 |
|
| 23. 简答题 | 详细信息 |
| 小丽在实验室发现了三瓶失去标签的化肥,分别是尿素、硝酸铵和氯化铵,请你设计实验帮她鉴别这三种化肥(写出步骤、现象和结论)。____________________。 | |
| 24. 流程题 | 详细信息 |
粗盐中含有少量不溶性杂质(泥沙),还含有少量可溶性杂质(CaCl2、MgCl2、Na2SO4),现以粗盐为原料制取精盐,生产流程如图所示: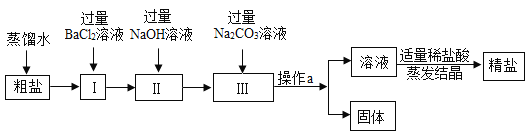 (1)在操作a中需要使用三种玻璃仪器,分别是__________________________? (2)请写出反应I的化学方程式__________________________。 (3)加入过量Na2CO3溶液的目的是为了除去__________________离子? |
|
| 25. 综合题 | 详细信息 |
|
金属用途十分广泛,牢固掌握金属的知识很有必要。 (1)下列关于金属的说法中不正确的是___________ A大多数金属都是银白色的 B铁是地壳中含量最高的金属 C金的活动性比较弱 D水银在常温下是液体 (2)“曾青得铁则化为铜”是炼铜的原理,请用化学方程式表示其原理_____________。 (3)铝在金属活动性顺序中位于氢前面,可小林发现铝与稀盐酸开始反应时,铝表面几乎没有气泡产生。请分析产生该现象的原因并写出相关的化学方程式______________。 (4)在Mg(NO3)2和Cu(NO3)2的混合溶液中加入质量为a g的Zn粉和Fe粉,充分反应后过滤,将滤渣洗净、干燥后称量,质量仍为a g。同学们对滤渣的成分做出猜想:猜想①:Cu;猜想②:Fe、Cu;猜想③:Zn、Fe、Cu (交流讨论)同学们一致认为猜想_____________不成立,理由是:____________________。 (5)铜的金属活动性虽然位于氢之后,但资料中显示铜可以和稀硝酸反应,其化学方程式为3Cu+8HNO3=3Cu(NO3)2+4H2O+2M,则M的化学式为____________。 (6)现将1.92g铜加到50g稀硝酸中,恰好完全反应,求稀硝酸中溶质的质量分数_____________。 |
|
最近更新



