2017-2018年高一12月联考化学在线测验(辽宁省东港二中、瓦房店高级中学等四校)
| 1. | 详细信息 |
|
化学与科学、技术、社会、环境密切相关,下列有关说法中错误的( ) A. 春节燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 B. 为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰 C. 小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂 D. 青铜是我国使用最早的合金材料,目前世界上使用量最大的合金材料是钢铁 |
|
| 2. | 详细信息 |
|
小明是高一学生,他的化学笔记中记录有如下内容: ①摩尔质量在数值上一定等于该物质的相对分子质量 ②静电除尘和明矾净水都应用了胶体的性质 ③氧化还原反应的本质是化合价升降 ④按照树状分类法可将化学反应分为:氧化还原反应和离子反应 你认为他的笔记中记录正确的是( ) A. ① B. ② C. ③ D. ④ |
|
| 3. | 详细信息 |
|
常温下,下列各组离子在指定溶液中一定能大量共存的是( ) A. 在透明溶液中:Cu2+、K+、SO42?、CO32? B. 在强碱性溶液中:K+、Na+、CO32?、AlO2? C. 在盐酸溶液中:K+、Fe2+、SO42?、NO3? D. 与铝反应产生氢气的溶液中:Na+、K+、HCO3?、Cl? |
|
| 4. | 详细信息 |
|
下列有关元素及其化合物的说法正确的是( ) A. Al(OH)3 具有两性,所以不能用于中和胃酸 B. FeCl3 既能通过化合反应制得,也能通过金属与酸的置换反应制得 C. Na 在空气中长期放置最终变为 Na2CO3 粉末 D. 等质量NaHCO3和Na2CO3分别与足量盐酸反应,生成的CO2在同温同压下体积相同 |
|
| 5. | 详细信息 |
|
下列有关元素及其化合物的说法正确的是( ) A. 将水蒸气通过灼热的铁粉,粉末变为红棕色 B. Al2O3熔点高,可用作耐高温材料 C. 无水CuSO4 可用于干燥实验室制备的氢气 D. 制备Fe(OH)2时,为了隔绝空气可以向FeSO4溶液加少量的酒精 |
|
| 6. | 详细信息 |
|
下列说法正确的是:( ) A. 向某溶液中加稀盐酸,将产生的无色无味的气体通入澄清石灰水中,石灰水变浑浊,则可以确定原溶液中一定有CO32? B. 根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和悬浊液 C. 向氯化钙溶液和澄清石灰水中分别通入少量CO2,都会出现白色沉淀 D. 向红褐色的氢氧化铁胶体中滴加稀盐酸的现象是:先沉淀,后沉淀溶解 |
|
| 7. | 详细信息 |
|
下列表示对应化学反应的离子方程式正确的是( ) A. 向FeCl3溶液中加入几滴KSCN溶液:3SCN? + Fe3+ ?Fe(SCN)3 ↓ B. AlCl3溶液中加入过量的浓氨水:Al3++4NH3?H2O?AlO2?+4NH4++2H2O C. 大理石溶于醋酸中的反应:CaCO3+2H+?Ca2++H2O+CO2↑ D. 钠与水反应: 2Na+2H2O?2Na++2OH?+H2↑ |
|
| 8. | 详细信息 |
|
下列说法正确的是:( ) A. 向饱和Na2CO3溶液中通入足量的CO2气体,无明显现象 B. 在酒精灯上加热铝箔,铝箔熔化,失去光泽,熔化的铝滴落下来 C. 次磷酸钠(NaH2PO2)是次磷酸与过量氢氧化钠反应的产物,是一种酸式盐 D. 加热放在坩埚中的小块钠,钠先熔化成光亮的小球,燃烧时火焰为黄色,燃烧后生成淡黄色固体 |
|
| 9. | 详细信息 |
下列实验能达到实验目的且符合安全要求的是( )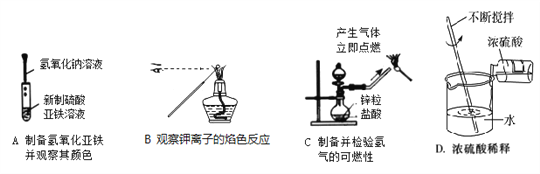 A. A B. B C. C D. D |
|
| 10. | 详细信息 |
|
宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载;“银针验毒”的原理是4Ag+2H2S+O2=2X+2H2O;下列说法正确的是( ) A. X的化学式为AgS B. 银针验毒时,空气中氧气失去电子 C. 反应中Ag和H2S均是还原剂 D. 每生成1mol X,反应转移2mol e- |
|
| 11. | 详细信息 |
饮茶是中国人的传统饮食文化之一.为方便饮用,可通过以下方法制取罐装饮料茶: 关于上述过程涉及的实验方法、实验操作和物质作用中说法不正确的是( ) A. ①是萃取 B. ②是过滤 C. ③是分液 D. 维生素C可作抗氧化剂 |
|
| 12. | 详细信息 |
|
已知在碱性溶液中可发生如下反应:2R(OH)3 + 3C1O-+ 4OH- = 2RO4n-+3Cl- +5H2O。关于该反应的说法正确的是( ) A. RO4n-中 R 的化合价是+6 B. ClO?是还原剂 C. 由上述离子方程式可知,该反应是由氨水提供的碱性环境 D. 反应过程中生成1mol RO4n-,转移6mol e-。 |
|
| 13. | 详细信息 |
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如右图所示。则下列离子组在对应的溶液中一定能大量共存的是 A. a点对应的溶液中:Na+、OH-、SO42-、NO3- B. b点对应的溶液中:H+、Fe3+、MnO4-、Cl- C. c点对应的溶液中:Na+、Ca2+、NO3-、Cl- D. d点对应的溶液中:S2-、NO3-、Fe2+、Ag+ |
|
| 14. | 详细信息 |
|
某同学参阅了“84消毒液”说明中的配方,欲用NaClO固体配制480mL含NaClO 25%,密度为1.19g/cm3的消毒液.下列说法正确的是 A. 配制过程只需要三种仪器即可完成 B. 容量瓶用蒸馏水洗净后必须烘干才能用于溶液的配制 C. 定容时俯视容量瓶的刻度线,会造成所配溶液物质的量浓度偏低 D. 需用托盘天平称量的NaClO固体的质量为148.8 g |
|
| 15. | 详细信息 | |||||||||||||||||||||||||
下表各组物质中,物质之间不可能实现如下图所示转化的是( )
|
||||||||||||||||||||||||||
| 16. | 详细信息 |
|
向100mL 1mol/LCa(HCO3)2溶液中投入Na,当沉淀最大量时,至少需要Na的质量是(? )g A. 2.3 B. 4.6 C. 1.15 D. 4 |
|
| 17. | 详细信息 |
|
在一定条件下,下列微粒的还原性顺序为SO2>I->Fe2+>Cl-,由此判断以下各反应在溶液中不能发生的是( ) A. 2Fe2++I2 B. I2+SO2+2H2O C. 2Fe3++SO2+2H2O D. Cl2+2I- |
|
| 18. | 详细信息 | |||||||||||||||
将物质X逐渐加入(或通入)Y溶液中,生成沉淀的量与加入X的物质的量关系如图所示,符合图示情况的是( )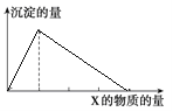
|
||||||||||||||||
| 19. | 详细信息 |
一块表面被氧化的铝分成两等分,若向其中一份中滴加1mol?L-1的NaOH溶液,向另一份中滴加x mol?L-1的稀盐酸,产生氢气的物质的量与所加NaOH溶液、稀盐酸的体积关系如图所示.下列说法不正确的是( ) A. a=260 B. x=1mol/L C. 该铝块的总质量为8.46g D. 该铝块中氧化铝与铝单质的物质的量之比为3:20 |
|
| 20. | 详细信息 |
|
(1)现有下列十种物质:①蔗糖②熔融NaCl③石墨④铜丝⑤NaOH固体⑥SO2⑦NaHSO4固体⑧K2O固体⑨液态H2SO4⑩饱和FeCl3溶液? 上述物质中可导电的是________(填序号,下同);上述物质中不能导电,但属于电解质的是_______________________。 (2)NaHSO4是一种酸式盐,请填写下列空白: ①NaHSO4晶体熔化时的电离方程式为______________________________。 ②3 mol?L-1 NaHSO4与2 mol?L-1 Ba(OH)2溶液等体积混合,该反应总的离子方程为___________。 (3)实验室制备少量Fe(OH)3胶体所用的物质有__________(填序号),反应的离子方程式为________________________________________________。 (4)某强酸性反应体系中,反应物和生成物共六种物质:O2、MnO4-、H2O、Mn2+、H2O2、H+,已知该反应中H2O2只发生了如下过程:H2O2→O2。写出该反应的离子方程式:_________________________。 |
|
| 21. | 详细信息 |
从某含有FeCl2、FeCl3、CuCl2的工业废液中回收铜并制备氯化铁晶体的流程如下: 已知:FeCl3在加热情况下与水反应生成Fe(OH)3。 回答下列问题: (1)试剂a是 ____________,过量的原因______________________。 (2)操作Ⅱ是___________,用到的玻璃仪器___________________________。 (3)若试剂C是Cl2,则反应的离子方程式: __________________________。 (4)滤液X、Z中都有同一种溶质,请设计实验验证该溶质的离子:___________。 (5)操作Ⅲ应该是(______) A 蒸发 B蒸馏 C 分液 D 结晶 |
|
| 22. | 详细信息 |
某课外活动小组模拟呼吸面具中的原理(过氧化钠与潮湿二氧化碳反应),设计用下图所示的仪器来制取氧气并测量氧气的体积。图中E为量气装置。 本实验可供选用的药品还有:稀硫酸、稀盐酸、过氧化钠、大理石、水。 试回答: (1)图中装置的连接顺序是(填装置的字母编号),其中连接胶管及支持装置省略:_________。 (2)装置C中放入的反应物是________和_________________。(写化学式) (3)装置A的作用是__________________;装置B的作用是_______________。 (4)装置D中发生的化学反应方程式为__________________________。 (5)为了较准确地测量氧气的体积,除了必须检查整个装置的气密性之外,在读反应前后甲管中液面的读数求其差值的过程中,应注意_____________。 a.视线与凹液面最低处相平 b.等待片刻,待乙管中液面不再上升时,立刻读数。 c.读数时应上下移动乙管,使甲、乙两管液面相平。 d.读数时不一定使甲、乙两管液面相平。 |
|
最近更新



