2018届高三上学期教学质量检测理科化学考试题(江西省抚州市临川区第一中学)
| 1. | 详细信息 |
|
生括高不开化学。某种金属制成的器皿,放置于空气中,其表面会逐渐交黑,如将表面变黑的上述器皿放入盛有食盐水的铝制容器中浸泡,一段时间后,黑色完全褪去。下列成语与该金属有关的是 A. 衣紫腰银 B. 点石成金 C. 铜驼荆棘 D. 铁杵成针 |
|
| 2. | 详细信息 |
|
NA表示阿伏加德罗常数的值。俗名为“臭碱”的硫化钠应用于冶金、燃料,皮革,电镀等工业。硫化钠的一种制备方法是Na2SO4+2C A. 1mol/LNa2SO4溶液中含氧原于的数目一定大于4NA B. 1L0.1mol/LNa2S溶液中含阴离子的数目小于0.1NA C. 生成1mol氧化产物时转移电子数为4NA D. 通常状况下,11.2LCO2中含质子的数目为11NA |
|
| 3. | 详细信息 |
某学习小组设计实验探究NO与铜粉的反应并检验NO,实验装置如图所示(夹持装置略)。实验开始前,向装置中通入一段时间的N2,排尽装置内的空气。 已知:在溶液中.FeSO4+NO A. 装置F、I中的试剂依次为水、硫酸亚铁溶液 B. 若观察到装置H中红色粉末变黑色,则NO与Cu发生了反应 C. 实验结束后,先熄灭酒精灯,再关闭分液漏斗的活塞 D. 装置J收集的气体中一定不含NO |
|
| 4. | 详细信息 |
某药物R的结构如图所示。下列说法不正确的是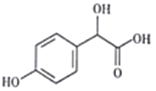 A. R含有的官能团是羧基、羟基 B. R能发生取代反应、加成反应、氧化反应 C. 用金属钠可以检验R分子中的羟基 D. R分子中至少有7个碳原子共平面 |
|
| 5. | 详细信息 |
如图为镁-间二硝基苯电池的工作原理示意图。已知:电池放电时,铁转化为氢氧化镁,间二硝基苯则转化为间苯二胺。下列说法不正确的是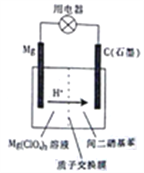 A. 电池放电时,电子由镁电极流出经过用电器流向石墨电极 B. 电池放电时,镁电极附近的电解质溶液的pH降低 C. 电池放电时,理论上每生成1mol间苯二胺就有12molH+通过质子交换膜 D. 电池放电时,石墨电板上发生的反应为  +12H+-12e-= +12H+-12e-=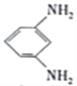 +4H2O +4H2O |
|
| 6. | 详细信息 |
短周期元素a、b、c、d的原子序数依次增大,b和c为两种常见的金属元素,a、b、c、d的最高价氧化物对应的水化物依次为甲、乙、丙、丁,它们之间存在如图所示的反应关系(图中用“--“相连的两种物质间能发生反应)。下列判断一定正确的是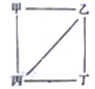 A. 简单离子半径:d>b>c>a B. 等物质的量的ba3、b3a所含离子总数不相等 C. d的最高化合价和最低化合价的代数和为6 D. b和d组成的化合物的水溶液是中性 |
|
| 7. | 详细信息 |
已知298K时,某碱MOH的电离平衡常数Kb=1.0×10-5;电离度a= A. a点对应的溶液中:c(OH-)=(M+)+<(H+) B. b点对应的V。=20.00mL C. 298K时,0.1000mol/LMOH溶液中,MOH的电离度a=1% D. 298K时,将0.1molMOH和0.1moMCl溶于水配制成1L混合溶液,溶液的pH>9 |
|
| 8. | 详细信息 |
|
氧、硫、硒、碲都位于元素周期表的VIA族,其化合物在化工生产中有广泛应用。 (1)下列性质的递变顺序不正确的是_____(填字母)。 A.酸性:H2SeO4>H2SeO3 B.非金属性:O>S>Se>Te C.还原性:H2Te>H2Se>H2S>H2O D.热稳定性:H2O>H2Te>H2Se>H2S E.沸点: H2Te>H2Se>H2S>H2O (2)在常温下进行的置换反应X+W→Y+V中, H2O可以扮演不同的“角色”。已知X、Y是短周期主族元素形成的单质,W、V是化合物。 ①若W是水,且作还原剂,反应的化学方程式为_________。 ②若V是水,为还原产物,反应的化学方程式为_____________。 (3) ①一定温度下,向恒容密闭容器中充入一定量的H2S,发生反应H2S(g) A.混合气体的密度不再变化 B.混合气体的压强不再变化 C. ②已知:液态CS2完全燃烧生成CO2、SO2气体,每转移3mol电子时放出269.2kJ热量。写出表示CS2(1)的燃烧热的热化学方程式:______________。 (4) ①工业上,用S02还原TeC14溶液制备碲(Te),反应中氧化产物与还原产物的物质的量之比为____________。 ②以石墨为电极,电解强碱性Na2TeO3溶液也可获得碲,电解过程中阴极的电极反应式为_____;阳极产生的气体是_____ (填化学式)。 |
|
| 9. | 详细信息 |
|
氢化铝锂(LiAlH4)是有机合成中的重要还原剂。某课题组设计实验制备氢化铝锂并测定其纯度。已知: 氢化铝锂、氢化锂遇水都剧烈反应并产生同一种气体。 I.制备氢化锂 选择图I中的装置制备氢化锂(有些装置可重复使用):  (1)装置的连接顺序(从左至右)为A→______________。 (2)检在好装蹬装置的气密性,点燃酒精灯前需进行的实验操作是_______________。 (3)写出制备氢化铝锂的化学方程式:__________________。 II. 制备氢化铝锂 1947年,Schlesinger,Bond和Finholt首次制得氢化铝锂,其方法是使氢化锂与无水三氯化铝按一定比例在乙醚中混合,搅样,充分反应后,经一系列操作得到LiAlH4晶体。 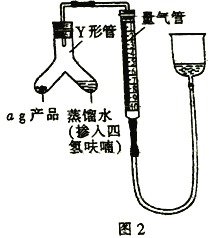 (4)写出氢化锂与无水三氯化铝反应的化学方程式:____________________。 III.测定氢化铝锂产品(不含氢化锂)的纯度 (5)按图2装配仪器、检查装置气密性并装好药品(Y形管中的蒸馏水足量,为了避免氢化铝锂遇水发生爆炸,蒸馏水中需掺入四氢呋喃作稀释剂),启动反应的操作是________。读数之前上下移动量气管右侧的容器,使量气管左、右有两侧的液面在同一水平面上,其目的是_________。 (6)在标准状况下,反应前量气管读数为V1 mL,反应完毕并冷却之后,量气管读数为V2 mL。该样品的纯度为_____________(用含a、V1、V2 的代数式表示)。如果起始读数时俯视刻度线,测得的结果将________(填“偏高”“偏低”或“无影响”)。 |
|
| 10. | 详细信息 |
|
为了缓解温室效应,科学家提出了多种回收和利用CO2 的方案。 方案I:利用FeO吸收CO2 获得H2 ?.6FeO(s) +CO2(g)=--2Fe3O4(s) +C(s) △H1=-76.0kJ/mol ?.C(s) +2H2O(g)=CO2(g) +2H2(g) △H2= +113.4kJ/mol (1)3FeO(s) +H2O(g)=Fe3O4(s) +H2(g) △H3=________。 (2)在反应i中,每放出38.0kJ热量,有_______g FeO 被氧化。 方案II :利用CO2 制备CH4 300℃时,向2L恒容密闭容器中充入2molCO2 和8 mol H2,发生反应:CO2(g) +4H2(g)  (3) ①从反应开始到恰好达到平衡时,H2 的平均反应速率v(H2) =_________。 ②300℃时,反应的平衡常数K=____________。 ③保持温度不变,向平衡后的容器中再充入2 molCO2和8 molH2,重新达到平衡时CH4 的浓度_________(填字母)。 A.等于0.8mol/L B.等于1.6 mol/L C.0.8 mol/L <c(CH4) <1.6 mol/L D.大于1.6 mol/L (4)300℃时,如果该容器中有1.6 molCO2、2.0molH2、5.6molCH4、4.0molH2O(g),则v正____v逆(填“>”“<”或“=”)。 (5)已知:200℃时,该反应的平衡常数K=64.8L2?mol-2。则△H4______0(填“>”“<”或“=”)。 方案Ⅲ:用碱溶液吸收CO2 利用100mL3mol/LNaOH溶液吸收4.48LCO2(标准状况),得到吸收液。 (6)该吸收液中离子浓度的大小排序为______________。将该吸收液蒸干、灼烧至恒重,所得固体的成分是__________(填化学式)。 |
|
| 11. | 详细信息 | ||||||||||
工业上采用氯化铵焙烧菱锰矿制备高纯度碳酸锰,工艺流程如下: 己知相关信息如下: ①菱猛矿的主要成分是MnCO3,还含少量Fe、Al、Ca、Mg等元素。 ②氢氧化物沉淀的条件:Al3+、Fe3+完全沉淀的pH分别为4.7、3 2;Mn2+、Mg2+开始沉淀的pH分别为8.1、9.1。 ③“焙烧”过程的主要反应MnCO3+2NH4Cl=MnCl2+2NH3↑+CO2↑+H2O。 ④常温下,几种难溶物的Ksp如下表所示:
|
|||||||||||