2017-2018年高一12月月考化学考试(宁夏育才中学勤行校区)
| 1. | 详细信息 |
|
将30 mL 0.5mol/L的NaOH溶液加水稀释到500 mL,稀释后NaOH的物质的量浓度为? ( ) A. 0.3 mol/L B. 0.03 mol/L C. 0.05 mol/L D. 0.04 mol/L |
|
| 2. | 详细信息 |
|
在过滤操作中,除了使用铁架台、烧杯、玻璃棒外,还需要用到的仪器是( ) A. 漏斗 B. 蒸发皿 C. 酒精灯 D. 天平 |
|
| 3. | 详细信息 |
|
做化学实验时必须注意安全,下列说法中不正确的是( ) A. 点燃氢气气体前,必须先检验它的纯度 B. 酒精灯洒出的酒精在桌上着火,应立即用湿抹布盖灭 C. 在实验室里,不能尝任何药品的味道 D. 碱溶液沾到皮肤上,应立即用抹布擦拭干净,再涂上稀盐酸 |
|
| 4. | 详细信息 |
|
某气体物质的质量为6.4g,含有6.02×1022个分子,则该气体的相对分子质量是( ) A. 32 B. 64 C. 64g?mol-1 D. 32g?mol-1 |
|
| 5. | 详细信息 |
|
下列物质的盛放不正确的是( ) A. 烧碱必须密封保存 B. 浓硝酸保存在细口棕色试剂瓶中 C. 金属钠保存在煤油中 D. 氢氧化钠溶液用带玻璃塞的试剂瓶存放 |
|
| 6. | 详细信息 |
|
分液漏斗是把密度不同且互不相溶的液体分离的仪器。下列各组物质中,能用分液漏斗进行分离的是 A.四氯化碳和液溴 B.汽油和花生油 C.苯和食盐水? D.酒精和水 |
|
| 7. | 详细信息 |
|
下列实验操作中,正确的是( ) A. 为使过滤速率加快,可用玻璃棒在过滤器中轻轻搅拌,加速液体流动 B. 用酒精灯给试管加热时,要将被加热的试管放在酒精灯火焰的外焰上 C. 为加速固体物质的溶解只能采用加热的方法 D. 为增大气体物质的溶解度,常采取搅拌、加热等措施 |
|
| 8. | 详细信息 |
|
1mol O2和1mol O3相比较,下列叙述一定正确的是 ( ) A. 体积相同 B. 质量相等 C. 原子数相等 D. 分子数相等 |
|
| 9. | 详细信息 |
|
下列实验操作中错误的是 ( ) A. 熄灭酒精灯时用灯帽盖灭 B. 用药匙或者纸槽把粉末状药品送入试管的底部 C. 如果没有试管夹,可以临时手持试管给固体或液体加热 D. 过滤时玻璃棒的末端应轻轻靠在三层的滤纸上 |
|
| 10. | 详细信息 | ||||||||||||||||||
除去下列物质中所含的杂质,选用的试剂正确的是( )
|
|||||||||||||||||||
| 11. | 详细信息 |
|
用NA表示阿伏加德罗常数,下列叙述正确的是( ) A. 64 g SO2含有氧原子数为1NA B. 物质的量浓度为0.5 mol?L-1的MgCl2溶液,含有Cl-数为1 NA C. 标准状况下,22.4 L H2O的分子数为1NA D. 常温常压下,14 g N2含有分子数为0.5 NA |
|
| 12. | 详细信息 |
|
下列常见物质的俗名与化学式对应正确的是 A. 烧碱?NaOH B. 小苏打?Na2SO4 C. 熟石灰?CaCl2 D. 明矾?Al2(SO4)3 |
|
| 13. | 详细信息 |
|
下列物质的水溶液能导电,但属于非电解质的是( ) A. CH3COOH B. SO2 C. (NH4)2CO3 D. Cl2 |
|
| 14. | 详细信息 |
|
下列关于电解质的说法正确的是 A.液态HCl不导电,所以HCl不是电解质 B.NH3溶于水形成的溶液能导电,所以NH3是电解质 C.稀硫酸能导电,所以稀硫酸是电解质 D.BaSO4在水溶液中难导电,但熔融状态下能导电,所以BaSO4是电解质 |
|
| 15. | 详细信息 |
|
下列各组离子一定能大量共存的是 A. 某无色透明的酸性溶液:Cl-、Na+、MnO4-、SO42- B. 能使pH试纸变深蓝色的溶液:Na+、NH4+、K+、CO32- C. 加入过量NaOH溶液后可得到澄清的溶液:K+、Ba2+、HCO3-、Cl- D. 常温下pH=12的溶液: K+、Ba2+、Cl-、NO3- |
|
| 16. | 详细信息 |
|
能正确表示下列反应的离子方程式是( ) A. 浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑ B. 氢氧化钠溶液吸收少量CO2气体:CO2+2OH-=CO32-+H2O C. NaHCO3溶液与稀H2SO4反应:CO32-+2H+=H2O+CO2↑ D. 钠与CuSO4溶液反应:2Na+Cu2+=Cu↓+2Na+ |
|
| 17. | 详细信息 |
|
用光洁铂丝蘸取某无色溶液在无色火焰上灼烧,直接观察到火焰呈黄色。下列判断正确的是 A. 只含有Na+ B. 一定含有Na+,可能含K+ C. 既含有Na+,又含K+ D. 可能含有Na+,可能含有K+ |
|
| 18. | 详细信息 |
|
下列变化不可能通过一步实验直接完成的是(? ) A.Al(OH)3→Al2O3 B.Al2O3→Al(OH)3 C.Al→AlO2 D.Al3+→AlO2- |
|
| 19. | 详细信息 |
|
下列关于铝及其化合物的说法中不正确的是( ) A.铝既可用于食品包装,也可用于建筑材料 B.氧化铝既可以用来冶炼铝,也可用作耐火材料 C.氢氧化铝既可以用于治疗胃酸过多的药物,也可用来制备一些铝盐 D.明矾既能用来净水,也可用作消毒剂 |
|
| 20. | 详细信息 |
|
下列关于钠与水反应的叙述,不正确的是(? ) ①将一小粒钠投入滴有紫色石蕊溶液的水中,反应后溶液变红 ②将一小粒钠投入稀盐酸中,钠先与水反应,后与HCl反应 ③钠在水蒸气中反应时因温度高会发生燃烧 ④将两小粒质量相等的金属钠,一粒直接投入水中,另一粒用铝箔包住,在铝箔上刺些小孔,然后投入水中,则二者放出氢气的质量相等 A.①② B.②③ C.②③④ D.①②③④ |
|
| 21. | 详细信息 |
将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法正确的是(? ) A. Mg和Al的总质量为8g B. 硫酸的物质的量浓度为5mol/L C. NaOH溶液的物质的量浓度为5mol/L D. 生成的H2在标准状况下的体积为11.2L |
|
| 22. | 详细信息 |
|
下列有关Na2CO3和NaHCO3性质的说法中,正确的是 A.热稳定性:Na2CO3<NaHCO3 B.相同温度下,在水中Na2CO3的溶解度小于NaHCO3 C.Na2CO3和NaHCO3均可与澄清石灰水反应 D.106gNa2CO3和84gNaHCO3分别与过量盐酸反应,放出CO2质量:Na2CO3>NaHCO3 |
|
| 23. | 详细信息 | |||||||||||||||
化学物质在生活中有着广泛的应用,下列对应关系错误的是
|
||||||||||||||||
| 24. | 详细信息 |
|
在含有1mol FeSO4的溶液中投入一小块金属钠,反应完全后,滤出沉淀并洗涤,然后在空气中灼烧沉淀得到的固体物质是( ) A. Fe B. FeO C. Fe(OH)3 D. Fe2O3 |
|
| 25. | 详细信息 |
|
把Ba(OH)2溶液滴入明矾溶液中,SO42-全部转化成BaSO4沉淀,此时铝元素的主要存在形式是 A. Al3+ B. Al(OH)3 C. AlO2- D. Al3+和Al(OH)3 |
|
| 26. | 详细信息 |
|
下列说法错误的是( ) A. 二氧化硅用于制备太阳能 B. 二氧化硅是生产光导纤维的主要材料 C. 从海水中提取物质不一定必须通过化学反应才能实现 D. 氢氟酸不能保存在玻璃瓶中 |
|
| 27. | 详细信息 |
|
KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为:2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O。(ClO2中氯元素的化合价为+4价) (1)浓盐酸在反应中表现出来的性质是_______(填写编号) ①只有还原性 ②还原性和酸性? ③只有氧化性? ④氧化性和酸性 (2)产生0.1molCl2,则转移电子的物质的量为________mol。 (3)用双线桥表示这个反应电子的转移情况2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O。 _____________________________ |
|
| 28. | 详细信息 |
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质之间的变化: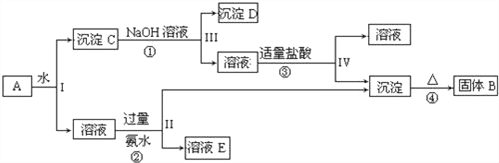 据此回答下列问题: (1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是_____. (2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式 沉淀固体B______;C________;沉淀D_____;溶液E________. (3)写出①、②、③、④四个反应方程式 ①_________________________; ②________________________; ③________________________; ④________________________. |
|
| 29. | 详细信息 |
已知有以下物质相互转化 试回答:(1)写出B的化学式 ,D的化学式 。 (2)写出由E转变成F的化学方程式 。 (3)写出用KSCN鉴别G溶液的实验现象是 ;向G溶液加入A的有关离子反应方程式 。 |
|
最近更新



