2018届高三12月月考化学在线测验(湖南省岳阳市第一中学)
| 1. | 详细信息 |
|
下列说法正确的是 A. 煤经过气化和液化两个物理变化,可变为清洁能源 B. 现代科技已经能够拍到氢键的“照片”,直观地证实了水分子间的氢键是一个水分子中的氢原子与另一个水分子中的氧原子间形成的化学键 C. 明矾净水时发生了化学及物理变化,能起到净水作用,而没有杀菌、消毒的作用 D. 用活性炭为糖浆脱色和用次氯酸盐漂白纸浆的原理相同 |
|
| 2. | 详细信息 |
|
下列热化学方程式书写正确的是(△H的绝对值均正确) A. C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g)? △H=-1367.0kJ?mol-1(燃烧热) B. NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)? △H=+57.3kJ?mol-1(中和热) C. 2NO2=O2+2NO? △H=+116.2kJ?mol-1(反应热) D. S(s)+O2(g)=SO2(g)? △H=-296.8kJ?mol-1(反应热) |
|
| 3. | 详细信息 | |||||||||||||||
物质制备过程中离不开物质的提纯。以下除杂方法正确的是
|
||||||||||||||||
| 4. | 详细信息 |
|
下列溶液中:①澄清石灰水②氯化钡溶液③KMnO4溶液④溴水⑤酸化的Ba(NO3)溶液⑥品红溶液⑦湿润的蓝色石蕊试纸⑧三氯化铁溶液⑨浓硫酸,不能用来区别SO2和CO2气体的是 A. ①②⑦⑨ B. ①③⑧ C. ①④⑤ D. ③④⑤⑥ |
|
| 5. | 详细信息 |
|
下列有关实验操作的叙述错误的是( ) A. 过滤操作中,漏斗的尖端应接触烧杯内壁 B. 从滴瓶中取用试剂时,滴管的尖嘴可以接触试管内壁 C. 滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁 D. 向容量瓶转移液体时,导流用玻璃棒可以接触容量瓶内壁 |
|
| 6. | 详细信息 | ||||||||
利用下列装置和操作不能达到实验目的的是( )
|
|||||||||
| 7. | 详细信息 |
|
下列叙述正确的是(用NA代表阿伏加德罗常数的值) A. 2.4g金属镁变为镁离子时失去的电子数为0.1NA B. 1molHCl气体中的粒子数与0.5mol/L 盐酸中溶质粒子数相等 C. 将1molCl2通入水中,HClO、Cl-、ClO-粒子数之和为2NA D. 在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10NA |
|
| 8. | 详细信息 | |||||||||||||||
下列实验操作能达到目的的是
|
||||||||||||||||
| 9. | 详细信息 | ||||||||||||||||||||
下列离子组在一定条件下能大量共存且加入相应试剂后所对应的离子方程式正确的是
|
|||||||||||||||||||||
| 10. | 详细信息 |
X、Y、Z、W是原子序数依次增大的四种短周期元素,A、B、C、D、F是由其中的两种或三种元素组成的化合物,E是由Z元素形成的单质,0.1mol?L-1 D溶液的pH为13(25℃)。它们满足如图转化关系,则下列说法正确的是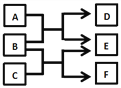 A. 由X、Y、Z、W四种元素组成的盐溶液pH小于7 B. 化合物F中含有共价键和离子键 C. 0.1molB与足量C完全反应共转移电子数为0.2NA D. Z元素的最高正价为+6 |
|
| 11. | 详细信息 | |||||||||||||||
将0.2mol?L-1的KI溶液和0.05mol?L-1Fe2(SO4)3溶液等体积混合充分反应后,取混合液分别完成下列实验,能说明溶液中存在化学平衡2Fe3++2I-
|
||||||||||||||||
| 12. | 详细信息 |
右图装置中发生反应的离子方程式为:Zn+2H+=Zn2++H2↑,下列说法错误的是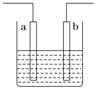 A. a、b不可能是同种材料的电极 B. 该装置可能是电解池,电解质溶液为稀盐酸 C. 该装置可能是原电池,电解质溶液为稀盐酸 D. 该装置可看作是铜-锌原电池,电解质溶液是稀硫酸 |
|
| 13. | 详细信息 |
常温下,用0.10mol?L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol?L-1CH3COOH溶液和HCN溶液所得滴定曲线如下图。下列说法正确的是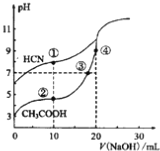 A. 点①和点②所示溶液中:c(CH3COO-)<c(CN-) B. 点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH) C. 点④所示溶液液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) D. 点②和点③所示溶液中都有:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+) |
|
| 14. | 详细信息 |
利用甲烷燃料电池电解饱和食盐水制备漂白液,下列说法中不正确的是(? )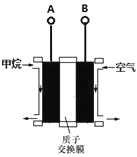 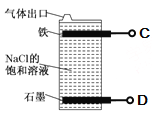 A. 燃料电池的A极连接电解池的C极 B. A电极的电极反应式为:CH4-8e-+2H2O = CO2+8H+ C. 燃料电池工作时H+移向左边 D. 电解池总反应式为NaCl+H2O |
|
| 15. | 详细信息 | ||||||||
部分弱酸的电离平衡常数如下表所示:
|
|||||||||
| 16. | 详细信息 |
在2L恒容密闭容器中充入2 mol X和1mol Y发生反应:2X(g)+Y(g) 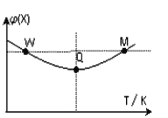 A. Q点时,Y的转化率最大 B. W点X的正反应速率等于M点X的正反应速率 C. 升高温度,平衡常数增大 D. 温度一定,平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大 |
|
| 17. | 详细信息 |
|
研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应: 2NO2(g)+NaCl(s) 2NO(g)+Cl2(g) (1)4NO2(g)+2NaCl(s) (2)为研究不同条件对反应(II)的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(II)达到平衡。测得10min内v(ClNO)=8.0×10-3mol?L-1?min-1,回答下列问题 ①平衡后n(Cl2)=__________mol, ②NO的转化率а1=_______。 ③其它条件保持不变,反应(II)在恒压条件下进行,平衡时NO的转化率а2________а1(填“>”“<”或“=”),平衡常数K2___________(填“增大”“减小”或“不变”)。 ④若要使K2减小,可采用的措施是________________________。 |
|
| 18. | 详细信息 |
|
某学生研究小组欲探究CuSO4溶液与Na2CO3溶液混合产生的蓝绿色沉淀组成,小组进行下列实验探究。 【提出假设】 假设1:沉淀为Cu(OH)2 假设2:沉淀为_________ 假设3:沉淀为碱式碳酸铜[化学式可表示为nCuCO3?mCu(OH)2] 【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水)。 【物质成分探究】 步骤1:将所得悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤 步骤2:甲同学取一定量固体,用气密性良好的下图装置(夹持仪器未画出)进行定性实验。 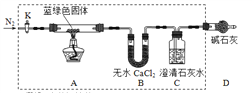 请回答下列问题: (1)假设2中的沉淀为___________________。 (2)假设1中沉淀为Cu(OH)2的理论依据是(用离子方程式表示)____________。 (3)无水乙醇洗涤的目的_______________________________________。 (4)若反应后A中蓝绿色固体变黑,C中无明显现象,证明___________成立。(填写“假设1” “假设2”或“假设3”)。 (5)乙同学认为只要将上图中B装置的试剂改用______试剂后,便可验证上述所有假设。 (6)乙同学更换B试剂后验证假设3成立的实验现象是_______________________。 |
|
| 19. | 详细信息 | ||||||||||
绿矾(FeSO4?7H2O) 是治疗缺铁性贫血药品的重要成分。下面是以市售铁屑(含少量锡、氧化铁等杂质) 为原料生产纯净绿矾的一种方法: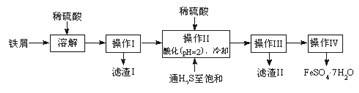 查询资料,得有关物质的数据如下表:
|
|||||||||||
| 20. | 详细信息 |
下图表示氮及其化合物在一定条件下的转化关系: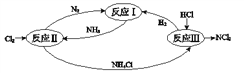 (1)反应I:N2(g)+3H2(g) 下左图是反应I中平衡混合气中NH3的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是________(填“温度”或“压强”)。  (2)①反应II的化学方程式是_________________________。 ②反应II其中一步反应为2NH3(g)+3Cl2(g)=N2(g)+6HCl(g)? ΔH=?462 kJ?mol-1 已知:N2(g) 断开1 mol H?N键与断开1 mol H?Cl键所需能量相差约为________kJ。 (3)反应III是利用上图所示装置电解制备NCl3(氯的化合价为+1),其原理是:NH4Cl+2HCl ①b接电源的_______极(填“正”或“负”)。② 阳极反应式是___________________。 (4)反应III得到的NCl3可以和NaClO2制备 ClO2,同时生成NH3,该反应的离子方程式是________。 |
|