河北2019年高一化学上册月考测验同步练习
| 1. | 详细信息 |
在盛放浓硫酸的试剂瓶标签上应印有下列警示标记中的( ) A. A B. B C. C D. D |
|
| 2. | 详细信息 |
|
钛具有硬度大、密度小、熔点高、抗腐蚀性强等优良性能,被誉为“未来金属”、二氧化钛(TiO2)中氧元素为﹣2价,则钛元素的化合价为( ) A. +1 B. +2 C. +3 D. +4 |
|
| 3. | 详细信息 |
|
下列符号能表示两个氢原子的是( ) A. H2 B. 2H2 C. 2H D. 2H+ |
|
| 4. | 详细信息 |
|
下列反应的离子方程式不正确的是( ) A. 向(NH4)2SO4溶液中加入足量Ba(OH)2:Ba2++SO42-=BaSO4↓ B. 向氢氧化钾溶液中滴加少量氯化铝溶液Al3++4OH-=AlO2-+2 H2O C. 碳酸氢钠溶液中加入过量氢氧化钠溶液 HCO3- + OH- =CO32- + H2O D. 向浓硝酸中加入铜片:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
|
| 5. | 详细信息 |
|
在某酸性溶液中,分别加入下列各组离子,一定能大量共存的是( ) A. NH4+、SO42-、CO32-、K+ B. Na+、Ba2+、Ca2+、HCO3- C. Ag+、SO42-、K+、Cl- D. K+、Cl-、Na+、SO42- |
|
| 6. | 详细信息 |
|
某同学欲配制溶质质量分数为8%的食盐水80g,在用托盘天平称量食盐时,他把食盐和砝码的位置放颠倒了(1g以下用游码),那么实际上他所配制的食盐水的溶质质量分数为 A. 8.5% B. 7.5% C. 14% D. 7.1% |
|
| 7. | 详细信息 |
|
某学习小组辨析以下说法:①粗盐和酸雨都是混合物;②非金属氧化物一定都是酸性氧化物;③冰和干冰既是纯净物又是化合物;④金属钠和镁的化学性质不同,主要是由于钠原子和镁原子的最外层电子数不同;⑤磷酸和醋酸都是多元酸;⑥纯碱和烧碱都是碱。说法正确的是 ( ) A. ②③④ B. ①②⑤ C. ③⑤⑥ D. ①③④ |
|
| 8. | 详细信息 |
|
化学使世界变得绚丽多彩。生活中的下列变化没有化学变化发生的是 A. 节日燃放焰火 B. 木炭烤熟食物 C. 西瓜榨成西瓜汁 D. 檀树皮制成宣纸 |
|
| 9. | 详细信息 |
|
绿水青山就是金山银山, 要保护好绿水青山,下列做法合理的是( ) A. 森林着火时,将火焰蔓延线路前的小片树林砍掉 B. 我国地域面积广阔,林木可以随意砍伐 C. 将塑料袋、矿泉水瓶等随手丢弃河道中 D. 随身携带打火机进入泰山旅游景区 |
|
| 10. | 详细信息 |
|
事物的宏观表象是由其微观性质决定的。下列事实及对这些事实的解释中,二者不相符的是( ) A. 成熟的菠萝会散发出浓浓的香味,说明分子在不断地运动 B. 水沸腾时能掀开壶盖,说明分子的大小随温度升高而增大 C. 50mL水和50mL酒精混合后总体积小于100mL,说明分子间有间隔 D. 湿衣服晾在太阳晒着的地方干得快,说明分子的运动速率与温度有关 |
|
| 11. | 详细信息 |
|
下列各组离子一定能共存的是( ) A. H+ Fe2+ Cl- NO3- B. Na+ K+ OH- CO32- C. NH4+ Na+ HCO3- OH- D. Fe3+ H+ SO42- SCN- |
|
| 12. | 详细信息 |
|
根据下列反应判断有关物质还原性由强到弱的顺序是( ) ①H2SO3+I2+H2O===2HI+H2SO4 ②2FeCl3+2HI===2FeCl2+2HCl+I2 ③3FeCl2+4HNO3===2FeCl3+NO↑+2H2O+Fe(NO3)3 A. H2SO3>I−>Fe2+>NO B. I−>Fe2+>H2SO3>NO C. Fe2+>I−>H2SO3>NO D. NO>Fe2+>H2SO3>I− |
|
| 13. | 详细信息 |
|
下列制取蒸馏水的实验装置与操作的说法中,不正确的是( ) A. 温度计的水银球应插入蒸馏烧瓶中的自来水中 B. 冷凝管中的水流方向是从下口进入,上口排出 C. 实验中需要在蒸馏烧瓶中加入几粒碎瓷片,防止出现暴沸现象 D. 加热蒸馏烧瓶必须垫石棉网 |
|
| 14. | 详细信息 |
|
用NA表示阿伏加德罗常数的值。下列判断错误的是( ) A. NA个H+的质量为1 g B. 2 L 0.5 mol/L Na2SO4溶液中含NA个Na+ C. 32 g O2中含有2NA个氧原子 D. 标准状况下,1 mol H2O中含有NA个分子 |
|
| 15. | 详细信息 |
在0.1 L由NaCl、MgCl2、BaCl2组成的混合溶液中,部分离子浓度大小如图所示,下列对该溶液成分说法不正确的是( )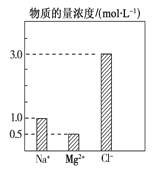 A. NaCl的物质的量为0.1mol B. 该混合液中BaCl2的物质的量为0.05mol C. 溶质MgCl2的质量为9.5 g D. 将该混合液加水稀释至体积为1 L,稀释后溶液中的Na+物质的量的浓度为0.1mol/L |
|
| 16. | 详细信息 |
|
下列实验操作:①过滤 ②溶解 ③蒸馏 ④取用药品 ⑤萃取 ⑥配制一定浓度的溶液,一定要用到玻璃棒的是 A. ①②⑥ B. ②③⑥ C. ③④⑥ D. ④⑤⑥ |
|
| 17. | 详细信息 |
|
在无色溶液中,下列离子能大量共存的是 A. Mg2+、SO42-、K +、Cl- B. Na+ 、NH4+ 、NO3-、MnO4- C. K + 、Cu2+ 、Cl-、Br- D. Ba2+ 、Na+ 、OH-、HCO3- |
|
| 18. | 详细信息 |
|
向50 mL 18 mol·L-1的H2SO4溶液中加入适量的铜片并加热。充分反应后,被还原的H2SO4的物质的量( ) A. 小于0.45 mol B. 等于0.45 mol C. 在0.45~0.90 mol之间 D. 大于0.45 mol |
|
| 19. | 详细信息 |
|
某固体A在一定条件下可完全分解,生成B、C、D三种气体的混合物。反应方程式如下:2A=B↑+2C↑+3D↑,此时测得混合气体的相对平均分子质量为30,则固体A的摩尔质量为( ) A. 30g/mol B. 90g/mol C. 30 D. 90 |
|
| 20. | 详细信息 |
|
下列关于加热的操作正确的是( ) A. 给试管中的液体加热时,试管口不准对着别人,但可以对着自己 B. 玻璃仪器都可以用于加热 C. 用H2还原氧化铜的实验中,应把H2通过预先加热的氧化铜 D. 无论给试管中的液体还是固体加热,都必须先预热 |
|
| 21. | 详细信息 |
|
某溶液含有NaCl、K2SO4、KCl三种溶质,已知c(Cl﹣)为0.4mol·L-1、c(K+)为0.7 mol·L-1、c(Na+)为0.1 mol·L-1。则该混合溶液中硫酸根离子浓度为 A. 0.1 mol·L-1 B. 0.2 mol·L-1 C. 0.3 mol·L-1 D. 0.4 mol·L-1 |
|
| 22. | 详细信息 |
|
选择下列实验方法分离物质,将分离方法的序号填在横线上。 A.萃取分液 B.升华 C.结晶 D.分液 E.蒸馏 F.过滤 (1)______分离饱和食盐水与沙子的混合物。 (2)______从硝酸钾和氯化钠的混合液中获得硝酸钾。 (3)______分离水和汽油的混合物。 (4)______从碘水中提取碘。 |
|
| 23. | 详细信息 | ||||||||||||||||||||||||||||||||||||
如表为元素周期表的一部分,标出了A~K共十种元素所在位置。请用元素符号或化学式回答下列问题。
|
|||||||||||||||||||||||||||||||||||||
| 24. | 详细信息 |
据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染。某种手机电路板中含有以下金属:Sn、Pb、Fe、Cu、Au、Ag、Ni(镍,银白色)、Pd (钯,银白色)。如图是某工厂回收其中部分金属的流程图.(假设流程图中各反应均恰好完全反应.己知:2Cu+O2+2H2SO4 (1)步骤②中产生的气体是________(写化学式)。 (2)滤渣2中含有的金属是________ (3)步骤⑤反应的化学方程式________。 (4)步骤⑥回收的纯净物B是________ (写化学式)•. (5) 金属Fe、Ni、Pd在溶液中的活动性由强到弱的顺序依次是________。 |
|
| 25. | 详细信息 |
无水四氯化锡(SnCl4)可由下述反应制得:Sn+2Cl2==SnCl4。氯气是一种黄绿色的气体。纯的四氯化锡在常温下是无色液体,极易与水反应,在空气中与水蒸汽作用而冒白烟。下图是制备四氯化锡的装置图: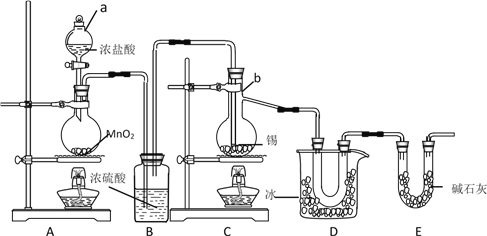 请回答下列问题: (1)写出仪器b的名称_________________ (2)写出下列装置的作用:A________________、D________________、E________________。 (3)装好药品,并安装好仪器后,开始制备SnCl4的系列实验操作是_______ |
|
| 26. | 详细信息 |
将2.5 g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶于水,制成稀溶液,然后向该溶液中逐滴加入1 mol·L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如下图所示:(提示:碳酸钠与少量盐酸反应生成碳酸氢钠和氯化钠。) (1)写出OA段所发生反应的化学方程式___________________________。 (2)当加入35 mL盐酸时,产生CO2的体积为________mL(标准状况)。 (3)原混合物中NaOH的质量为________g,碳酸钠的质量分数为________。 |
|
| 27. | 详细信息 |
| 将10.4g金属铁与镁投入到足量的稀盐酸中完全反应,共收集到标准状况下气体6.72L,求混合物中两种金属的物质的量之比_______。 | |
高中化学 试卷推荐
最近更新



