2018年至2019年高二前半期9月月考化学试卷带参考答案和解析(广西壮族自治区贵港市覃塘高级中学)
| 1. | 详细信息 |
|
下列化学用语表达不正确的是( ) ①丙烷的球棍模型  ②丙烯的结构简式为CH3CHCH2 ③某有机物的名称是2,3-二甲基戊烷 ④ A. ①② B. ②③ C. ③④ D. ②④ |
|
| 2. | 详细信息 |
|
下列命称的有机物实际上不可能存在的是( ) A. 2,2﹣二甲基丁烷 B. 2﹣甲基﹣4﹣乙基﹣1﹣己烯 C. 3﹣甲基﹣2﹣戊烯 D. 3,3﹣二甲基﹣2﹣戊烯 |
|
| 3. | 详细信息 |
|
NA为阿伏加德罗常数,下列说法正确的是 A. 28g乙烯所含共用电子对数目为6NA B. 标准状况下,11.2L的正戊烷所含的分子数为0.5NA C. 常温常压下,11.2 L一氯甲烷所含分子数为0.5 NA D. 14g乙烯、丙烯、丁烯的混合气体,其原子数为4NA |
|
| 4. | 详细信息 |
|
下列有机物中,可以形成顺反异构的是( ) A. 2-甲基-2-丁烯 B. 丙烯 C. 1-氯-1-丙烯 D. 2,3-二甲基-2-丁烯 |
|
| 5. | 详细信息 |
|
某烃结构式用键线表示为 A. 3种 B. 6种 C. 5种 D. 4种 |
|
| 6. | 详细信息 |
|
下列化合物的核磁共振氢谱中出现三组峰的是: A.2,2,3,3一四甲基丁烷 B.2,3,4一三甲基戊烷 C.3,4一二甲基己烷 D.2,5一二甲基己烷 |
|
| 7. | 详细信息 | ||||||||||||||||||||
为除去杂质,所选用的除杂试剂和分离方法都正确的是( )
|
|||||||||||||||||||||
| 8. | 详细信息 |
已知有机物A的结构简式如下图所示,1mol A与足量的NaOH溶液混合共热,充分反应后最多消耗NaOH的物质的量为( ) A. 6mol B. 7mol C. 8mol D. 9mol |
|
| 9. | 详细信息 |
|
下列表示对应化学反应的离子方程式正确的是 A. 向银氨溶液中滴加乙醛:CH3CHO+2[Ag(NH3)2]++H2O B. 苯酚钠溶液中通入少量CO2: C. 硫酸氢铵溶液中滴加少量NaOH溶液:H++ D. 氯乙酸与足量的氢氧化钠溶液共热:CH2ClCOOH+OH− |
|
| 10. | 详细信息 |
|
一氧化碳、烯烃和氢气在催化剂作用下发生烯烃的醛化反应,又称羰基的合成,如由乙烯可制丙醛:CH2=CH2+CO+H2 A. 2种 B. 3种 C. 4种 D. 5种 |
|
| 11. | 详细信息 |
某烃的结构简式如图所示,若分子中共线碳原子数为a,可能共面的碳原子最多为b,含四面体结构碳原子数为c,则a、b、c分别是( ) A. 3,4,5 B. 3、14,4 C. 3,l0,4 D. 4,l0,4 |
|
| 12. | 详细信息 |
|
某烃经催化加氢后,不能得到2-甲基丁烷,该烃是 A. 2-甲基-1-丁烯 B. 2-甲基-2-丁烯 C. 3-甲基-1-丁炔 D. 3,3-二甲基-1-丁炔 |
|
| 13. | 详细信息 |
|
I.现有下列十组物质: ①O2和O3 ②126C 和146C ③4039K和4020Ca ④甲烷和丙烷 ⑤甲醇和乙二醇 ⑥  和 和  ⑦ ⑦ 和 和 ⑧葡萄糖和果糖 ⑨蔗糖和麦芽糖 ⑩淀粉和纤维素 (1)互为同分异构体的是_______________;(填序号) (2)互为同系物的是_______________;(填序号) (3)⑦中有机物  按系统命名法命名为______________。 按系统命名法命名为______________。Ⅱ.写出下列化合物的名称或结构简式: ① 有机物 ② ③ CH2===CHCOOH_____________________________, ④ 2,5 -二甲基-2,4 -己二烯的结构简式:__________________________________。 |
|
| 14. | 详细信息 |
|
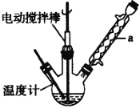
现有四种有机物:①乙烯 ②2-丙醇 ③ 甲苯 ④ 乙炔,其中: (1)能发生消去反应的是_________(填序号,下同),其化学方程式是________。 (2)能衡量一个国家的石油化工生产水平的是__________,该物质可用于一种常用塑料,其反应的化学方程式是__________。 (3)能用来制取梯恩梯(TNT)的是________,其发生反应的化学方程式是________。 (4)碳元素的质量百分含量最高的是________,实验室制取该物质的反应装置如下:  甲中反应的化学方程式是________,滴加饱和食盐水而不直接滴加水的原因是________,乙中硫酸铜溶液的作用是________。 |
|
| 15. | 详细信息 | ||||||||||||||||||||||||||||||
甲苯(
|
|||||||||||||||||||||||||||||||
| 16. | 详细信息 |
有机物G( )是一种重要的有机高分子材料,实验室由有机物A制备G的一种合成路线如下: )是一种重要的有机高分子材料,实验室由有机物A制备G的一种合成路线如下: 回答下列问题: (1)D的名称是________B分子中含有的官能团的名称是___________________________。 (2)A→B、B→C的反应类型分别为_____________________、_________________________。 (3)下列说法正确的是_____________________(填字母编号)。 a.A分子存在顺反异构 b.可以用NaHCO3鉴别D和F c.E分子中最多有14个原子位于同一平面上 (4)写出D+F→G的化学方程式________________________。 (5)H是F的同系物,其相对分子质量比F多28,H的核磁共振氢谱有三组峰,峰面积比为3︰1︰1,则符合该条件的H的同分异构体共有______种,写出其中H的一种结构简式___________。 |
|