2017甘肃高一下学期人教版高中化学月考试卷
| 1. | 详细信息 |
|
下列反应中,起了氮的固定作用的是 A.N2与H2在一定条件下合成氨 B.由氨制成碳酸氢铵或硫酸铵 C.NO与O2反应生成NO2 D.NO2与H2O反应生成HNO3
|
|
| 2. | 详细信息 |
|
下列微粒中:①13Al3+ ② A.①②③ B.②③④ C.①②④ D.①③④
|
|
| 3. | 详细信息 |
|
1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学史上的重要里程碑之一。下列有关元素周期表的说法正确的是 A.元素周期表含元素最多的族是第ⅢB族 B.元素周期表有18个族 C.第ⅠA族的元素全部是金属元素 D.短周期是第一、二、三、四周期
|
|
| 4. | 详细信息 |
|
下列叙述正确的是 A.浓硫酸、浓盐酸和浓硝酸长期暴露在空气中,质量都会减小,浓度都会降低 B.氯水和活性炭都可使红墨水褪色,且原理相似 C.浓硝酸中的HNO3见光会分解,故有时在实验室看到的浓硝酸呈黄色 D.浓H2SO4有强氧化性,常温下能与Cu发生剧烈反应
|
|
| 5. | 详细信息 |
|
以下关于锂、钠、钾、铷、铯的叙述不正确的是 ①氢氧化物中碱性最强的是CsOH ②单质熔点最高的是铯 ③与O2反应均可得到多种氧化物 ④它们的密度依次 ⑤其单质的还原性依次增强 ⑥它们对应离子的氧化性也依次增强 ⑦单质与水反应的剧烈程度依次增强 A.①⑤⑦ B.②⑤⑥ C.②③④⑥ D. ②③⑤⑦
|
|
| 6. | 详细信息 |
|
下列说法正确的是 A.离子键就是使阴、阳离子结合成化合物的静电引力 B.所有金属与所有非金属之间都能形成离子键 C.含有共价键的化合物一定是共价化合物 D.含有离子键的化合物一定是离子化合物
|
|
| 7. | 详细信息 |
|
X元素原子的L层比Y元素原子的L层少3个电子,X元素原子的核外电子总数比Y原子核外电子总数少5个,则X、Y可形成的化合物是 A. 离子化合物Y(XO4)2 B. 离子化合物Y2X3 C . 共价化合物XY2 D. 离子化合物Y3X2
|
|
| 8. | 详细信息 |
|
下图所示各为元素周期表中的一部分,表中数字是原子序数,其中X为35的是
|
|
| 9. | 详细信息 |
|
最近医学界通过用放射性14C标记C60,发现一种C60的羧酸衍生物在特定条件下可通过断裂DNA杀死细胞,从而抑制艾滋病(AIDS),下列有关14C的 A.与12C与C60中普通碳原子的化学性质不同 B.14C与14N含的中子数相同 C.14C是C60的同素异形体 D.14C与12C互为同位素
|
|
| 10. | 详细信息 |
|
在周期表中金属和非金属的分界线附近能找到 A.制农药的元素 B.制催化剂的元素 C.制半导体的元素 D.制耐高温合金材料的元素
|
|
| 11. | 详细信息 |
|
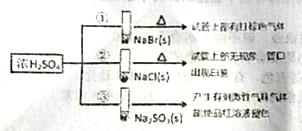
浓硫酸分别和三种钠盐反应,下列分析正确的是
A.对比①和②可以说明还原性Br->Cl- B.①和③相比可说明氧化性Br2>SO2 C.②中试管口白雾是HCl遇水蒸气所致,说明酸性H2SO4>HCl D.③中浓H2SO4被还原成SO2
|
|
| 12. | 详细信息 |
|
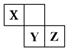
X、Y、Z三种短周期元素在周期表中的位置如下图,X通过共用三队电子形成X2分子,下列说法不正确的是
A.化合物XZ3中各原子均满足8电子的稳定结构 B.X、Y、Z三种元素形成的含氧酸都是强酸 C.常温下,Z单质可与Y的氢化物发生置换反应 D.一定条件下,X2与Al反应得到AlX
|
|
| 13. | 详细信息 |
|
分别处于第二、第三周期的主族元素A和B,它们的离子电子层结构相差两层,已知A处于第m族,B处于第n族,A只有正化合价,则A、B的原子序数分别是 A.m、n B.3、7 C.m-2、10-n D.m+2、n+10
|
|
| 14. | 详细信息 |
|
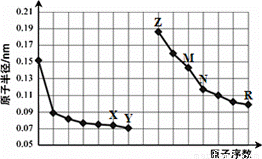
下图是部分短周期元素原子半径与原子序数关系图,下列说法正确的是
A.X与M形成的一个阴离子中含有29个电子 B.气态氢化物沸点:Y > C.由X与N两种元素组成的化合物不能与任何酸反应,但能与强碱反应 D.Z单质不能从M与R元素构成的盐溶液中置换出单质M
|
|
| 15. | 详细信息 |
|
下列判断错误的是 A.稳定性:NH3>PH3>AsH3 B.离子半径:Li+>O2->F- C.酸性:H3PO4>H2SO4>HClO4 D.碱性:LiOH>NaOH>KOH
|
|
| 16. | 详细信息 |
|
根据元素在元素周期表中的位置,运用元素周期律分析下面推断,其中错误的是 A.铍(Be)的氧化物的水化物可能具有两性 B.砹(At)为有色固体,HAt不稳定,AgAt感光性很强,不溶于水也不溶于酸 C.锶是第五周期第ⅡA族的元素,硫酸锶(SrSO4)是难溶于水的白色固体 D.硒是第四周期第ⅡA族的元素,硒化氢(H2Se)是有色有毒的气体,比H2S稳定
|
|
| 17. | 详细信息 |
|
有两种短周期元素组成的化合物,其中两种元素的原子个数比为1:3,若两种元素的原子序数分别为a和b,则a和b的关系可能是 ①a=b+4;② A.①②③④ B.①③④ C.②④ D.③④
|
|
| 18. | 详细信息 |
|
下列分子中所有原子最外层都满足8电子稳定结构的是 A.BF3 B.CO2 C.NH3 D.PCl5
|
|
| 19. | 详细信息 |
|
已知1-18号元素的离子aXm+、bYn+、cZp-、dWk-都具有相同的电子层结构,下列关系正确的是 A.若p>k,则还原性:cZp-> dWk- B.若m>n,则碱性:X(OH)m>Y(OH)n C.若半径,aX D.若半径aXm+>bYn+,则X的单质一定能从含Yn+的盐溶液中置换出Y
|
|
| 20. | 详细信息 |
|
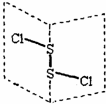
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如左下图所示。常温下,S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体.下列说法中错误的是
A.S2Cl2的电子式为 B.S2Cl2同时含有极性键又有非极性 C.S D.S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl
|
|
| 21. | 详细信息 |
|
下表中的实线表示元素周期表的部分边界,a-1分
(1)请在上表中用实线补全元素周期表边界。 (2)表中所列元素,不属于短周期元素有 ,不属于主族元素的有 (填相应的元素符号) (3)指出下列元素在周期表中的位置: ①b元素位于第 周期 族;②g元素位于第 周期 族;③i元素位于第 周期 族; (4)①写出b与c的化合物(温室气体)电子式: ; ②用电子式表示k与h化合物形成过程: 。
|
|
| 22. | 详细信息 |
|
现有下列物质:①Cl2 ②Na2O2 ③NaOH ④HCl ⑤H2O2 ⑥MgF2 ⑦NH4Cl (1)只由离子键构成的物质是 (填序号,下同) (2)只由极性键构成的物质是 (3)由极性键和非极性键构成的物质是 (4)由离子键和非极性键构成的物质是 (5)属于离子化合物的物质是 (6)属于共价化合物的物质的是 (7)下列变化(填字母)A碘的升华B烧碱熔化C氯化 既发生离子键又发货所能共价键破坏的是 。
|
|
| 23. | 详细信息 | ||||||||||||||||||||||||
|
a、b、c、d、e、f、g为七种由短周期元素构成的粒子,它们都具有10个电子,其结构特点如下:
其中b的离子半径大于e的离子半径;d是由极性键构成的四原子分子;试写出: (1)a粒子的原子结构示意图 (2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为 > (用化学式表示)。 (3)d与一种含有极性键双核18电子分子反应的化学方程式为 。 (4)g与一种含有非极性键双核18电子分子反应的化学方程式为 上述反应中,断裂化学键是 ,写出的化学键是 (填“离子键”、“极性键”、“非极性键”、“氢键”)
|
|||||||||||||||||||||||||
| 24. | 详细信息 |
|
A、B、C、D、E、F是短周期元素,周期表中A与B、B与C相邻;C与E同主族;A与C最外层电子数之比为2:3,B的最外层电子数比C的最外层电子数少1个; F元素的原子在周期表中半径最小;常见化合物D2C2与水反应生成C的单质,且溶液使酚酞溶液变红。 (1)F的三种核素表示符号为 ,E的名称为 ,D的最高价氧化物的水化物的电子式: 。 (2)在B、C、D、E、F原子形成的单核离子中离子半径最小的是 ,离子半径最大的是 。(填离子符号) (3)A、B、C的氢化物稳定性顺序为 (用分子式表示);B的氢化物和B的最高价氧化物的水化物反应生成Z,反应中断裂化学键是 ,形成的化学键是 。(填“离子键”、“极性键”、“非极性键”、“氢键”) (4)F2C和F2E中,沸点较高的是 (填化学式),其主要原因是 。 (5)两种均含C、D、E、F四种元素的化合物相互反应放出气体的反应离子方程式为 。
|
|
| 25. | 详细信息 |
|
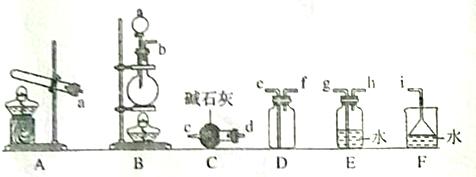
(1)写出实验室中由固体物质制取氨气的化学方程式 ; (2)欲收集一瓶干燥的氨气,选择下图中的装置,其连接顺序为 发生装置
|
|
| 26. | 详细信息 |
|
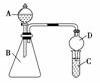
某学习小组同学为探究同周期或同主族元素性质的递变规律,设计了如下系列实验: Ⅰ.探究同周期金属性和非金属性的递变规律 (1)将等质量的钠、镁、铝分别投入到足量的同浓度的盐酸中,实验结果:上述金属中 与盐酸反应最剧烈, 与盐酸反应产生的气体最多,可证明金属性: > > 。(填元素符号) (2)向Na2S溶液中通入氯气,反应现象是 ,反应的离子方程式为 ,可证明非金属性: > 。 Ⅱ.利用如图装置来验证同主族元素非金属性的变化规律
(1)要证明非金属性:Cl>I,在A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加 溶液,观察到C中溶液________的现象,即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用 溶液吸收尾气。 (2)要证明非金属性:C>Si,在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,将观察到C中 的现象。但老师认为,该现象不足以证明酸性强弱关系为碳酸>硅酸,请用文字叙述理由 。 因此应在B、D之间增加一个盛有
|
|
| 27. | 详细信息 |
|
将一定质量由Cu和CuO组成的固体粉末加入到100mL 11mol/L的浓HNO3中,充分反应后,固体溶解完全,收集到NO、NO2混合气体6.72L(标准状况)。若将该混合气体与2.24L O2(标准状况)混合并通入到足量水中,恰好生成HNO3. (1)固体粉末中Cu单质的质量是多少克? (2)向浓HNO3反应后的溶液中加入4mol/L的NaOH溶液,当Cu2+恰好沉淀完时,需要NaOH溶液的体积是多少升?
|
|