2016四川九年级下学期人教版初中化学期中考试
| 1. | 详细信息 |
|
家庭生活中处处有物质的变化,以下属于物理变化的是( ) A.鲜牛奶变质 B.酵母粉发酵 C.钢丝球刷碗 D.洁厕精除垢
|
|
| 2. | 详细信息 |
|
PM2.5是造成雾霾天气的“元凶”之一,下列做法不会增加空气中的PM2.5的是( ) A.焚烧秸杆 B.植树造林 C.燃放鞭炮 D.工厂排放烟尘
|
|
| 3. | 详细信息 |
|
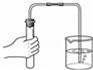
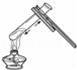
下列图示的实验操作不规范的是( ) A.
|
|
| 4. | 详细信息 |
|
2015年中国科学家屠呦呦获诺贝尔医学奖,她研究发现了青蒿素(C15H22O5),开创了疟疾治疗的新方法.下列关于青蒿素(C15H22O5)的说法错误的是( ) A.青蒿素中氢元素的质量分数最高 B.青蒿素属有机物 C.青蒿素中C、O元素的质量比为9:4 D.青蒿素的组成元素全部是非金属元素
|
|
| 5. | 详细信息 |
|
我国科学家率先用铝合金和石墨烯按一定比例混合制成“烯合金”,该材料有望生产出“一分钟能充满电的电池”,下列关于“烯合金”的说法不正确的是( ) A.含有金属材料 B.含碳元素和铝元素 C.具有导电性 D.是一种纯净物
|
|
| 6. | 详细信息 |
|
下列有关燃烧的说法正确的是( ) A.二氧化碳和水都可用于灭火,目的是降低可燃物的着火点 B.将煤制成蜂窝煤进行燃烧是为了使其燃烧更加充分 C.物质燃烧时反应中一定有氧气参加 D.煤、天然气和石油常称为化石燃料,都是可再生能源
|
|
| 7. | 详细信息 |
|
甲、乙、丙、丁四种金属.甲即使在高温时也不与氧气反应.乙、丙、丁在一定条件下都能与氧气反应.丁盐的水溶液可用丙制的容器盛放,但不能用乙制的容器盛放.这四种金属的活动性由强到弱的顺序是( ) A.甲>乙>丁>丙 B.丙>丁>乙>甲 C.丙>乙>丁>甲 D.乙>丁>丙>甲
|
|
| 8. | 详细信息 |
|
下列实验方案或做法不合理的是( ) A.热固性塑料和热塑性塑料,可加热观察外形变化 B.用排水法收集O2结束时,先熄灭酒精灯,后移出导管 C.用稀H2SO4区别NaOH、K2CO3、BaCl2三种白色固体 D.为区别化肥硝酸钾和硝酸铵用加入熟石灰研磨闻气味
|
|
| 9. | 详细信息 |
|
氢氧化钴[Co(OH)2]受热易分解,能与酸性溶液反应,可作涂料和油漆的干燥剂,其制备方法为:①Co+2HCl═CoCl2+H2↑;②CoCl2+NaOH═Co(OH)2↓+2NaCl.下列判断正确的是( ) A.钴的金属活动性比铜强 B.①为置换反应,②中和反应 C.氢氧化钴的化学性质稳定 D.氢氧化钴可用来干燥氯化氢气体
|
|
| 10. | 详细信息 | ||||||||||||||||||||
|
除去下列各物质中的少量杂质,所用方法不可行的是( )
A.A B.B C.C D.D
|
|||||||||||||||||||||
| 11. | 详细信息 |
|
用化学用语填空. (1)核内质子和中子都为6的原子 ; (2)2个铵根离子 ; (3)造成“温室效应”气体 ;(4)位于第三周期ⅢA族的元素是 ; (5)实验室常用的液体燃料 ;(6)蒸馒头用的发酵粉中含有的盐 .
|
|
| 12. | 详细信息 |
|
生活生产中处处有化学,化学就在身边. (1)生活中要降低饮用水的硬度,可采用 的方法,要测定饮用水的酸碱度,可用 p . (2)电解水的化学方程式是 ,通过该实验得到的结论是 (任写一点). (3)雨水淋湿的衣服在空气中能晾干,说明分子的性质是 . (4)二氧化氯(ClO2)是饮用水的高效消毒剂,制取ClO2反应为:Cl2+2NaClO2═2ClO2+2X,则X的化学式为 . (5)镍(Ni)是铸造钱币的主要材料,镍及其化合物能发生如下反应,请回答: Ⅰ.Ni+2HCl═NiCl2+H2↑Ⅱ.NiO2+4HCl═NiCl2+Cl2↑+2H2O ①反应Ⅱ中Ni的化合价在反应前后 (填“不变”、“升高”或“降低”). ②金属镍(Ni)与硝酸银溶液反应的化学方程式为 .
|
|
| 13. | 详细信息 |
|
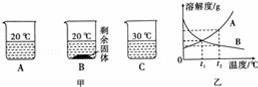
向装有等质量水的A、B、C烧杯中分别加入10g、25g、25g的NaNO3固体,充分溶解后如图甲所示.
(1)烧杯中溶液一定属于饱和溶液的是 (填序号); (2)图乙中能表示NaNO3溶解度曲线的是 (填“A”或“B”); (3)由图乙分析,若将100gB的饱和溶液从t2℃降温到t1℃,溶液的溶质质量分数 (填“增大”、“减小”或“不变”) (4)实验室配置100g 16%的硝酸钠溶液,下列做法正确的是 (填序号) A.计算:需要16g硝酸钠,100g水 B.称量:用托盘天平称量所需的硝酸钠 C.量取:用50mL量筒量取所需的水 D.溶解:将称得的硝酸钠倒入量筒溶解.
|
|
| 14. | 详细信息 |
|
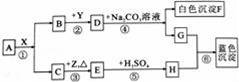
如图是初中化学常见几种物质的转化关系图(个别产物略去).其中A、B常温下均为液态,且组成元素相同.F是大理石的主要成分.X、Y为氧化物,Z是紫红色固体.请回答下列问题. (1)写出物质A的化学式: . (2)在反应①中,物质X起 作用. (3)反应⑥的化学方程式为: . (4)反应①~⑥涉及的基本反应类型共有 种.
|
|
| 15. | 详细信息 |
|
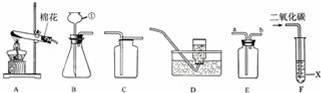
A~F是实验室制取、收集、验证气体的常见装置图,请根据装置图回答.
(1)写出图中仪器①的名称 . (2)若用A、D组合制取实验室的一种气体,发生装置中需装入的药品是(填化学式). (3)实验室用B、E、C装置制取并收集干燥的二氧化碳,则E中应盛放的试剂是 (填名称). (4)图F中若X是石蕊试液,能观察到的现象是 .若X是澄清石灰水,写出发生反应的化学方程式 .
|
|
| 16. | 详细信息 | ||||||||||||
|
食品包装中常使用一种袋装为“504双吸剂”防腐剂,标签如图所示.作用:防潮、防氧化.双吸剂变质失效后,固体中大部分是灰白色的,少许是红棕色的.甲、乙、丙三位同学对一包久置的“双吸剂”的变质情况进行探究. 【提出问题】变质后,固体成分中有什么物质?颜色有什么变化? 【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁,氧化铁粉为红棕色. 【作出猜想】变质后的固体成分中可能含有:Fe、CaO、Fe2O3、Ca(OH)2、CaCO3. 【分析猜想】根据“双吸剂”的作用:防潮、防氧化.由此说明“双吸剂”成分中的物质可吸收 和 两种物质,从而可防止食品腐败. 【实验探究】三位同学的探究方案如下表.
【反思应用】 (1)综合上述探究,请分析甲、乙、丙的实验结论中,不合理的是 . (2)采取什么实验方法可以使失效后的红棕色粉末“还原”?(用化学方程式表示) .
|
|||||||||||||
| 17. | 详细信息 |
|
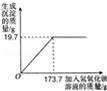
为测定氢氧化钠固体样品的变质程度,化学兴趣小组的同学进行了如下实验:称取20.0g固体样品放入烧杯中,逐渐加入氢氧化钡溶液至不再产生沉淀为止,过滤后,得到一定质量的滤液和沉淀,并绘制加入氢氧化钡溶液质量与产生沉淀的关系如图所示,请解答下列问题: (1)写出氢氧化钠发生变质的化学方程式: . (2)样品中碳酸钠的质量分数?(写出必要的计算过程)如果实验中称得的沉淀质量偏小,那么计算出的样品中碳酸钠的质量分数 (填“偏大”、“偏小”或“不变”). (3)所得滤液中溶质的质量分数.
|
|
 B.
B.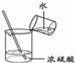
 C.
C.
 D.
D.