2020人教版初中化学专题练习
| 1. | 详细信息 |
|
取氯酸钾和二氧化锰的混合物17.5g,放入一大试管中加热,完全反应后冷却到反应前温度,称残余固体质量为12.7g。求: (1)生成氧气________g。 (2)生成氯化钾的质量是多少__________?
|
|
| 2. | 详细信息 |
|
某学校化学兴趣小组的同学为测定某石灰石样品(其中杂质不溶于水且不与稀盐酸反应)中碳酸钙的质量分数,称取12g样品做了下述实验,请根据下图所示的实验过程和提供的数据,计算:
(1)该石灰石样品中碳酸钙的质量分数。 (2)反应后所得溶液的质量分数。
|
|
| 3. | 详细信息 |
|
维生素C的化学式为C6H8O6,关于“C6H8O6”表示的意义,四名同学表达了四种说法:①表示维生素C这种物质;②表示一个维生素C分子;③表示维生素C由……;④表示每个维生素C分子由……。 请你将说法③、说法④省略的部分填写在横线上。 说法③:表示维生素C由_______________________________组成。 说法④:表示每个维生素C分子由_______________________________构成。
|
|
| 4. | 详细信息 |
|
用化学符号表示: (1)碳元素 ; (2)2个钙离子 ; (3)氯化铝 ; (4)氧化铜中铜元素化合价为+2价 。
|
|
| 5. | 详细信息 |
|
科学家发现,中草药成分中提取的“汉防己碱”能有效避免病毒进入细胞,有助于预防埃博拉感染,其分子式为C38H42N2O6。请回答: (1)汉防己碱属于 (填“无机物”或“有机物”); (2)汉防己碱由 种元素组成,分子中氢、氧的原子个数比为 (填最简比); (3)汉防己碱中 元素的质量分数最小。
|
|
| 6. | 详细信息 |
|
下列是初中化学中的一些重要实验,请回答:
|
|
| 7. | 详细信息 |
|
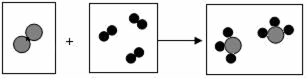
如图是某化学反应的微观示意图,“○”和“●”分别表示不同的原子,请根据图示回答下列问题.
(1)一个丙分子由 个原子构成;由大量丙分子聚集成的丙物质 (填“可能”或“不可能”)是氧化物. (2)甲分子与乙分子化学性质不同的原因是 . (3)该反应的基本反应类型是 . (4)参加反应的甲和乙的分子个数比是 .
|
|
| 8. | 详细信息 |
|
抗病毒处方药磷酸奥可他韦能够有效治疗甲型和乙型流感,分子式为C16H28N2O4•H3PO4下列说法正确的是( ) A.分子式中含7种元素 B.C16H28N2O4中C、O元素的质量比为4:1 C.H3PO4由3个氢原子、1个磷原子、4个氧原子构成的 D.H3PO4和H2SO4的相对分子质量相同
|
|
| 9. | 详细信息 |
|
对下列化学用语中“2所表示意义的理解中,错误的是( ) A.Fe2+中的“2表示一个亚铁离子带两个单位正电荷 B.2NH3中的“2”表示两个氨分子 C. D.2O中的“2”表示两个氧元素
|
|
| 10. | 详细信息 |
|
正确的实验操作是学习化学的基础,下列操作正确的是( )
|
|
| 11. | 详细信息 |
|
我国成功研究出一种由质量数为18的氧原子构成的双原子分子气体,下列说法正确的是( ) A.这种原子的核外不一定有8个电子 B.这种气体的分子中含16个电子,相对分子质量为36 C.这种气体里氧元素的化合价不为零 D.若这种原子和氢原子构成水分子,其相对分子质量是18
|
|
| 12. | 详细信息 |
|
下列化学用语书写正确的是( ) A.两个钙离子:2Ca+2 B.氧化铝:AlO C.两个氢原子:H2 D.过氧化氢中氧元素的化合价:
|
|
| 13. | 详细信息 |
|
茶叶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46 下列说法错误的是( ) A.单宁酸由碳、氢、氧三种元素组成 B.一个单宁酸分子中有76个碳原子、52个氢原子和46个氧原子 C.单宁酸是有机高分子化合物 D.单宁酸中氢元素的质量分数最小
|
|
| 14. | 详细信息 |
|
下列化学用语书写正确的是( ) A.氧气中氧元素的化合价: C.碳酸钠:NaCO3 D.4个铍原子:4Be
|
|
| 15. | 详细信息 |
|
下列化学用语书写正确的是( ) A.银元素——AG B.3个氧原子——O3 C.4个水分子——4H2O D.镁离子——Mg+2
|
|
| 16. | 详细信息 |
|
某反应的微观示意图如图,用“
A.该反应属于化合反应 B.反应前后原子的种类不发生变化 C.反应前后物质的化学性质不发生变化 D.该反应的化学方程式表示为A2+3B2═2AB3
|
|
| 17. | 详细信息 |
|
200多年前,法国化学家拉瓦锡用定量方法研究空气成分,其中一项实验是加热红色氧化汞粉末得到汞和氧气,反应的微观示意图如图所示。该项实验( )
A.可说明分子质量大、原子质量小 B.可说明原子不能保持物质的化学性质 C.氧化汞由一个汞原子和一个氧原子构成 D.所得氧气与原空气中的氧气化学性质相同
|
|
| 18. | 详细信息 |
|
下列应用或相应原理(用化学方程式表示)都正确的是 ( ) A.实验室制取氧气 2KMnO4 △ K2MnO2+MnO2+O2↑ B.探究铁和铜的金属活动性 2Fe+3CuSO4====Fe2(SO4) 3+3Cu C.用稀盐酸洗出试管壁上的铜 Cu+2HCl===CuCl2+ H2↑ D.焦炭还原氧化铁 3C+2Fe2O3 高温 4Fe+3CO2↑
|
|
| 19. | 详细信息 |
|
对于三个化学反应相同点的比较叙述正确的是( ) 2Mg + O2 ①反应条件都是点燃 ②都是化合反应 ③都是单质与氧气发生的反应 ④反应物的物质的量之比都为2:1 ⑤都是氧化反应 A.①②⑤ B.②③④ C.①②④⑤ D.①④⑤
|
|
| 20. | 详细信息 |
|
二硫化碳(CS2)燃烧的化学方程式为:CS2 + 3O2 A.SO2 B.SO3 C.S2O6 D.S
|
|
| 21. | 详细信息 |
|
将一定量的乙醇(C2H5OH)和O2放入一密闭容器中引燃,测得反应前后各物质的质量如下表:
下列判断错误的是 ( ) A.表中Y的值为5.4 B.在该反应中,生成水和二氧化碳的分子个数比为3:2 C.该反应是氧化反应 D.若起始时氧气的质量为9.6g,则无CO生成
|
|
| 22. | 详细信息 |
|
化学反应中不发生改变且能解释质量守恒定律原理的是下列①~⑥中的( ) ①物质种类; ②分子种类; ③分子数目; ④原子种类; ⑤原子数目;⑥原子质量. A.① B.②③ C.④⑤⑥ D.①②③④⑤⑥
|
|
| 23. | 详细信息 |
|
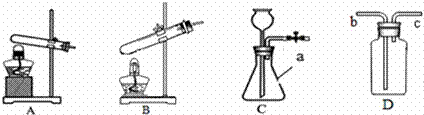
如图是初中化学常用来制取气体的装置,请根据要求回答下列问题
(1)仪器a的名称是______________ (2)实验室用加热氯酸钾和二氧化锰的方法制氧气,选用的发生装置是___(填装置字母),反应的化学方程式为________________,若将装置D盛满水来收集氧气,则氧气应从导管___(填“b”或“c”)端通入 (3)实验室常用锌粒和稀硫酸制取氢气,可选用装置C作为发生装置,检验该装置气密性的方法是:用止水夹夹住导管右端的乳胶管,向长颈漏斗中加水,如果一段时间后_____________,则说明装置气密性良好。
|
|
| 24. | 详细信息 |
|
物质甲、乙与盐酸的关系如图9所示(“→”表示一种物质经过一步反应生成另一种物质;“—”表示相连物质间一定发生反应;“---”表示相连物质间可能发生反应、也可能不发生反应)。
⑴若甲乙属于不同类别的含钠化合物,且盐酸能与乙反应则乙是______(写化学式);“甲—盐酸”反应的化学方程式为__________________。 ⑵若甲为硝酸银溶液,乙是难溶于水的物质 ① 若盐酸不与乙反应,则乙为__________(写化学式)。 ② 若盐酸能与乙反应,则“甲→乙”反应的化学方程式为______________。 (3)若甲、乙均为金属单质,甲可以转化为乙,且乙不与盐酸反应,则甲、乙在金属活动性顺序中的位置关系是_________________________
|
|
| 25. | 详细信息 |
|
实验室有一固体混合物,可能含有Fe2O3、Cu、C、NH4HCO3、NH4Cl、(NH4)2SO4等物质中的几种,设计以下流程进行检验:(已知:Fe2(SO4)3+Cu === CuSO4+2FeSO4)。
(1)由操作①推知,固体混合物中一定没有_______________________(填名称)。 (4)由操作⑥⑦推知,固体A含有的物质是_______________(填化学式);操作⑦反应生成红色固体的化学方程式为___________________。
|
|





 CO2 + 2 X
CO2 + 2 X