2017жұҹиӢҸд№қе№ҙзә§дёӢеӯҰжңҹиӢҸж•ҷзүҲеҲқдёӯеҢ–еӯҰжңҹдёӯиҖғиҜ•
| 1. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еұһдәҺзәҜеҮҖзү©зҡ„жҳҜВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В AпјҺж¶ІжҖҒж°§В В В В В В В В BпјҺеҠ зўҳзӣҗВ В В В В В В В CпјҺзҹізҒ°ж°ҙВ В В В В В В В В DпјҺдёҚй”Ҳй’ў
|
|
| 2. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еұһдәҺзү©зҗҶеҸҳеҢ–зҡ„жҳҜВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В AпјҺз”өжұ ж”ҫз”ө В В В В В В BпјҺйЈҹзү©еҸҳиҙЁВ В В В В В CпјҺжө·ж°ҙи’ёйҰҸВ В В В В В В DпјҺз”ҹй“ҒзӮјй’ў
|
|
| 3. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҢ–еӯҰз”ЁиҜӯй”ҷиҜҜзҡ„жҳҜ В В AпјҺе°ҸиӢҸжү“вҖ”NaHCO3В В В В В В В В В В В В В В В В В BпјҺзўҳй…’дёӯжә¶иҙЁвҖ”I В В CпјҺз”ҹзҹізҒ°вҖ” CaO В В В В В В В В В В В В В В В В В В В В В DпјҺй•ҒзҰ»еӯҗвҖ”Mg2+
|
|
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—иҜҙжі•й”ҷиҜҜзҡ„жҳҜВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В AпјҺйҒ“и·Ҝжҙ’ж°ҙпјҢеҮҸе°‘жү¬е°ҳВ В В В В В В В В В В В В В В BпјҺе…¬дәӨеҮәиЎҢпјҢдҪҺзўіз”ҹжҙ» CпјҺйҮ‘еұһеӣһ收пјҢиө„жәҗеҶҚз”ҹ В В В В В В В В В В В В В В В DпјҺж·ұеҹӢз”өжұ пјҢж¶ҲйҷӨжұЎжҹ“
|
|
| 5. | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||
|
дёӢеҲ—еҪ’зұ»й”ҷиҜҜзҡ„жҳҜВ В В В В В В В В В В В В В В В В В В В В В В В В В
|
||||||||||||||||
| 6. | иҜҰз»ҶдҝЎжҒҜ |
|
е®һйӘҢе®ӨеҲ¶еҸ–H2пјҢ并еҲ¶еӨҮZnSO4вҖў7H2Oжҷ¶дҪ“зҡ„е®һйӘҢж“ҚдҪңжңүй”ҷиҜҜзҡ„жҳҜВ В В В В В В В В В В В В В В В В В В В В В В AпјҺиЈ…зҪ®з”ІпјҡеҲ¶еҸ–ж°ўж°”В В В В В В В В В В В В В В В В В BпјҺиЈ…зҪ®д№ҷпјҡ收йӣҶж°ўж°” CпјҺиЈ…зҪ®дёҷпјҡеӣһ收иҝҮйҮҸзҡ„й”ҢВ В В В В В В В В В В В В DпјҺиЈ…зҪ®дёҒпјҡи’ёе№Іж»Өж¶Іеҫ—еҲ°зЎ«й…ёй”Ңжҷ¶дҪ“
|
|
| 7. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||||||||||||||||
|
BпјҺзү©иҙЁзҡ„жә¶и§ЈжҖ§пјҡ
|
|||||||||||||||||||||||||||||
| 8. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—е®һйӘҢи®ҫи®ЎжӯЈзЎ®зҡ„жҳҜВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В AпјҺз”Ёжө“зЎ«й…ёе№ІзҮҘNH3В В В В В В В В В В В В В В В В В BпјҺеҠ зғӯеҢәеҲҶNaClе’ҢNH4HCO3зІүжң« В В CпјҺз”ЁиҝҮж»ӨиЈ…зҪ®е°ҶзЎ¬ж°ҙиҪҜеҢ–В В В В В В В В В В В В В DпјҺеҗ‘зӣӣж°ҙйҮҸзӯ’дёӯеҠ жө“зЎ«й…ёй…ҚеҲ¶зЁҖзЎ«й…ё
|
|
| 9. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—е®һйӘҢзҺ°иұЎжҸҸиҝ°жӯЈзЎ®зҡ„жҳҜВ В В В В В В В В В В В В В В В В В В В В В В В В В В В AпјҺзЎ«зІүзҮғзғ§дә§з”ҹж— иүІж— е‘іж°”дҪ“В В В В В В BпјҺзәўзЈ·зҮғзғ§дә§з”ҹеӨ§йҮҸзҷҪиүІзғҹйӣҫ В В CпјҺз”өи§Јж°ҙиҙҹжһҒдә§з”ҹзҡ„ж°”дҪ“иғҪиў«зӮ№зҮғВ В В В В В DпјҺй“ңзүҮжөёе…ҘзЁҖзӣҗй…ёпјҢеҪўжҲҗи“қиүІжә¶ж¶І
|
|
| 10. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеӣҫиЎЁзӨәжІ»зҗҶжұҪиҪҰе°ҫж°”еҸҚеә”зҡ„еҫ®и§ӮиҝҮзЁӢгҖӮдёӢеҲ—иҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜВ В В В В В В
В В AпјҺеӣҫдёӯзү©иҙЁжңүдёүз§Қж°§еҢ–зү©В В В В В В В В В В В BпјҺжІ»зҗҶеҗҺе°ҫж°”еҜ№зҺҜеўғжІЎжңүд»»дҪ•еҪұе“Қ В В CпјҺеҸҚеә”еүҚеҗҺжңүе…ғзҙ еҢ–еҗҲд»·ж”№еҸҳВ В В В В В В DпјҺеҸҚеә”еүҚеҗҺеҺҹеӯҗз§Қзұ»гҖҒдёӘж•°еқҮдёҚеҸҳВ В
|
|
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҢ–еӯҰж–№зЁӢејҸиғҪжӯЈзЎ®иЎЁзӨәжүҖиҝ°еҶ…е®№зҡ„жҳҜ AпјҺиҜҒжҳҺй“ңжҜ”银жҙ»жіјпјҡCu+ 2AgClпјқCuCl2+2Ag BпјҺй…ёйӣЁзҡ„еҪўжҲҗеҺҹзҗҶпјҡCO2 + H2OпјқH2CO3 CпјҺзӣҗй…ёйҷӨй“Ғй”ҲпјҲFe2O3вҖўnH2OпјүпјҡFe2O3вҖўnH2O+6HClпјқ2FeCl3+(n+3)H2O DпјҺйҷӨеҺ»H2дёӯж··жңүзҡ„HClж°”дҪ“пјҡNa2CO3 +2HClпјқ2NaCl + H2O +CO2вҶ‘
|
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҒҡжі•еҗҲзҗҶзҡ„жҳҜ В В AпјҺз”Ёж¶ІжҖҒCO2жү‘зҒӯеӣҫд№ҰйҰҶзҒ«зҒҫ В В В В В В В BпјҺз”Ёй’ўдёқзҗғж“Ұжҙ—й“қй”… В В CпјҺз”Ёзғ§зўұжІ»з–—иғғй…ёиҝҮеӨҡ В В В В В В В В В В В В В DпјҺз”ЁйЈҹзӣҗж°ҙеҺ»йҷӨж°ҙеһўВ
|
|
| 13. | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||
|
дёӢеҲ—йҷӨжқӮж–№жЎҲжӯЈзЎ®зҡ„жҳҜВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В
|
||||||||||||||||
| 14. | иҜҰз»ҶдҝЎжҒҜ | |||
|
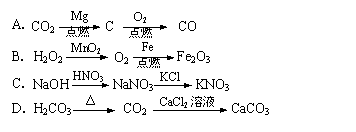
дёӢеҲ—иҪ¬еҢ–дёӯпјҢиғҪе®Ңе…Ёе®һзҺ°зҡ„дёҖз»„жҳҜ
|
||||
| 15. | иҜҰз»ҶдҝЎжҒҜ |
|
е·ІзҹҘзўій…ёж°ўй’ еҸ—зғӯжҳ“еҲҶи§ЈпјҢиҖҢзўій…ёй’ зғӯзЁіе®ҡжҖ§еҘҪгҖӮеҸ–зўій…ёж°ўй’ е’Ңзўій…ёй’ зҡ„ж··еҗҲзү©10.0gпјҢеҠ зғӯеҲ°еӣәдҪ“иҙЁйҮҸдёҚеҶҚж”№еҸҳдёәжӯўпјҢеҫ—еү©дҪҷеӣәдҪ“6.9gпјҺдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜ AпјҺеү©дҪҷеӣәдҪ“дёәж··еҗҲзү©В BпјҺеҸҚеә”еҗҺз”ҹжҲҗCO2зҡ„иҙЁйҮҸдёә3.1g CпјҺеҺҹж··еҗҲзү©дёӯNaHCO3е’ҢNa2CO3иҙЁйҮҸжҜ”дёә21:29 В В DпјҺеҸҚеә”еүҚеҗҺзҡ„еӣәдҪ“еҲҶеҲ«дёҺзӣёеҗҢжө“еәҰзЁҖзӣҗй…ёжҒ°еҘҪе®Ңе…ЁеҸҚеә”жүҖйңҖзӣҗй…ёиҙЁйҮҸзӣёеҗҢ
|
|
| 16. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҗ„з»„жә¶ж¶ІпјҢдёҚз”Ёе…¶д»–иҜ•еүӮе°ұдёҚиғҪйүҙеҲ«зҡ„жҳҜВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В AпјҺMgSO4 В BaCl2 В Na2CO3 В В Na2SO4В В В В В BпјҺNa2SO4В В BaCl2В В Na2CO3В HCl CпјҺFeCl3 В В В HCl В В NaOHВ В В KNO3В В В В В В DпјҺBa(OH)2В Na2SO4В CuCl2В В В MgCl2
|
|
| 17. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В AпјҺжҙ—жҙҒзІҫжҙ—еҺ»йӨҗе…·дёҠзҡ„жІ№жұЎпјҢеҲ©з”Ёе…¶д№іеҢ–дҪңз”Ё BпјҺдёҚйҘұе’Ңжә¶ж¶ІиҪ¬еҸҳжҲҗйҘұе’Ңжә¶ж¶ІпјҢжә¶иҙЁиҙЁйҮҸеҲҶж•°дёҖе®ҡеўһеӨ§ CпјҺжҹҗеҢ–иӮҘеҠ зҶҹзҹізҒ°з ”зЈЁжңӘй—»еҲ°ж°ЁиҮӯе‘іпјҢиҜҘеҢ–иӮҘдёҖе®ҡдёҚжҳҜж°®иӮҘ DпјҺзҮғзқҖзҡ„жңЁжқЎдјёе…ҘйӣҶ气瓶дёӯзҶ„зҒӯпјҢиҜҙжҳҺ瓶дёӯж°”дҪ“дёҖе®ҡжҳҜдәҢж°§еҢ–зўі
|
|
| 18. | иҜҰз»ҶдҝЎжҒҜ | |||
|
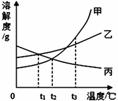
еҰӮеӣҫжҳҜз”ІгҖҒд№ҷгҖҒдёҷдёүз§ҚеӣәдҪ“зү©иҙЁзҡ„жә¶и§ЈеәҰжӣІзәҝпјҢдёӢеҲ—еҸҷиҝ°жӯЈзЎ®зҡ„жҳҜ
|
||||
| 19. | иҜҰз»ҶдҝЎжҒҜ |
|
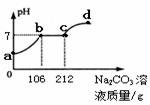
еҗ‘зӣҗй…ёдёҺж°ҜеҢ–й’ҷзҡ„ж··еҗҲжә¶ж¶ІдёӯйҖҗж»ҙж»ҙе…ҘиҙЁйҮҸеҲҶж•°10%зҡ„зўій…ёй’ жә¶ж¶ІиҮіиҝҮйҮҸгҖӮи®°еҪ•
В В В AпјҺabж®өеҸҚеә”жңүзҷҪиүІжІүж·Җз”ҹжҲҗ В В В В В В BпјҺbзӮ№жүҖеҫ—жә¶ж¶Ідёӯжә¶иҙЁдёәNaClе’ҢCaCl2 В CпјҺbcж®өжә¶ж¶ІиҙЁйҮҸеўһеҠ 106gВ В В В В В В В В DпјҺbгҖҒcгҖҒdзӮ№жә¶ж¶ІдёӯNaClиҙЁйҮҸе…ізі»пјҡm(d)=m(c)=2m(b)
|
|
| 20. | иҜҰз»ҶдҝЎжҒҜ | |||
|
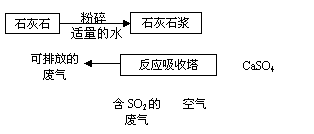
е·ҘдёҡдёҠз”ЁзҹізҒ°зҹіжөҶеҗёж”¶еәҹж°”дёӯзҡ„дәҢж°§еҢ–зЎ«пјҢ并еҲ¶еҸ–зҹіиҶҸпјҲдё»иҰҒжҲҗеҲҶдёәзЎ«й…ёй’ҷпјүзҡ„з®Җжҳ“жөҒзЁӢеҰӮдёӢеӣҫгҖӮдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В AпјҺзЎ«е…ғзҙ еңЁеҸҚеә”еүҚеҗҺеҢ–еҗҲд»·дёҚеҸҳ BпјҺзҹізҒ°зҹіеҲ¶жҲҗжөҶзҡ„зӣ®зҡ„жҳҜеўһеӨ§жҺҘи§Ұйқўз§ҜпјҢВ В В В В В В В В В В В В В В В В В жҸҗй«ҳSO2зҡ„еҗёж”¶зҺҮ В В CпјҺиҜҘжөҒзЁӢеҸҜеҮҸе°‘дәҢж°§еҢ–зЎ«зҡ„жҺ’ж”ҫпјҢдё»иҰҒ жҳҜдёәдәҶеҮҸзј“жё©е®Өж•Ҳеә” DпјҺеҗёж”¶еЎ”дёӯеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸпјҡ2CaCO3+2SO2+O2в•җ2CaSO4+2CO2
|
||||
| 21. | иҜҰз»ҶдҝЎжҒҜ |
|
з”ЁеҢ–еӯҰз¬ҰеҸ·иЎЁзӨәпјҡ пјҲ1пјүзЎ«е…ғзҙ В в–І В пјӣВ В В В В В В В В В В пјҲ2пјү2дёӘй“ҒзҰ»еӯҗ в–І пјӣ пјҲ3пјүж°ЁеҲҶеӯҗ В В в–І В пјӣВ В В В В В В В В В пјҲ4пјүж°§еҢ–й“қ В В В в–І В гҖӮ
|
|
| 22. | иҜҰз»ҶдҝЎжҒҜ |
|
йҖүжӢ©дёӢеҲ—йҖӮеҪ“зҡ„зү©иҙЁеЎ«з©әпјҲеЎ«еӯ—жҜҚеәҸеҸ·пјүпјҡ В В В AпјҺж°§ж°”В BпјҺе№ІеҶ° В CпјҺзҶҹзҹізҒ°В DпјҺжӯҰеҫ·еҗҲйҮ‘В В EпјҺе°ҸиӢҸжү“В В FпјҺзғ§зўұВ В GпјҺжҳҺзҹҫ пјҲ1пјүеҠ©зҮғжҖ§ж°”дҪ“ В в–ІВ В В пјӣВ В В пјҲ2пјүж”№иүҜй…ёжҖ§еңҹеЈӨ В в–ІВ В В пјӣ пјҲ3пјүеҸҜдҪңеҮҖж°ҙеүӮ В в–ІВ В В пјӣВ В В пјҲ4пјүз”ЁдәҺз„ҷеҲ¶зі•зӮ№ В в–ІВ В В пјӣ пјҲ5пјүдҝқйҷ©дёқжқҗж–ҷВ в–І В В В пјӣВ В В пјҲ6пјүз”ЁдәҺдәәе·ҘйҷҚйӣЁ В в–ІВ В В гҖӮВ В В В В
|
|
| 23. | иҜҰз»ҶдҝЎжҒҜ |
|
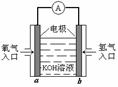
пјҲ1пјүз”өжұ е·ҘдҪңзҡ„еҸҚеә”еҺҹзҗҶпјҡВ в–ІВ В В пјҲеҶҷеҢ–еӯҰеҸҚеә”ж–№зЁӢејҸпјүпјӣ пјҲ2пјүз”өжұ е·ҘдҪңдёҖж®өж—¶й—ҙеҗҺпјҢKOHжә¶ж¶Ізҡ„pHВ в–ІВ В В пјӣ пјҲеЎ«еҸҳеӨ§гҖҒеҸҳе°ҸжҲ–дёҚеҸҳпјүгҖӮ
|
|
| 24. | иҜҰз»ҶдҝЎжҒҜ |
|
е°ҶдәҢж°§еҢ–ж°Ҝжә¶ж¶ІеҠ е…ҘеҲ°зЎ«еҢ–ж°ўпјҲH2Sпјүжә¶ж¶ІдёӯпјҢиғҪз”ҹжҲҗдёӨз§Қеёёи§Ғзҡ„й…ёгҖӮ В В В пјҲ1пјүдәҢж°§еҢ–ж°Ҝдёӯж°Ҝе…ғзҙ еҢ–еҗҲд»·дёәгҖҖв–ІВ пјӣ В В В пјҲ2пјүиҜ·еҶҷеҮәиҜҘеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸгҖҖв–ІВ гҖӮ
|
|
| 25. | иҜҰз»ҶдҝЎжҒҜ |
|
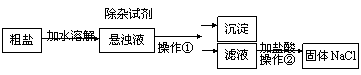
еңЁеҢ–е·Ҙз”ҹдә§дёӯпјҢйҖҡеёёйңҖиҰҒеҜ№зІ—зӣҗпјҲеҗ«жңүе°‘йҮҸзҡ„MgCl2гҖҒCaCl2гҖҒNa2SO4 жқӮиҙЁпјүпјҢиҝӣиЎҢйҷӨжқӮеӨ„зҗҶжүҚиғҪдҪҝз”ЁгҖӮдёӢеҲ—жҳҜйҷӨжқӮиҝҮзЁӢзӨәж„ҸеӣҫгҖӮ
пјҲ1пјүеҠ ж°ҙжә¶и§Јж—¶з”ЁзҺ»з’ғжЈ’жҗ…жӢҢзҡ„зӣ®зҡ„жҳҜВ в–ІВ В В пјӣ пјҲ2пјүж“ҚдҪңв‘ зҡ„еҗҚз§°жҳҜВ в–ІВ В В пјӣ пјҲ3пјүеӣҫдёӯзҡ„йҷӨжқӮиҜ•еүӮдҫқж¬ЎеҠ е…ҘиҝҮйҮҸзҡ„NaOHгҖҒиҝҮйҮҸзҡ„BaCl2е’ҢиҝҮйҮҸзҡ„В в–ІВ В пјҲеЎ«еәҸеҸ·пјүпјӣ a. K2CO3В В В В В В В В В b. Na2CO3В В В В В В В c.AgNO3 пјҲ4пјүж»Өж¶ІдёӯеҠ зӣҗй…ёзҡ„зӣ®зҡ„жҳҜВ в–ІВ В гҖӮ
|
|
| 26. | иҜҰз»ҶдҝЎжҒҜ |
|
жңүдёҖеҢ…зҷҪиүІеӣәдҪ“пјҢеҸҜиғҪеҗ«жңү NaOH гҖҒNaCl гҖҒK2SO4гҖҒNa2CO3гҖҒCuSO4дёӯзҡ„еҮ з§ҚгҖӮдёәзЎ®е®ҡе…¶з»„жҲҗпјҢиҝӣиЎҢдёӢеҲ—е®һйӘҢгҖӮиҜ·ж №жҚ®е®һйӘҢзҺ°иұЎеҲӨж–ӯпјҡ пјҲ1пјүеҸ–иҜ•ж ·жә¶дәҺж°ҙпјҢеҫ—ж— иүІжҫ„жё…жә¶ж¶ІAпјҢеҲҷжӯӨеӣәдҪ“дёӯдёҖе®ҡжІЎжңүгҖҖв–ІВ пјӣ пјҲ2пјүжә¶ж¶ІAдёӯеҠ е…Ҙи¶ійҮҸBa(NO3)2жә¶ж¶ІпјҢдә§з”ҹзҷҪиүІжІүж·ҖBпјҢдёҠеұӮжё…ж¶Ідёӯж»ҙеҠ й…ҡй…һеҸҳзәў еҲҷжӯӨеӣәдҪ“дёӯдёҖе®ҡеҗ«жңүгҖҖв–ІВ пјӣ пјҲ3пјүеҸ–зҷҪиүІжІүж·ҖBеҠ е…ҘиҝҮйҮҸзҡ„зЁҖзЎқй…ёпјҢжІүж·ҖйғЁеҲҶж¶ҲеӨұгҖӮ еҲҷеҺҹеӣәдҪ“дёӯдёҖе®ҡиҝҳеҗ«жңүгҖҖв–ІВ гҖҒгҖҖв–ІВ гҖӮеҶҷеҮәжІүж·Җжә¶и§Јзҡ„еҢ–еӯҰж–№зЁӢејҸгҖҖв–ІВ В гҖӮ
|
|
| 27. | иҜҰз»ҶдҝЎжҒҜ | |||
|
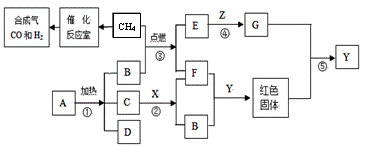
дёӢеӣҫиЎЁзӨәжҹҗдәӣзү©иҙЁй—ҙиҪ¬еҢ–е…ізі»гҖӮеӣәдҪ“AгҖҒDз»„жҲҗе…ғзҙ зӣёеҗҢпјҢдё”Aдёәзҙ«й»‘иүІпјҢCгҖҒZдёәй»‘иүІзІүжң«пјҢBгҖҒEгҖҒGдёәж°”дҪ“пјӣXдёҺFжҳҜз»„жҲҗе…ғзҙ зӣёеҗҢзҡ„ж— иүІж¶ІдҪ“пјӣеҸҚеә”в‘Өеёёз”ЁжқҘзӮјй“ҒгҖӮеӣһзӯ”дёӢеҲ—й—®йўҳпјҡ
пјҲ1пјүAзҡ„еҢ–еӯҰејҸжҳҜВ В в–ІВ В В гҖӮ пјҲ2пјүCзү©иҙЁеңЁеҸҚеә”в‘Ўдёӯзҡ„дҪңз”ЁВ В В в–ІВ гҖӮ пјҲ3пјүеҶҷеҮәеҸҚеә”в‘ЈгҖҒв‘Өзҡ„еҢ–еӯҰж–№зЁӢејҸ: в‘ЈВ В В В В В В В В В В в–І В В В В В В В В В В В пјӣв‘ӨВ В В В В В В В В В в–І В В В В В В В В В В В В гҖӮ пјҲ4пјүе°ҶEгҖҒGдёӨз§Қж°”дҪ“еҢәеҲ«ејҖжқҘпјҢеҸҜдҪҝз”Ёзҡ„дёҖз§Қжә¶ж¶ІдёәВ В В в–ІВ В В В пјҲеЎ«еҗҚз§°пјүгҖӮ пјҲ5пјүCOе’ҢH2еңЁдёҖе®ҡжқЎд»¶дёӢжҢүз…§дёҚеҗҢзҡ„жҜ”дҫӢеҸҜд»ҘеҗҲжҲҗдёҚеҗҢзҡ„еҢ–е·ҘеҺҹж–ҷпјҢиҫҫеҲ°еҺҹеӯҗеҲ©з”ЁзҺҮжңҖеӨ§зҡ„иҰҒжұӮгҖӮCOе’ҢH2д»ҘеҲҶеӯҗдёӘж•°жҜ”1вҲ¶2еҸҜд»ҘеҗҲжҲҗдёӢеҲ—зү©иҙЁдёӯзҡ„В в–І В гҖӮ AпјҺз”ІйҶҮпјҲCH4OпјүВ В BпјҺд№ҷй…ёпјҲC2H4O2пјү CпјҺд№ҷйҶҮпјҲC2H6Oпјү DпјҺз”ІйҶӣпјҲCH2Oпјү
|
||||
| 28. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||||
|
й’ҷиў«з§°дёәдәәдҪ“дёӯзҡ„вҖңй’ўзӯӢж··еҮқеңҹвҖқпјҢ гҖҗдәәдҪ“дёӯзҡ„й’ҷгҖ‘ пјҲ1пјүдәәдҪ“зјәй’ҷдёҚдјҡеҜјиҮҙВ В в–ІВ В В гҖӮ В В В В В AпјҺдҪқеҒ»з—…В В В В В В В В В BпјҺдҫҸе„’з—ҮВ В В В В В В В CпјҺйӘЁиҙЁз–Ҹжқҫ пјҲ2пјүй’ўзӯӢж··еҮқеңҹеұһдәҺВ В В В в–ІВ В В гҖӮ AпјҺж— жңәжқҗж–ҷВ В В В В В В BпјҺеҗҲжҲҗжқҗж–ҷВ В В В В В CпјҺеӨҚеҗҲжқҗж–ҷ пјҲ3пјүдәәдҪ“дёӯй’ҷе…ғзҙ дё»иҰҒеӯҳеңЁдәҺйӘЁйӘје’ҢзүҷйҪҝдёӯпјҢд»ҘзҫҹеҹәзЈ·й…ёй’ҷ[Ca10(PO4)6(OH)2]еҪўејҸеӯҳеңЁпјҢе…¶дёӯзЈ·е…ғзҙ еҢ–еҗҲд»·дёәВ В в–ІВ гҖӮ гҖҗеҚ•иҙЁй’ҷгҖ‘ жҸҗеҮәй—®йўҳпјҡй’ҷзҡ„еҢ–еҗҲзү©еҫҲеӨҡпјҢдёәд»Җд№ҲжҲ‘们еҫҲе°‘жҸҗиө·еҚ•иҙЁй’ҷе‘ўпјҹ
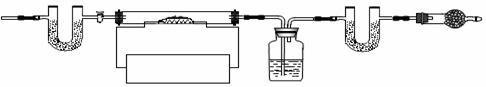
е®һйӘҢйӘҢиҜҒдёҖпјҡ жҹҘйҳ…иө„ж–ҷпјҡеңЁдёҖдёӘеҢ–еӯҰеҸҚеә”дёӯпјҢжңүе…ғзҙ еҢ–еҗҲд»·еҚҮй«ҳпјҢеҗҢж—¶е°ұжңүе…ғзҙ еҢ–еҗҲд»·йҷҚдҪҺгҖӮ пјҲ4пјүе®һйӘҢз»“и®әпјҡ в‘ еҶҷеҮәй’ҷдёҺж°ҙеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸпјҡВ В в–ІВ В В гҖӮ В В В В В В В В В В В в‘ЎиҜҘеҸҚеә”В В в–ІВ В В зғӯйҮҸгҖӮпјҲйҖүеЎ«вҖңеҗёж”¶вҖқжҲ–вҖңйҮҠж”ҫвҖқпјү гҖҗе№ІзҮҘеүӮдёӯзҡ„й’ҷгҖ‘ жҸҗеҮәй—®йўҳпјҡдёҖеҢ…з”ҹзҹізҒ°е№ІзҮҘеүӮпјҢдҪҝз”ЁдёҖж®өж—¶й—ҙеҗҺеҸҜиғҪжңүе“ӘдәӣеӣәдҪ“пјҹ зҢңжғіеҒҮи®ҫпјҡеӣәдҪ“дёӯеҗ«жңүж°§еҢ–й’ҷгҖҒж°ўж°§еҢ–й’ҷгҖҒзўій…ёй’ҷгҖӮ е®һйӘҢйӘҢиҜҒдәҢпјҡ пјҲ5пјүеҸ–еӣәдҪ“ж ·е“ҒеҠ е…Ҙж°ҙдёӯпјҢиӢҘжё©еәҰжҳҺжҳҫеҚҮй«ҳпјҢеҲҷеҗ«жңүВ В в–ІВ В В пјӣж»ҙеҠ й…ҡй…һеҗҺж¶ІдҪ“еҸҳзәўпјӣ继з»ӯеҠ и¶ійҮҸзЁҖзӣҗй…ёпјҢеҰӮи§ӮеҜҹеҲ°В В в–ІВ В В пјҢеҲҷеӣәдҪ“еҗ«жңүзўій…ёй’ҷгҖӮ пјҲ6пјүе°ҸжҳҺи®Өдёәж— жі•еҲӨж–ӯжҳҜеҗҰжңүж°ўж°§еҢ–й’ҷгҖӮзҗҶз”ұжҳҜпјҡВ В в–ІВ В В гҖӮ
AВ В В В В В В В В В В В В BВ В В В В В В В В В В В В В CВ В В В В В В В В DВ В В В В В В В В В E жҹҘйҳ…иө„ж–ҷпјҡCa(OH)2еҠ зғӯиҮі580в„ғгҖҒCaCO3еҠ зғӯиҮі825в„ғеҲҶеҲ«еҲҶи§Јз”ҹжҲҗдёӨз§Қж°§еҢ–зү©гҖӮ в‘ В е®һйӘҢеүҚйҰ–е…ҲиҰҒВ В в–ІВ В В пјҢеҶҚиЈ…е…Ҙж ·е“ҒгҖӮиЈ…зҪ®Aзҡ„дҪңз”ЁжҳҜВ В в–ІВ В В гҖӮ в‘ЎВ жҺ§жё©еҠ зғӯдҪҝиЈ…зҪ®BдёӯеҸҚеә”е®Ңе…ЁпјҢеҶҚйҖҡдёҖж®өж—¶й—ҙз©әж°”пјҢжөӢеҫ—еҸҚеә”еүҚеҗҺиЈ…зҪ®CгҖҒDеҲҶеҲ«еўһйҮҚ18.0gе’Ң22.0gпјҢеҲҷеӣәдҪ“ж ·е“ҒдёӯдёӨз§Қзү©иҙЁзҡ„иҙЁйҮҸжҜ”дёәВ В в–ІВ В В гҖӮ в‘ўВ иЈ…зҪ®Eзҡ„дҪңз”ЁжҳҜВ В в–ІВ В В гҖӮ е°ҶиЈ…зҪ®BдёӯеҸҚеә”еҗҺеү©дҪҷзҡ„еӣәдҪ“ж°§еҢ–зү©еҠ е…Ҙи¶ійҮҸж°ҙдёӯжә¶и§ЈпјҢи’ёеҸ‘жүҖеҫ—еӣәдҪ“пјҲдёҚеҗ«ж°ҙпјүеўһйҮҚ36.0gпјҢеҲҷеҺҹеӣәдҪ“ж ·е“ҒдёӯCaOзҡ„иҙЁйҮҸдёәВ В в–ІВ В В gгҖӮ
|
|||||||||||||||||
| 29. | иҜҰз»ҶдҝЎжҒҜ |
|
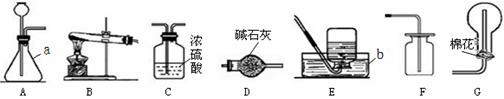
иҜ·з»“еҗҲдёӢеӣҫеӣһзӯ”й—®йўҳгҖӮ
пјҲ1пјүеҶҷеҮәеӣҫдёӯж ҮеҸ·д»ӘеҷЁеҗҚз§°a. гҖҖв–ІВ пјӣb. гҖҖв–ІВ гҖӮ пјҲ2пјүйҖүжӢ©иЈ…зҪ®E收йӣҶO2зҡ„зҗҶз”ұжҳҜгҖҖв–ІВ гҖӮ пјҲ3пјүе®һйӘҢе®ӨеҲ¶еҸ–CO2зҡ„еҢ–еӯҰж–№зЁӢејҸгҖҖв–І пјӣд»ӘеҷЁaдёӯзӣҙжҺҘеҠ е…Ҙзҡ„иҚҜе“ҒеҗҚз§°жҳҜгҖҖв–І пјӣдёҖиҲ¬йҖүжӢ©ж”¶йӣҶиЈ…зҪ® в–І пјҲйҖүеЎ«еәҸеҸ·пјүпјӣйӘҢж»Ўзҡ„ж–№жі•жҳҜгҖҖв–ІВ гҖӮ пјҲ4пјүе®һйӘҢе®ӨеҠ зғӯж°ҜеҢ–й“өе’ҢзҶҹзҹізҒ°дёӨз§ҚеӣәдҪ“зҡ„ж··еҗҲзү©жқҘеҲ¶еҸ–ж°Ёж°”гҖӮж°Ёж°”еҜҶеәҰе°ҸдәҺз©әж°”пјҢ жңүеҲәжҝҖжҖ§ж°”е‘іпјҢжһҒжҳ“жә¶дәҺж°ҙгҖӮе…¶ж°ҙжә¶ж¶ІиғҪдҪҝзҙ«иүІзҹіи•ҠиҜ•ж¶ІеҸҳдёәгҖҖв–ІВ иүІгҖӮ в‘ В еҶҷеҮәе®һйӘҢе®ӨеҲ¶еҸ–ж°Ёж°”зҡ„еҢ–еӯҰж–№зЁӢејҸгҖҖв–ІВ гҖӮ в‘Ў еҲ¶еҸ–并收йӣҶе№ІзҮҘзҡ„ж°Ёж°”пјҢеә”йҖүз”Ёзҡ„иЈ…зҪ®йЎәеәҸдёәгҖҖв–ІВ гҖӮ AпјҺAвҖ”CвҖ”GВ В В В В BпјҺBвҖ”DвҖ”EВ В В В В CпјҺBвҖ”CвҖ”GВ В В В В DпјҺBвҖ”DвҖ”G
|
|
| 30. | иҜҰз»ҶдҝЎжҒҜ |
|
е°Ҷ4cmе…үдә®й•ҒжқЎж”ҫе…ҘдёҖе®ҡйҮҸзҡ„зЁҖHC1дёӯпјҢдә§з”ҹеӨ§йҮҸж°”жіЎеҗҺеҮәзҺ°зҷҪиүІеӣәдҪ“гҖӮ е°Ҹз»„еҗҢеӯҰдёәжҺўз©¶зҷҪиүІдёҚжә¶зү©зҡ„жҲҗеҲҶиҝӣиЎҢеҰӮдёӢе®һйӘҢгҖӮ гҖҗиө„ж–ҷгҖ‘ еңЁMgCl2жә¶ж¶ІдёӯпјҢеёёжё©дёӢеҸ‘з”ҹеҸҚеә”пјҡMg + 2H2O = Mg(OH)2вҶ“+ H2вҶ‘гҖӮ гҖҗзҢңжғігҖ‘ в… пјҺз”ҹжҲҗзҡ„MgCl2иҝҮеӨҡиҖҢжһҗеҮәВ В в…ЎпјҺеҸҚеә”еҗҺжңүй•ҒзІүеү©дҪҷВ в…ўпјҺз”ҹжҲҗдәҶMg(OH)2жІүж·Җ гҖҗе®һйӘҢгҖ‘зӣёеҗҢ3ж¬Ўе®һйӘҢпјҢиҝҮж»Ө并用蒸йҰҸж°ҙжҙ—ж¶ӨеӣәдҪ“пјҢзӣҙиҮіжңҖеҗҺдёҖж¬Ўжҙ—ж¶ӨжүҖеҫ—ж»Өж¶Ідёӯж»ҙеҠ зЎқ酸银жә¶ж¶Іж— гҖҖв–ІВ пјҲеЎ«зҺ°иұЎпјүпјҢеҲҶеҲ«еҫ—еҲ°е№ІзҮҘжҙҒеҮҖеӣәдҪ“m gгҖӮ пјҲ1пјүеҜ№жҜ”е®һйӘҢпјҡе°Ҷm gеӣәдҪ“дёҺm g гҖҖв–ІВ пјҢеҲҶеҲ«еҠ е…Ҙ5 mLи’ёйҰҸж°ҙдёӯпјҢе……еҲҶжҢҜиҚЎпјҢи§ӮеҜҹеӣәдҪ“жңүж— жҳҺжҳҫеҮҸе°‘гҖӮ з»“и®әпјҡеҒҮи®ҫв… дёҚжҲҗз«ӢгҖӮ пјҲ2пјүеҸ–m gеӣәдҪ“пјҢеҠ е…ҘзЁҖзӣҗй…ёгҖӮиӢҘи§ӮеҜҹеҲ°гҖҖв–ІВ зҺ°иұЎгҖӮ з»“и®әпјҡеҒҮи®ҫв…Ўд№ҹдёҚжҲҗз«ӢгҖӮ пјҲ3пјүеҸ–m gеӣәдҪ“пјҢе…ЁйғЁжә¶дәҺзЁҖзЎқй…ёпјҢе°ҶжүҖеҫ—жә¶ж¶ІеҲҶжҲҗдёӨзӯүд»ҪгҖӮ в‘ еҗ‘дёҖд»Ҫжә¶ж¶Ідёӯж»ҙеҠ иҝҮйҮҸзҡ„NaOHжә¶ж¶ІпјҢз”ҹжҲҗдәҶ1.16gMg(OH)2жІүж·Җ; в‘Ўеҗ‘еҸҰдёҖд»Ҫжә¶ж¶Ідёӯж»ҙеҠ иҝҮйҮҸзҡ„AgNO3жә¶ж¶ІпјҢз”ҹжҲҗдәҶ2.87 gжІүж·ҖгҖӮ з»“и®әпјҡеҒҮи®ҫв…ўд№ҹдёҚжҲҗз«ӢпјҢиӢҘе·ІзҹҘзҷҪиүІеӣәдҪ“еҢ–еӯҰејҸдёә[ Mgx(OH)yВ В В z]пјҢеҲҷзјәе°‘зҡ„е…ғзҙ з¬ҰеҸ·дёәгҖҖв–ІВ гҖӮ гҖҗз»“и®әгҖ‘з»Ҹи®Ўз®—еҲҶжһҗx:z= В гҖҖв–ІВ пјҢx:y= В гҖҖв–ІВ гҖӮ иҜ·еҶҷеҮәеҫ—еҲ°зҷҪиүІеӣәдҪ“е’ҢH2зҡ„еҢ–еӯҰж–№зЁӢејҸпјҲе·ІзҹҘдёӨиҖ…и®ЎйҮҸж•°жҜ”дёә1вҲ¶2пјүпјҡгҖҖв–ІВ гҖӮ
|
|
- зҰҸе»әзңҒжіүе·һеёӮжғ е®үеҺҝжғ е®үиҚ·еұұдёӯеӯҰ2020-2021е№ҙеҲқдёүдёҠеҶҢ第дёҖж¬ЎжңҲиҖғеҢ–еӯҰиҜ•еҚ·еёҰеҸӮиҖғзӯ”жЎҲе’Ңи§Јжһҗ
- еҚ—йғЁеҺҝзӣҳйҫҷдёӯеӯҰд№қе№ҙзә§еҢ–еӯҰ2018е№ҙдёҠеҚҠе№ҙжңҲиҖғжөӢйӘҢе…Қиҙ№иҜ•еҚ·е®Ңж•ҙзүҲ
- ж–°з–Ҷд№ҢйІҒжңЁйҪҗеёӮй«ҳж–°еҢәдёӯиҖғдёҖжЁЎеҢ–еӯҰйўҳејҖеҚ·жңүзӣҠ(2019е№ҙ)
- йҳіжұҹеёӮ2019е№ҙд№қе№ҙзә§еҢ–еӯҰдёҠеҚҠжңҹжңҹжң«иҖғиҜ•иҜ•еҚ·еёҰи§ЈжһҗеҸҠзӯ”жЎҲ
- жў…е·һеёӮ2019е№ҙд№қе№ҙзә§дёҠеӯҰжңҹеҢ–еӯҰжңҲиҖғжөӢйӘҢеңЁзәҝе…Қиҙ№иҖғиҜ•
- жөҷжұҹзңҒйҮ‘еҚҺеёӮ2021е№ҙдёӯиҖғеҢ–еӯҰйўҳеёҰеҸӮиҖғзӯ”жЎҲ
- 2019-2020е№ҙеҲқдёүдёҠжңҹ第дёҖж¬ЎжңҲиҖғеҢ–еӯҰпјҲеҶ…и’ҷеҸӨеҜҹе“Ҳе°”еҸізҝјеүҚ旗第дёүдёӯеӯҰпјү
- 2017еұҠеҲқдёүдёҠеӯҰжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰиҖғиҜ•е®Ңж•ҙзүҲпјҲе№ҝдёңзңҒдёңиҺһеёӮпјү