2019дәәж•ҷзүҲеҲқдёӯеҢ–еӯҰеҚ•е…ғжөӢиҜ•
| 1. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—жңүе…із©әж°”зҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺз©әж°”зҡ„жҲҗеҲҶжҢүиҙЁйҮҸи®Ўз®—пјҢж°§ж°”еӨ§зәҰеҚ 21% BпјҺз©әж°”дёӯеҗ„жҲҗеҲҶзҡ„еҗ«йҮҸжҳҜжҒ’е®ҡдёҚеҸҳ CпјҺз©әж°”иҙЁйҮҸжҠҘе‘ҠдёӯжүҖеҲ—зҡ„з©әж°”иҙЁйҮҸзә§еҲ«и¶Ҡе°ҸпјҢз©әж°”иҙЁйҮҸи¶ҠеҘҪ DпјҺзӣ®еүҚи®Ўе…Ҙз©әж°”жұЎжҹ“жҢҮж•°зҡ„жңүе®іж°”дҪ“еҢ…жӢ¬пјҡдәҢж°§еҢ–зЎ«гҖҒдәҢж°§еҢ–зўігҖҒдәҢж°§еҢ–ж°®е’ҢиҮӯж°§зӯү
|
|
| 2. | иҜҰз»ҶдҝЎжҒҜ |
|
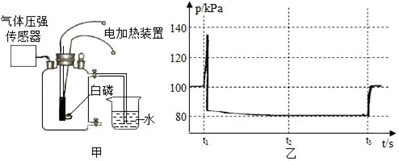
жҹҗеҗҢеӯҰеҲ©з”Ёеӣҫз”ІжүҖзӨәиЈ…зҪ®жөӢе®ҡз©әж°”дёӯж°§ж°”зҡ„еҗ«йҮҸпјҢе…¶дёӯзҮғзғ§еҢҷеҶ…зҡ„зҷҪзЈ·з”Ёз”өеҠ зғӯиЈ…зҪ®зӮ№зҮғпјҢ瓶еҶ…ж°”еҺӢз”Ёж°”дҪ“еҺӢејәдј ж„ҹеҷЁжөӢе®ҡпјҢе…¶еҸҳеҢ–еҰӮеӣҫд№ҷжүҖзӨәгҖӮеҲҷдёӢеҲ—еҲҶжһҗеҗҲзҗҶзҡ„жҳҜпјҲгҖҖгҖҖпјү
AпјҺt1ж—¶еҲ»еҗҺзҡ„дёҖж®өж—¶й—ҙиғҪи§ӮеҜҹеҲ°зҷҪзЈ·зҮғзғ§дә§з”ҹеӨ§йҮҸзҷҪиүІзғҹйӣҫ BпјҺд»Һ瓶еҶ…ж°”еҺӢиҫҫеҲ°жңҖй«ҳзӮ№зӣҙиҮіt2ж—¶еҲ»пјҢ瓶еҶ…жё©еәҰе§Ӣз»ҲдҝқжҢҒдёҚеҸҳ CпјҺж №жҚ®t2ж—¶еҲ»з“¶еҶ…зҡ„ж°”еҺӢеҖјпјҢеҸҜд»Ҙи®Ўз®—еҮәж°§ж°”еҚ з©әж°”дҪ“з§Ҝзҡ„зҷҫеҲҶжҜ” DпјҺt3ж—¶еҲ»еҗҺзҡ„дёҖж®өж—¶й—ҙеҶ…瓶еҶ…ж°”еҺӢеҸҲжҳҫи‘—еўһеҠ пјҢе…¶еҺҹеӣ жҳҜжё©еәҰеҸҲеҚҮй«ҳдәҶ
|
|
| 3. | иҜҰз»ҶдҝЎжҒҜ |
|
еӨҸж—Ҙзҡ„еҫ®йЈҺпјҢеёҰзқҖеӨ§иҮӘ然зӮҪзғӯзҡ„з”ҹе‘Ҫж°”жҒҜгҖӮз»ҸиҝҮдёүе№ҙзҡ„з”ҹзү©еӯҰд№ пјҢвҖңдәәдёҺиҮӘ然е’Ңи°җеҸ‘еұ•вҖқзҡ„зҗҶеҝөе·Іж №жӨҚдҪ зҡ„еҝғеә•гҖӮдёӢеҲ—еҸҷиҝ°дёҚз¬ҰеҗҲиҝҷдёҖзҗҶеҝөзҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺжҸҗеҖЎйӘ‘иҮӘиЎҢиҪҰжҲ–жӯҘиЎҢзҡ„ж–№ејҸеҮәиЎҢВ В В В В В В В В В В В В BпјҺе»әз«ӢиҮӘ然дҝқжҠӨеҢәпјҢдҝқжҠӨз”ҹзү©еӨҡж ·жҖ§ CпјҺејҖеҸ‘жЈ®жһ—иө„жәҗпјҢеӨҡдҪҝз”ЁдёҖж¬ЎжҖ§жңЁзӯ·В В DпјҺеҸ‘еұ•з”ҹжҖҒеҶңдёҡпјҢжҸҗй«ҳеәҹејғзү©зҡ„еҶҚеҫӘзҺҜзҺҮ
|
|
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
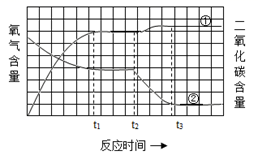
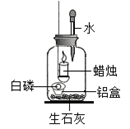
еҲ©з”ЁеҸіеӣҫиЈ…зҪ®жҺўз©¶ж°§ж°”зҡ„иҙЁйҮҸеҲҶж•°еҜ№зҮғзғ§зҡ„еҪұе“ҚгҖӮзӮ№зҮғиңЎзғӣеҗҺз«ӢеҚіеЎһзҙ§ж©Ўзҡ®еЎһпјҢеҫ…иңЎзғӣзҶ„зҒӯеҗҺпјҢе°Ҷж»ҙз®Ўдёӯзҡ„ж°ҙе…ЁйғЁж»ҙе…ҘйӣҶ气瓶дёӯпјҢй“қзӣ’дёӯзҡ„зҷҪзЈ·з«ӢеҚізҮғзғ§гҖӮе·ҰеӣҫжҳҜзүҲдёӯв‘ дәҢж°§еҢ–зўіе’Ңв‘Ўж°§ж°”зҡ„еҗ«йҮҸйҡҸж—¶й—ҙеҸҳеҢ–зҡ„еӣҫиұЎгҖӮдёӢеҲ—жңүе…іиҜҙжі•й”ҷиҜҜзҡ„жҳҜ:
AпјҺеңЁt1иҮіt2ж—¶й—ҙж®өеҶ…иңЎзғӣе·ІзҶ„зҒӯиҖҢзҷҪзЈ·иҝҳжІЎжңүејҖе§ӢзҮғзғ§ BпјҺеңЁt1иҮіt3ж—¶й—ҙж®өж°”дҪ“еҗ«йҮҸзҡ„еҸҳеҢ–жҳҜеӣ дёәзЈ·зҮғзғ§ж¶ҲиҖ—ж°§ж°”з”ҹжҲҗеӣәдҪ“ CпјҺиҜҘе®һйӘҢиҜҒжҳҺдәҶдёҚеҗҢзү©иҙЁзҡ„зҮғзғ§еҜ№ж°§ж°”зҡ„иҙЁйҮҸеҲҶж•°йңҖжұӮдёҚеҗҢ DпјҺиҜҘе®һйӘҢиҜҒжҳҺдәҶиңЎзғӣзҮғзғ§з”ҹжҲҗзҡ„дәҢж°§еҢ–зўіж°”дҪ“д»ҚиғҪж”ҜжҢҒзҷҪзЈ·зҡ„зҮғзғ§
|
|
| 5. | иҜҰз»ҶдҝЎжҒҜ |
|
дёәдәҶжөӢе®ҡз©әж°”дёӯж°§ж°”зҡ„еҗ«йҮҸпјҢжҹҗиҜҫеӨ–жҙ»еҠЁе°Ҹз»„и®ҫ计并иҝӣиЎҢдәҶеҰӮеӣҫжүҖзӨәзҡ„е®һйӘҢжҺўз©¶гҖӮдёӢеҲ—жңүе…іиҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜ(В В )
AпјҺиҜҘе®һйӘҢеҸҜз”ЁзўізІүжқҘд»Јжӣҝй“ңзІүиҝӣиЎҢжөӢе®ҡ BпјҺиҜҘе®һйӘҢж–№жі•еҲ©з”Ёзҡ„жҳҜй—ҙжҺҘжөӢйҮҸзҡ„ж–№жі• CпјҺйҖ жҲҗиҜҘе®һйӘҢеҮәзҺ°иҜҜе·®зҡ„еҺҹеӣ еҸҜиғҪжҳҜй“ңзІүзҡ„йҮҸдёҚи¶і DпјҺе®һйӘҢз»“жқҹеҗҺпјҢеҜҶй—ӯиЈ…зҪ®еҶ…еү©дҪҷж°”дҪ“зҡ„еҢ–еӯҰжҖ§иҙЁжҜ”иҫғзЁіе®ҡ
|
|
| 6. | иҜҰз»ҶдҝЎжҒҜ |
|
е°ҸиҪ©еҒҡзЎ«зҮғзғ§е®һйӘҢж—¶пјҢиҝӣиЎҢдәҶеҰӮдёӢж“ҚдҪңпјҡв‘ еңЁй“әжңүз»ҶжІҷзҡ„зҮғзғ§еҢҷйҮҢж”ҫе…Ҙе°‘йҮҸзЎ«пјӣв‘Ўе°ҶзҮғзғ§еҢҷеңЁй…’зІҫзҒҜзҒ«з„°дёҠеҠ зғӯпјҢзӣҙиҮізЎ«зҮғзғ§пјӣв‘ўе°ҶзҮғзғ§еҢҷдјёе…Ҙзӣӣжңүж°§ж°”зҡ„йӣҶ气瓶дёӯгҖӮе®һйӘҢдёӯеҸҜи§ӮеҜҹеҲ°зҡ„зҺ°иұЎдёҺз»“и®әдёҚжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺеҜ№жҜ”в‘ е’Ңв‘ЎеҸҜиҜҙжҳҺзЎ«зҮғзғ§йңҖиҰҒиҫҫеҲ°дёҖе®ҡзҡ„жё©еәҰ BпјҺеҜ№жҜ”в‘Ўе’Ңв‘ўдёӯзЎ«зҡ„зҮғзғ§зҺ°иұЎиҜҙжҳҺж°§ж°”е…·жңүеҠ©зҮғжҖ§ CпјҺеңЁв‘ЎдёӯжңүеҲәжҝҖжҖ§ж°”е‘іж°”дҪ“дә§з”ҹпјҢиҜҙжҳҺеҸ‘з”ҹдәҶеҢ–еӯҰеҸҳеҢ– DпјҺеңЁв‘ўдёӯи§ӮеҜҹеҲ°еҫ®ејұзҡ„ж·Ўи“қиүІзҒ«з„°пјҢ并жңүеӨ§йҮҸзҷҪзғҹ
|
|
| 7. | иҜҰз»ҶдҝЎжҒҜ |
|
еҰӮеӣҫжҳҜе…ідәҺж°§ж°”еҢ–еӯҰжҖ§иҙЁзҡ„йғЁеҲҶзҹҘиҜҶзҪ‘з»ңпјҢе…ідәҺиҜҘеӣҫиҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү
AпјҺIгҖҒв…ЎдёӨзұ»еҸҚеә”еқҮдҪ“зҺ°дәҶж°§ж°”зҡ„ж°§еҢ–жҖ§ BпјҺFeеңЁIгҖҒв…ЎдёӨзұ»еҸҚеә”дёӯзҡ„дә§зү©зӣёеҗҢ CпјҺв… зұ»еҸҚеә”ж”ҫеҮәзғӯйҮҸпјҢв…Ўзұ»еҸҚеә”еҗёж”¶зғӯйҮҸ DпјҺв… гҖҒв…ЎдёӨзұ»еҸҚеә”еқҮдјҡеҸ‘е…ү
|
|
| 8. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зү©иҙЁеңЁз©әж°”жҲ–ж°§ж°”дёӯзҮғзғ§ж—¶пјҢзҺ°иұЎжҸҸиҝ°жӯЈзЎ®зҡ„жҳҜпјҲВ В пјү AпјҺй•ҒжқЎеңЁз©әж°”дёӯзҮғзғ§пјҢеҶ’еҮәжө“зғҲзҡ„й»‘зғҹпјҢж”ҫеҮәзғӯйҮҸпјҢз”ҹжҲҗй»‘иүІзІүжң« BпјҺй“ҒдёқеңЁж°§ж°”дёӯеү§зғҲзҮғзғ§пјҢзҒ«жҳҹеӣӣжә…пјҢж”ҫеҮәзғӯйҮҸпјҢз”ҹжҲҗзәўиүІзІүжң« CпјҺжңЁзӮӯеңЁж°§ж°”дёӯзҮғзғ§пјҢеҸ‘еҮәзҷҪе…үпјҢж”ҫзғӯпјҢдә§з”ҹиғҪдҪҝжҫ„жё…зҹізҒ°ж°ҙеҸҳжө‘жөҠзҡ„ж°”дҪ“ DпјҺзЎ«еңЁж°§ж°”дёӯзҮғзғ§пјҢеҸ‘еҮәеҫ®ејұзҡ„ж·Ўи“қиүІзҒ«з„°пјҢж”ҫзғӯпјҢдә§з”ҹжІЎжңүж°”е‘ізҡ„ж°”дҪ“
|
|
| 9. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||
|
жҹҗе“ҒзүҢеҠ й…¶жҙ—иЎЈзІүдҪҝз”Ёж–№жі•дёӯжҸҗзӨәпјҡз”Ёжё©ж°ҙжөёжіЎгҖӮжҹҗ科еӯҰе…ҙи¶Је°Ҹз»„еҜ№иҜҘеҠ й…¶жҙ—иЎЈзІүжҙ—ж¶Өж•ҲжһңдёҺж°ҙжё©д№Ӣй—ҙзҡ„е…ізі»иҝӣиЎҢз ”з©¶пјҢжҜҸж¬Ўе®һйӘҢжүҖйҖүзҡ„иЎЈж–ҷгҖҒеҘ¶жёҚзҡ„йҮҸгҖҒжҙ—иЎЈзІүзҡ„з”ЁйҮҸе’Ңз”Ёж°ҙйҮҸеқҮзӣёеҗҢгҖӮеңЁдёҚеҗҢж°ҙжё©жқЎд»¶дёӢпјҢжөӢеҫ—иҝҷз§ҚеҠ й…¶жҙ—иЎЈзІүйҷӨеҺ»иЎЈжңҚдёҠеҘ¶жёҚжүҖйңҖзҡ„ж—¶й—ҙпјҢе®һйӘҢз»“жһңеҰӮдёӢиЎЁжүҖзӨәпјҡ
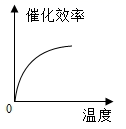
ж №жҚ®иЎЁдёӯжңүе…іж•°жҚ®еҲӨж–ӯпјҢиғҪжӯЈзЎ®иЎЁзӨәжё©еәҰеҜ№иҜҘй…¶еӮ¬еҢ–ж•ҲзҺҮеҪұе“Қзҡ„еӣҫиұЎжҳҜпјҲгҖҖгҖҖпјү AпјҺ CпјҺ
|
|||||||||||||||
| 10. | иҜҰз»ҶдҝЎжҒҜ |
|
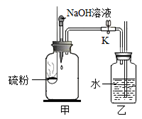
е°ҸйҮ‘з”ЁеӣҫзӨәиЈ…зҪ®иҝӣиЎҢе®һйӘҢгҖӮе·ІзҹҘпјҡ2NaOH+SO2=Na2SO3+H2OпјҺв‘ е…ій—ӯKпјҢжү“ејҖз”Ізҡ„ж©Ўиғ¶еЎһпјҢзӮ№зҮғзЎ«зІүеҗҺиҝ…йҖҹеЎһзҙ§ж©Ўиғ¶еЎһпјӣв‘ЎеҶ·еҚҙиҮіеёёжё©пјҢе°Ҷиғ¶еӨҙж»ҙз®Ўдёӯзҡ„и¶ійҮҸNaOHжә¶ж¶ІжҢӨе…Ҙ瓶дёӯпјҢжҢҜиҚЎпјҢдҪҝеҸҚеә”е……еҲҶпјӣв‘ўжү“ејҖKпјҢи§ӮеҜҹд№ҷдёӯзҡ„зҺ°иұЎгҖӮдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү
AпјҺжӯҘйӘӨ BпјҺжӯҘйӘӨ CпјҺжӯҘйӘӨ DпјҺжӯҘйӘӨ
|
|
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
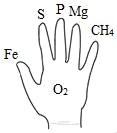
еҰӮеӣҫжҳҜе°Ҹеҫҗз”ЁжүӢжҺҢжҖ»з»“ж°§ж°”зҡ„еҢ–еӯҰжҖ§иҙЁзҡ„иЎЁзӨәж–№жі•пјҢжүӢжҢҮдёҠзҡ„зү©иҙЁиғҪдёҺжүӢжҺҢеҝғж°§ж°”еҸҚеә”гҖӮеҲҷдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜ(В )
AпјҺй“ҒеңЁз©әж°”дёӯзҮғзғ§пјҢз”ҹжҲҗеӣӣж°§еҢ–дёүй“Ғ BпјҺз…Өи„ұзЎ«зҡ„зӣ®зҡ„жҳҜеҮҸе°‘дәҢж°§еҢ–зЎ«зҡ„з”ҹжҲҗ CпјҺзЈ·зҮғзғ§дә§з”ҹеӨ§йҮҸзҡ„зҷҪйӣҫпјҢдјҡжұЎжҹ“з©әж°” DпјҺж°§ж°”зҡ„еҢ–еӯҰжҖ§иҙЁйқһеёёжҙ»жіјпјҢиғҪдёҺжүҖжңүзҡ„зү©иҙЁеҸҚеә”
|
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
|
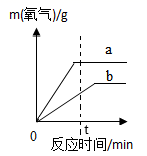
еҲҶи§ЈaгҖҒbдёӨд»ҪиҝҮж°§еҢ–ж°ўжә¶ж¶ІпјҢ并иҝӣиЎҢи®°еҪ•пјҢеҫ—еҲ°еҰӮеӣҫгҖӮдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү
AпјҺaгҖҒbдёӯиҝҮж°§еҢ–ж°ўеҗ«йҮҸзӣёеҗҢ BпјҺж—¶й—ҙдёәtж—¶пјҢaиҝҳжІЎжңүз»“жқҹеҸҚеә” CпјҺе®Ңе…ЁеҲҶи§ЈеҗҺпјҢaдә§з”ҹзҡ„ж°§ж°”жҜ”bзҡ„еӨҡ DпјҺдёәдәҶеўһеҠ bдёӯж°§ж°”зҡ„йҮҸпјҢеҸҜд»ҘйҖүжӢ©еҠ е…ҘеӮ¬еҢ–еүӮ
|
|
| 13. | иҜҰз»ҶдҝЎжҒҜ |
|
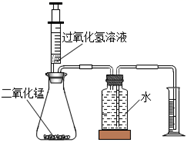
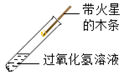
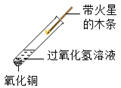
дёӢеӣҫжҳҜе®һйӘҢе®Өж°§ж°”зҡ„еҲ¶еӨҮгҖҒ收йӣҶгҖҒжЈҖйӘҢгҖҒйӘҢиҜҒжҖ§иҙЁзҡ„ж“ҚдҪңпјҢе…¶дёӯжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺ CпјҺ
|
|
| 14. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҸҷиҝ°дёӯпјҢжӯЈзЎ®зҡ„дёӘж•°жңүпјҲгҖҖгҖҖпјү в‘ з”ЁжҺ’ж°ҙ法收йӣҶж°§ж°”з»“жқҹеҗҺпјҢе…ҲзҶ„зҒӯй…’зІҫзҒҜпјҢеҶҚд»Һж°ҙдёӯжӢҝеҮәеҜјз®Ў в‘Ўе®һйӘҢе®Өз”ЁиҝҮж°§еҢ–ж°ўеҲ¶еҸ–ж°§ж°”ж—¶еҸҜд»ҘеҠ е…ҘзЎ«й…ёй“ңжә¶ж¶Ід»ҘеҠ еҝ«еҢ–еӯҰеҸҚеә”йҖҹзҺҮ в‘ўз”ЁжҺ’ж°ҙ法收йӣҶж°§ж°”еҗҺпјҢе…Ҳе°ҶйӣҶ气瓶移еҮәж°ҙж§ҪпјҢ然еҗҺзӣ–дёҠзҺ»з’ғзүҮ в‘Јж°§ж°”зҡ„з”ЁйҖ”еҫҲеӨҡпјҢжҜ”еҰӮеҸҜд»ҘеҒҡзҮғж–ҷв‘ӨеҒҡй“ҒдёқеңЁж°§ж°”дёӯзҮғзғ§зҡ„е®һи„ёж—¶йңҖиҰҒеңЁйӣҶ气瓶еә•ж”ҫе°‘йҮҸзҡ„дёҖеұӮз»ҶжІҷ AпјҺ1дёӘВ В В В В В В В В В В В В В В В В В В В В В BпјҺ2дёӘВ В В В В В В В В В В В В В В В В В В В В В CпјҺ3дёӘВ В В В В В В В В В В В В В В В В В В В В В DпјҺ4дёӘ
|
|
| 15. | иҜҰз»ҶдҝЎжҒҜ |
|
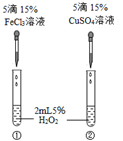
дёәжҜ”иҫғFe3+е’ҢCu2+еҜ№иҝҮж°§еҢ–ж°ўеҲҶи§ЈеҸҚеә”зҡ„еӮ¬еҢ–ж•ҲжһңпјҢжҹҗеҗҢеӯҰи®ҫи®ЎдәҶеҰӮеӣҫжүҖзӨәзҡ„е®һйӘҢпјҲFeCl3жә¶ж¶ІгҖҒCuSO4жә¶ж¶ІдёӯйғҪеҗ«жңүйҳҙйҳізҰ»еӯҗе’Ңж°ҙеҲҶеӯҗпјүпјҢжңүе…іе®һйӘҢжңүеҰӮдёӢиҜҙжі•пјҡ в‘ иҝҮж°§еҢ–ж°ўдёӯж°§е…ғзҙ зҡ„еҢ–еҗҲд»·дёә-1д»·пјӣ в‘ЎиӢҘеӣҫ1жүҖзӨәе®һйӘҢдёӯеҸҚеә”йҖҹзҺҮдёәв‘ пјһв‘ЎпјҢеҲҷдёҖе®ҡиҜҙжҳҺFe3+жҜ”Cu2+еҜ№H2O2еҲҶи§ЈеӮ¬еҢ–ж•ҲжһңеҘҪпјӣ в‘ўе®һйӘҢдёӯеҸҜйҖҡиҝҮи§ӮеҜҹдә§з”ҹж°”жіЎеҝ«ж…ўжқҘжҜ”иҫғеҸҚеә”йҖҹзҺҮпјӣ в‘Јж»ҙеҠ FeCl3жҲ–CuSO4жә¶ж¶ІеҗҺиҝҮж°§еҢ–ж°ўеҲҶи§ЈйҖҹзҺҮеҠ еҝ«пјҢеҲҷFeCl3жҲ–CuSO4жҳҜиҝҮж°§еҢ–ж°ўеӮ¬еҢ–еүӮ д»ҘдёҠиҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү
AпјҺв‘ в‘ЎВ В В В В В В В В В В В В В В В В В В В В BпјҺв‘ в‘ЈВ В В В В В В В В В В В В В В В В В В В В CпјҺв‘Ўв‘ЈВ В В В В В В В В В В В В В В В В В В В В DпјҺв‘ўв‘Ј
|
|
| 16. | иҜҰз»ҶдҝЎжҒҜ |
|
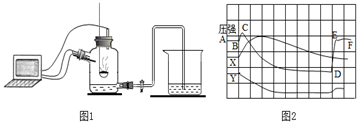
дёәдәҶжӣҙеҘҪзҡ„зҗҶи§ЈдҪҝз”ЁзҮғзғ§зәўзЈ·жі•жөӢе®ҡз©әж°”дёӯж°§ж°”еҗ«йҮҸзҡ„е®һйӘҢеҺҹзҗҶпјҢеҸҜд»ҘеҲ©з”Ёдј ж„ҹеҷЁжҠҖжңҜе®һж—¶жөӢе®ҡеӣҫ1е®һйӘҢиЈ…зҪ®еҶ…зҡ„еҺӢејәгҖҒжё©еәҰе’Ңж°§ж°”жө“еәҰеҸҳеҢ–пјҢдёүжқЎжӣІзәҝеҸҳеҢ–и¶ӢеҠҝеҰӮеӣҫ2жүҖзӨәгҖӮдёӢеҲ—еҸҷиҝ°й”ҷиҜҜзҡ„жҳҜпјҲгҖҖгҖҖпјү
AпјҺXжӣІзәҝиЎЁзӨәзҡ„жҳҜжё©еәҰеҸҳеҢ– BпјҺYжӣІзәҝиЎЁзӨәзҡ„жҳҜж°§ж°”зҡ„жө“еәҰеҸҳеҢ– CпјҺеӣҫ2дёӯCDж®өеҜ№еә”зҡ„еҸҳеҢ–иҝӣзЁӢжҳҜзәўзЈ·зҮғзғ§ DпјҺеӣҫ2дёӯDEж®өеҜ№еә”зҡ„еҸҳеҢ–иҝӣзЁӢжҳҜж°ҙеҖ’еҗёиҝӣе№ҝеҸЈз“¶
|
|
| 17. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||
|
жҹҗж ЎеӯҰз”ҹеңЁеҒҡж°§ж°”зҡ„жҖ§иҙЁе®һйӘҢж—¶пјҢеҘ№е°ҶеёҰзҒ«жҳҹзҡ„жҹҗз§ҚжқҗиҙЁе°ҸжңЁжқЎжҸ’е…Ҙзӣӣ满氧气氧气瓶дёӯпјҢеҸ‘зҺ°жңЁжқЎеӨҚзҮғпјҢеҸ–еҮәеҗ№зҒӯеҗҺпјҢеҶҚж¬Ўе°Ҷе°ҶеёҰзҒ«жҳҹжңЁжқЎжҸ’е…ҘпјҢеҸ‘зҺ°е°ҸжңЁжқЎеҸҲиғҪеӨҚзҮғпјҢеӨҡж¬ЎйҮҚеӨҚдёҠиҝ°ж“ҚдҪңеҗҺеҸ‘зҺ°пјҢжңЁжқЎжңҖеҗҺдёҚеҶҚеӨҚзҮғгҖӮдәҺжҳҜеҘ№дёҺе°ҸжқҺзӯүе…¶д»–еҗҢеӯҰеҶіе®ҡжҺўз©¶иғҪдҪҝеёҰзҒ«жҳҹзҡ„иҜҘз§ҚжқҗиҙЁзҡ„жңЁжқЎеӨҚзҮғжүҖйңҖж°§ж°”зҡ„жңҖе°‘зҡ„дҪ“з§ҜеҲҶж•°гҖӮпјҲеҒҮи®ҫжӯӨж—¶з©әж°”дёӯж°®ж°”гҖҒж°§ж°”зҡ„дҪ“з§ҜеҲҶж•°еҲҶеҲ«дёә79%гҖҒ21%пјүе®һйӘҢжӯҘйӘӨеҰӮдёӢпјҡв‘ еҸ–5дёӘеӨ§е°ҸзӣёеҗҢзҡ„йӣҶ气瓶пјҢеҲҶеҲ«зј–еҸ·дёә1гҖҒ2гҖҒ3гҖҒ4гҖҒ5пјҢ并еҲҶеҲ«дҪҝйӣҶ气瓶еҶ…з•ҷжңүеҚ йӣҶ气瓶容з§Ҝ10%гҖҒ20%гҖҒ30%гҖҒ40%гҖҒ50%зҡ„ж°ҙпјҲдҪҷдёӢдёәз©әж°”пјүпјҢз”ЁзҺ»з’ғзүҮзӣ–дҪҸпјҢ并еҖ’жүЈдәҺиЈ…жңүж°ҙзҡ„ж°ҙж§ҪдёӯгҖӮв‘ЎеҲҶеҲ«з”ЁжҺ’ж°ҙжі•еҗ‘дёҠиҝ°5дёӘйӣҶ气瓶дёӯйҖҡе…Ҙж°§ж°”пјҢе°Ҹеҝғең°жҠҠ5дёӘйӣҶ气瓶еҶ…зҡ„ж°ҙжҺ’е°ҪпјҢз”ЁзҺ»з’ғзүҮзӣ–дҪҸ瓶еҸЈпјҢеҸ–еҮәжӯЈз«Ӣж”ҫеҘҪгҖӮв‘ўеҲҶеҲ«е°ҶеёҰзҒ«жҳҹзҡ„жңЁжқЎдјёе…ҘйӣҶ气瓶дёӯпјҢи§ӮеҜҹеҲ°зҡ„зҺ°иұЎеҰӮдёӢпјҡпјҲи§ҒдёӢиЎЁпјү
пјҲ1пјүиӢҘе°ҶеёҰзҒ«жҳҹзҡ„жңЁжқЎдјёе…Ҙзј–еҸ·дёә5зҡ„йӣҶ气瓶пјҢе…¶зҺ°иұЎдёәпјҡ________________гҖӮ пјҲ2пјүжң¬е®һйӘҢиғҪеӨҹйЎәеҲ©е®ҢжҲҗпјҢиҜҙжҳҺж°§ж°”е…·жңү_____________гҖҒ_______________гҖҒ___________зҡ„жҖ§иҙЁгҖӮ пјҲ3пјүж°”дҪ“зҡ„дҪ“з§ҜеҲҶж•°жҳҜжҢҮжҹҗж°”дҪ“зҡ„дҪ“з§ҜдёҺжҖ»ж··еҗҲж°”дҪ“зҡ„дҪ“з§ҜжҜ”гҖӮе°ҶеёҰзҒ«жҳҹзҡ„жңЁжқЎдјёе…Ҙзј–еҸ·дёә4зҡ„йӣҶ气瓶еүҚпјҢ4еҸ·з“¶дёӯж°§ж°”зҡ„дҪ“з§ҜеҲҶж•°дёә_______________гҖӮпјҲжҸҗзӨәпјҡж°§ж°”зәҰеҚ з©әж°”дҪ“з§Ҝзҡ„21%пјү пјҲ4пјүе°ҸжқҺи®Өдёәе®һйӘҢеҲ°жӯӨиҝҳжІЎжңүеҫ—еҮәз»“и®әпјҢд»–еҶіе®ҡ继з»ӯиҝӣиЎҢз ”з©¶гҖӮдёәдҪҝе®һйӘҢжӣҙе…·й’ҲеҜ№жҖ§пјҢдҪ и®Өдёәд»–еә”иҜҘдҪҝйӣҶ气瓶еҶ…ж°§ж°”зҡ„дҪ“з§ҜеҲҶж•°_____________________пјҲеЎ«вҖңеӨ§дәҺвҖқжҲ–вҖңе°ҸдәҺвҖқпјү4еҸ·з“¶дёӯж°§ж°”зҡ„дҪ“з§ҜеҲҶж•°гҖӮ пјҲ5пјүиҜ•з”Ёеҫ®зІ’и§ӮзӮ№и§ЈйҮҠж°§ж°”жө“еәҰи¶ҠеӨ§пјҢеҸҚеә”и¶Ҡеү§зғҲиҝҷдёҖзҺ°иұЎпјҡ________________________гҖӮ
|
|||||||||||||
| 18. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||||||||||||||
|
жҹҗж ЎеҢ–еӯҰе…ҙи¶Је°Ҹз»„е°ұз©әж°”дёӯж°§ж°”зҡ„еҗ«йҮҸиҝӣиЎҢдәҶеҲҶз»„е®һйӘҢжҺўз©¶гҖӮ в… з»„пјҡпјҲ1пјүв… з»„еҗҢеӯҰи®Ёи®әеҗҺи®ӨдёәпјҢйҖүжӢ©зҡ„иҚҜе“Ғж—ўиҰҒиғҪж¶ҲиҖ—ж°§ж°”пјҢеҸҲдёҚдјҡи·ҹз©әж°”дёӯзҡ„е…¶д»–жҲҗеҲҶеҸҚеә”иҖҢдё”з”ҹжҲҗзү©дёәеӣәдҪ“гҖӮ他们еә”иҜҘйҖүжӢ©_________пјҲеЎ«еәҸеҸ·пјүпјҢдёәдәҶе……еҲҶж¶ҲиҖ—е®№еҷЁдёӯзҡ„ж°§ж°”пјҢиҚҜе“Ғзҡ„з”ЁйҮҸеә”дҝқиҜҒ_______________________гҖӮ
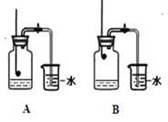
пјҲ2пјүе°Ҹз»„еҗҢеӯҰе…ұеҗҢи®ҫи®ЎдёӢеӣҫжүҖзӨәзҡ„дёӨеҘ—иЈ…зҪ®пјҢдҪ и®ӨдёәеҗҲзҗҶзҡ„жҳҜ______пјҲеЎ«еәҸеҸ·пјүгҖӮдёәдәҶзЎ®дҝқе®һйӘҢзҡ„жҲҗеҠҹпјҢеңЁиЈ…иҚҜе“Ғд№ӢеүҚеә”иҜҘ ____________________________________________гҖӮ
пјҲ3пјүеңЁи®Ёи®әзҡ„еҹәзЎҖдёҠпјҢ他们еҲҶз»„иҝӣиЎҢдәҶе®һйӘҢгҖӮ пјҲж•°жҚ®еҲҶжһҗпјүе®һйӘҢз»“жқҹеҗҺпјҢж•ҙзҗҶж•°жҚ®еҰӮдёӢпјҡпјҲжіЁпјҡйӣҶ气瓶容з§Ҝдёә100 mLпјү
пјҲ4пјүйҖҡиҝҮеҜ№е®һйӘҢз»“жһңзҡ„дәӨжөҒпјҢеӨ§еӨҡж•°еҗҢеӯҰйғҪйӘҢиҜҒеҮәж°§ж°”зәҰеҚ з©әж°”дҪ“з§Ҝзҡ„_________гҖӮ в…Ўз»„пјҡв…Ўз»„еҗҢеӯҰеҸ‘зҺ°в… з»„е®һйӘҢеҸҜиғҪдә§з”ҹе®һйӘҢиҜҜе·®пјҢеҜ№е®һйӘҢиҝӣиЎҢдәҶж”№иҝӣпјҢдёӢеӣҫжҳҜв…Ўз»„еҗҢеӯҰжөӢе®ҡз©әж°”дёӯж°§ж°”еҗ«йҮҸе®һйӘҢзҡ„дёӨеҘ—иЈ…зҪ®еӣҫпјҢиҜ·з»“еҗҲеӣҫзӨәеӣһзӯ”жңүе…ій—®йўҳгҖӮ
пјҲ1пјүж №жҚ®дёӢиЎЁжҸҗдҫӣзҡ„е®һйӘҢж•°жҚ®пјҢе®ҢжҲҗдёӢиЎЁ
пјҲ2пјүиЈ…зҪ®дёӯж°”зҗғзҡ„дҪңз”ЁжҳҜВ В В В В В В В В В В В В В В гҖӮ пјҲ3пјү иЈ…зҪ®дёҖе’ҢиЈ…зҪ®дәҢдёӯж°”зҗғзҡ„дҪҚзҪ®дёҚеҗҢпјҢВ В В В В В В (еЎ«вҖңиЈ…зҪ®дёҖвҖқжҲ–вҖңиЈ…зҪ®дәҢвҖқ)жӣҙеҗҲзҗҶпјҢзҗҶз”ұжҳҜВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В гҖӮ пјҲ4пјү еҰӮдҪ•жЈҖжҹҘиҜҘиЈ…зҪ®зҡ„ж°”еҜҶжҖ§пјҹВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В гҖӮ
|
|||||||||||||||||||||||||||
| 19. | иҜҰз»ҶдҝЎжҒҜ |
|
иҜ·ж №жҚ®дёӢеҲ—е®һйӘҢиЈ…зҪ®еӣҫеӣһзӯ”й—®йўҳпјҺ
пјҲ1пјүеҶҷеҮәд»ӘеҷЁaгҖҒbзҡ„еҗҚз§°пјҡa______пјҢb______пјҺ пјҲ2пјүз”ЁAиЈ…зҪ®еҲ¶еҸ–O2зҡ„еҢ–еӯҰж–№зЁӢејҸдёә_________________пјҢеә”йҖүз”Ёзҡ„收йӣҶиЈ…зҪ®дёә______пјҲеЎ«иЈ…зҪ®зј–еҸ·пјүпјҺз”ЁBиЈ…зҪ®еҲ¶еҸ–CO2зҡ„еҢ–еӯҰж–№зЁӢејҸдёә__________________ пјҲ3пјүеҰӮеӣҫFжҳҜвҖңй“ҒдёқеңЁж°§ж°”дёӯзҮғзғ§вҖқе®һйӘҢзҡ„ж”№иҝӣиЈ…зҪ®пјҺе®һйӘҢж—¶пјҢжү“ејҖеҲҶж¶ІжјҸж–—жҙ»еЎһпјҢйҖҡе…Ҙе№ІзҮҘж°§ж°”зәҰ10з§’пјҢеј•зҮғй“ҒдёқдёӢз«ҜзҒ«жҹҙжқҶпјҢдјёе…ҘеЎ‘ж–ҷ瓶еҶ…пјҢ并еҜ№еҮҶзҺ»з’ғз®ЎеҸЈжӯЈдёҠж–№пјҢи§ӮеҜҹеҲ°зҡ„зҺ°иұЎжҳҜпјҡ й“Ғдёқеү§зғҲзҮғзғ§пјҢ______________________пјҺж”№иҝӣеҗҺзҡ„дјҳзӮ№жҳҜ______пјҲеЎ«еәҸеҸ·пјүпјҺ в‘ ж°§ж°”ж— йңҖжҸҗеүҚеҲ¶еӨҮе’Ң收йӣҶпјҢж“ҚдҪңжӣҙж–№дҫҝ в‘ЎеЎ‘ж–ҷ瓶代жӣҝйӣҶ气瓶пјҢйҳІжӯўйӣҶ气瓶зӮёиЈӮпјҢжӣҙе®үе…Ё в‘ўиЈ…зҪ®йӣҶж°§ж°”зҡ„еҲ¶еҸ–гҖҒе№ІзҮҘе’ҢжҖ§иҙЁйӘҢиҜҒдәҺдёҖдҪ“пјҢе®һйӘҢжӣҙдјҳеҢ–
|
|
| 20. | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||||||||||||||||||||
|
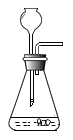
е®һйӘҢе®Өеёёз”ЁиҝҮж°§еҢ–ж°ўжә¶ж¶Іе’ҢдәҢж°§еҢ–й”°пјҲеӮ¬еҢ–еүӮпјүеҲ¶еҸ–ж°§ж°”пјҺ пјҲжҸҗеҮәй—®йўҳпјүдәҢж°§еҢ–й”°жҳҜеӮ¬еҢ–еүӮпјҢдәҢж°§еҢ–й”°зҡ„з”ЁйҮҸеҜ№еҸҚеә”йҖҹзҺҮжҳҜеҗҰжңүеҪұе“Қпјҹ пјҲи®ҫи®Ўе®һйӘҢпјүпјҲ1пјүе®һйӘҢиЈ…зҪ®еҰӮеӣҫжүҖзӨәпјҺ
пјҲ2пјүе®һйӘҢи®°еҪ•пјҡжҜҸж¬Ўз”Ё30жҜ«еҚҮ10%зҡ„иҝҮж°§еҢ–ж°ўжә¶ж¶ІпјҢйҮҮз”ЁдёҚеҗҢйҮҸдәҢж°§еҢ–й”°зІүжң«дҪңеӮ¬еҢ–еүӮиҝӣиЎҢе®һйӘҢпјҢжөӢе®ҡзӣёе…іж•°жҚ®и®°еҪ•дәҺдёӢиЎЁдёӯпјҡ
пјҲеҲҶжһҗпјүпјҲ1пјүдёҠиҝ°е®һйӘҢеә”иҜҘжөӢе®ҡзҡ„вҖңеҫ…жөӢж•°жҚ®вҖқеҸҜиғҪжҳҜ_____________пјҺ пјҲ2пјү10ж¬Ўе®һйӘҢвҖңжҜҸж¬Ўз”Ё30жҜ«еҚҮ10%зҡ„иҝҮж°§еҢ–ж°ўжә¶ж¶ІвҖқзҡ„зӣ®зҡ„жҳҜ_____________пјҺ пјҲ3пјүиӢҘ第2ж¬Ўе®һйӘҢжҜ”第3ж¬ЎиҜ•йӘҢзҡ„вҖңеҫ…жөӢж•°жҚ®вҖқжӣҙ______________пјҲеЎ«вҖңеӨ§вҖқжҲ–вҖңе°ҸвҖқпјүпјҢиҜҙжҳҺеӮ¬еҢ–еүӮзҡ„з”ЁйҮҸи¶ҠеӨҡпјҢеҸҚеә”и¶Ҡеҝ«пјҺ пјҲе®һйӘҢдёҺз»“жһңпјүз»ҸеӨҡж¬Ўе®һйӘҢиҜҒжҳҺпјҢ第1ж¬Ўе®һйӘҢиҮіз¬¬7ж¬Ўе®һйӘҢдёӯиҝҮж°§еҢ–ж°ўзҡ„еҲҶи§ЈйҖҹзҺҮдҫқж¬ЎеҠ еҝ«пјҢ第7ж¬Ўе®һйӘҢиҮіз¬¬10ж¬Ўе®һйӘҢжүҖи®°еҪ•зҡ„вҖңеҫ…жөӢж•°жҚ®вҖқж— жҳҺжҳҫе·®ејӮпјҺ пјҲз»“и®әпјү__________________пјҺ
|
||||||||||||||||||||||||||||||||||
| 21. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||||
|
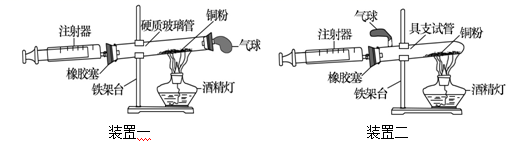
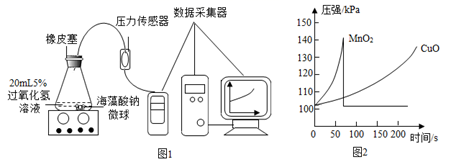
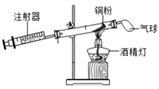
жҹҗеҢ–еӯҰе…ҙи¶Је°Ҹз»„еҜ№вҖңж°§еҢ–й“ңиғҪеҗҰдҪңиҝҮж°§еҢ–ж°ўеҲҶи§Јзҡ„еӮ¬еҢ–еүӮвҖңиҝӣиЎҢдәҶжҺўз©¶ пјҲе®һйӘҢжҺўз©¶пјү
пјҲ1пјүеҶҷеҮәе®һйӘҢв‘ЎдёӯеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸпјҡ___________________гҖӮ пјҲдәӨжөҒеҸҚжҖқпјүе®һйӘҢиҝҮзЁӢдёӯеҠ е…ҘеҲ°дёӨж”ҜиҜ•з®ЎйҮҢзҡ„иҝҮж°§еҢ–ж°ўжә¶ж¶Іеә”ж»Ўи¶ізҡ„иҰҒжұӮжңү_________________гҖӮ в‘ дҪ“з§ҜзӣёеҗҢВ В В В в‘Ўжө“еәҰзӣёеҗҢВ В В В В В в‘ўжё©еәҰзӣёеҗҢ пјҲ2пјүе°ҸжҳҺеҗҢеӯҰи®Өдёәд»…з”ұдёҠиҝ°е®һйӘҢиҝҳдёҚиғҪе®Ңе…Ёеҫ—еҮәиЎЁеҶ…зҡ„вҖңжҖ»з»“вҖқпјҢд»–иЎҘе……и®ҫи®ЎдәҶд»ҘдёӢдёӨдёӘжҺўз©¶е®һйӘҢ е®һйӘҢдёҖпјҡз§°йҮҸеҸҚеә”еҗҺеӣәдҪ“иҙЁйҮҸпјҢ并дёҺеҸҚеә”еүҚзҡ„з§°йҮҸж•°жҚ®дҪңжҜ”иҫғпјҢе…¶зӣ®зҡ„жҳҜ________________гҖӮ е®һйӘҢдәҢпјҡеҸҰеҸ–5mL5%зҡ„иҝҮж°§еҢ–ж°ўжә¶ж¶ІдәҺиҜ•з®ЎдёӯпјҢеҶҚеҗ‘е…¶дёӯеҠ е…Ҙе®һйӘҢв‘ЎеҸҚеә”еҗҺзҡ„еӣәдҪ“еү©дҪҷзү©пјҢеҰӮеӣҫ1жүҖзӨәпјҢе…¶зӣ®зҡ„жҳҜиҜҒжҳҺ_______________________гҖӮ пјҲе®һйӘҢжӢ“еұ•пјүе°ҸзәўеҗҢеӯҰз”ЁMnO2гҖҒCuOдёӨз§ҚеӮ¬еҢ–еүӮеҲҶеҲ«дёҺжө·и—»й…ёй’ жә¶ж¶Іж··еҗҲпјҢж»ҙе…Ҙж°ҜеҢ–й’ҷжә¶ж¶ІеҲ¶жҲҗеҗ«зӯүиҙЁйҮҸеӮ¬еҢ–еүӮгҖҒеӨ§е°ҸзӣёеҗҢзҡ„жө·и—»й…ёй’ еҫ®зҗғжҺўз©¶еҲҶи§ЈиҝҮж°§еҢ–ж°ўжә¶ж¶ІеҲ¶еҸ–ж°§ж°”зҡ„йҖӮе®ңеӮ¬еҢ–еүӮгҖӮ е®һйӘҢж“ҚдҪңпјҡеҸ–30зІ’еҗ«MnO2зҡ„жө·и—»й…ёй’ еҫ®зҗғпјҢйҮҮз”Ёеӣҫ1иЈ…зҪ®иҝӣиЎҢе®һйӘҢгҖӮж”№з”ЁеҸҰдёҖз§Қеҫ®зҗғпјҢеҲҶеҲ«йҮҚеӨҚдёҠиҝ°е®һйӘҢпјҢеҫ—еҲ°еӣҫ2зҡ„й”ҘеҪўз“¶еҶ…еҺӢејәйҡҸж—¶й—ҙеҸҳеҢ–зҡ„жӣІзәҝеӣҫгҖӮ
пјҲ3пјүжҜҸж¬Ўе®һйӘҢж—¶пјҢжө·и—»й…ёй’ еҫ®зҗғж•°еә”зӣёеҗҢзҡ„еҺҹеӣ жҳҜ_____________гҖӮ пјҲ4пјүз”Ёеҗ«MnO2зҡ„жө·и—»й…ёй’ еҫ®зҗғиҝӣиЎҢе®һйӘҢпјҢ60sж—¶еҺӢејәзһ¬й—ҙеӣһиҗҪпјҢе…¶еҺҹеӣ жҳҜ_______________гҖӮ пјҲ5пјүд»Һе®һйӘҢжӣІзәҝзңӢпјҢеӮ¬еҢ–ж•ҲжһңиҫғеҘҪгҖҒеҸҚеә”жё©е’Ңзҡ„еӮ¬еҢ–еүӮжҳҜ__________________гҖӮ
|
|||||||||||||||||
- 2017е№ҙйҷ•иҘҝзңҒдёӯиҖғеҢ–еӯҰйқўеҜ№йқўеҚ·и®Іи§ЈеҶҢеҲқдёүеҹәзЎҖдё“йўҳж”»з•Ҙдё“йўҳеӣӣ
- еҲқдёүдёҠеӯҰжңҹжңҹдёӯеҢ–еӯҰе…Қиҙ№иҜ•еҚ·е®Ңж•ҙзүҲпјҲ2019-2020е№ҙзҰҸе»әзңҒиҺҶз”°еёӮйғҠе°ҫгҖҒжһ«дәӯе…ӯж Ўж•ҷз ”е°ҸзүҮеҢәпјү
- еҗүе®үеёӮ2019е№ҙд№қе№ҙзә§еҢ–еӯҰеҗҺеҚҠжңҹжңҹдёӯиҖғиҜ•йҷ„зӯ”жЎҲдёҺи§Јжһҗ
- зҰҸе»әд№қе№ҙзә§еҢ–еӯҰ2018е№ҙдёӢеӯҰжңҹжңҲиҖғжөӢйӘҢеҗҢжӯҘз»ғд№
- жү¬е·һеёӮд№қе№ҙзә§еҢ–еӯҰжңҲиҖғжөӢйӘҢпјҲ2017е№ҙдёҠеҚҠжңҹпјүе®Ңж•ҙиҜ•еҚ·
- 2019еұҠеҲқдёүдёӢеҶҢдёӯиҖғжЁЎжӢҹеҢ–еӯҰйўҳејҖеҚ·жңүзӣҠпјҲеӣӣе·қзңҒжё еҺҝеҙҮеҫ·е®һйӘҢеӯҰж Ўпјү
- 2017-2018е№ҙд№қе№ҙзә§дёӢеҚҠе№ҙжңҹдёӯеҢ–еӯҰеңЁзәҝжөӢйӘҢе®Ңж•ҙзүҲпјҲжұҹиӢҸзңҒж— й”ЎеёӮжұҹйҳҙеёӮеҚ—иҸҒе®һйӘҢеӯҰж Ўпјү
- иҫҪе®Ғд№қе№ҙзә§еҢ–еӯҰжңҹжң«иҖғиҜ•пјҲ2019е№ҙдёҠеӯҰжңҹпјүйҷ„зӯ”жЎҲдёҺи§Јжһҗ

 В В В B
В В В B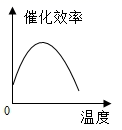 В В В В В В В В В В В В В В В В В В В В В В
В В В В В В В В В В В В В В В В В В В В В В 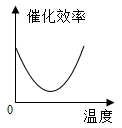 В В В D
В В В D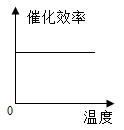
 В В B
В В B В В В В В В В В В В В В В В В В
В В В В В В В В В В В В В В В В  В В В В D
В В В В D