2016河南高三下学期人教版高中化学月考试卷
| 1. | 详细信息 |
|
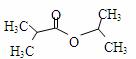
由羟基与下列基团组成的化合物中,属于醇类的是 A、 |
|
| 2. | 详细信息 |
|
下列有关日常生活中涉及到的化学知识的描述不正确的是 A.用煮面汤洗涤餐具上的油污 B.用碘水检测土豆中含有淀粉 C.用料酒清洗热水瓶中的水垢 D.利用丁达尔效应区别鸡蛋清和食盐水 |
|
| 3. | 详细信息 |
|
有机化学试剂氨基酸(如图所示)常用语制备磺胺类药物,抗癌药等。下列有关说法正确的是
A.既有酸性也有碱性 B.既能溶于水,又能溶于乙醇 C.分子内σ键与π键数目之比为1:1 D.分子内中所有原子共面 |
|
| 4. | 详细信息 |
|
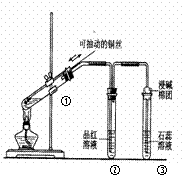
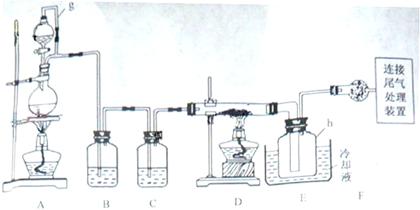
下列实验装置是探究铜丝与过量浓硫酸的反应,下列叙述不正确的是
A.装置①能控制反应的发生和结束 B.若将反应后②的试管取下,在通风橱中加热,会产生刺激性气味的气体,溶液呈红色 C.③中石蕊溶液变红色 D.为确认CuSO4生成,向①中加水,观察溶液颜色 |
|
| 5. | 详细信息 |
|
已知4 NH3+5O2=4NO+6H2O,若反应速率分别用v (NH3)、v (O2)、 v (NO)、 v (H2O)表示,则正确的关系是 A. C. |
|
| 6. | 详细信息 |
|
下列食品添加剂可作为防腐剂的是 A.味精 B.碳酸氢钠 C.苯甲酸钠 D.叶绿素 |
|
| 7. | 详细信息 |
|
19世纪末,人类开始揭开原子内部结构的秘密,最先发现电子的科学家是 A.法国化学家拉瓦锡 B.英国物理学家汤姆生 C.意大利物理学家阿伏加德罗 D.英国化学家道尔顿 |
|
| 8. | 详细信息 |
|
下列叙述中正确的是 A.最外层为2个电子的原子都是金属原子 B.电子能量越低,其运动区域离核越近 C.每个电子层作为最外层时,最多可容纳的电子数均为8 D.从Li到F、从Na到Cl,元素的最高正化合价均呈现从+1到+7价的变化 |
|
| 9. | 详细信息 |
|
用0.10 mol/L 的盐酸滴定0.10 mol/L 的氨水,滴定过程中不可能出现的结果是 A.c(NH4+)>c(Cl C.c(Cl |
|
| 10. | 详细信息 |
|
下列5个有机化合物中,能够发生酯化、加成和氧化三种反应的是( ) ①CH2=CHCOOH ②CH2=CHCOOCH3 ③CH2=CHCH2OH ④CH3CH2CH2OH ⑤CH3CH(OH)CH2CHO A.①③④ B.②④⑤ C.①③⑤ D.①②⑤ |
|
| 11. | 详细信息 |
|
在空气中久置而不易变质的物质是( ) A、过氧化钠 B、纯碱 C、硅酸钠溶液 D、亚硫酸钠 |
|
| 12. | 详细信息 |
|
NA表示阿伏加德罗常数,下列说法正确的是( ) A.在常温常压下,11.2 LN2含有的分子数为0.5 NA B.在常温常压下,1molNe含有的原子数为NA C.71gCl2所含原子数为NA D.在同温、同压下,相同体积的任何气体单质所含的原子数相同 |
|
| 13. | 详细信息 |
|
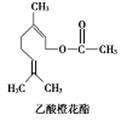
一种食用香料是乙酸橙花酯,其结构简式如图,关于该有机物的叙述中正确的是
①属于芳香族化合物 ②不能发生银镜反应 ③分子式为C12H20O2 ④它的同分异构体中可能有酚类 ⑤1 mol该有机物水解时只能消耗1 mol NaOH A.②③⑤ B.②③④ C.①②③ D.①④⑤ |
|
| 14. | 详细信息 |
|
下列各组离子一定能大量共存的是 A.在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- B.在强碱性溶液中:Na+、K+、AlO2-、CO32- C.在c(H+)=10-13mol/L的溶液中:NH4+、Al3+、SO42-、NO3- D.在pH=1的溶液中:K+、Fe2+、Cl-、NO3- |
|
| 15. | 详细信息 |
|
下列装置或操作能达到实验目的的是( )
|
|
| 16. | 详细信息 |
|
某有机物X加氢反应后的还原产物是CH3CH(CH3)CH2OH,关于X的下列说法正确的是 A.X可能是乙醛的同系物 B.X可能是正丁醇的同分异构体 C.X可能是乙烯的同分异构体 D.X分子中可能有碳碳双键 |
|
| 17. | 详细信息 |
|
在下列①~⑩中选出适宜的词语填入下列每小题的空格中(填编号): ①渗析 ②盐析 ③聚沉 ④溶胶 ⑤凝胶 ⑥布朗运动 ⑦电泳 ⑧丁达尔现象 ⑨中和 ⑩水解 (1)肥皂水中透过强光,可以见到光亮的“通路”。这种现象称为___________。 (2)在制取肥皂时,加入食盐细粒使肥皂析出,这个过程称为_____________。 (3)在肥皂水中滴加酚酞,溶液变成红色,说明高级脂肪酸根离子发生了____________。 (4)在氢氧化铁胶体中加入浓硫酸铵溶液,产生红褐色沉淀,这种现象叫做___________。 (5)用半透膜把制取的氢氧化铁胶体中含有的NaCl分离出来的方法叫做___________。 |
|
| 18. | 详细信息 |
|
铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列各题。 (1)所含铁元素既有氧化性又有还原性的物质是( )(用字母代号填)。 A.Fe B. FeCl3 C. FeSO4 D. Fe2O3
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeCl3溶液与铜反应的化学方程式:__________________;检验反应后的溶液中存在Fe3+的试剂是_____________,该反应的离子方程式为__________________________。 |
|
| 19. | 详细信息 |
|
物质结构决定物质性质。回答下列问题: A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题: (1)四种元素中电负性最大的是________(填元素符号),其中C原子的核外电子排布式为__________。 (2)单质A有两种同素异形体,其中沸点高的是__________________(填分子式);B的氢化物所属的晶体类型为________________。
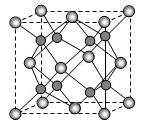
(3)化合物D2A的立体构型为_______________中心原子的杂化轨道类型为_______________。 (4)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566nm,F的化学式为_____________:列式计算晶体F的密度(g.cm-3)___________。 |
|
| 20. | 详细信息 |
|
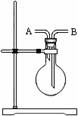
单晶硅是信息产业中重要的基础材料。通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝、硫、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450-500°C),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
|
|
| 21. | 详细信息 |
|
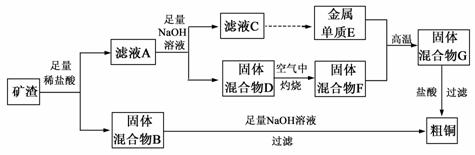
某工业矿渣中主要含有Cu2O,还有少部分Al2O3、Fe2O3、SiO2 ,从该矿渣中提取铜的操作流程如下:(已知:Cu2O+2H+═Cu+Cu2++H2O)
(1)固体混合物B与氢氧化钠溶液反应的化学方程式为 。 该反应物的一种重要用途为 。 (2)滤液A中铁元素的存在形式只能为Fe2+,理由是 。 涉及的离子方程式为(不必书写Cu2O与盐酸的反应) 、 。 检验滤液A中Fe2+的试剂为 。 (3)若将滤液C中的铝元素以沉淀形式析出,可选用的最佳试剂为 (填序号)。 A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳 金属E与固体F某一成分发生的反应可用于焊接钢轨,该反应的化学方程为 。 |
|
| 22. | 详细信息 |
|
2.7克铝与100毫升3摩尔/升的盐酸完全反应。(请写出解题过程) (1)在标准状况下放出氢气是多少升? (2)若在反应后的溶液中继续滴加350毫升1摩尔/升氢氧化钠溶液,可得沉淀多少克? |
|
| 23. | 详细信息 |
|
非诺洛芬是一种治疗类风湿性关节炎的药物,可通过以下方法合成:
请回答下列问题: 52、有机化合物B中的含氧官能团为 (填名称)。 53、上述反应中,过程②的反应类型是 反应。 54、若过程①发生的是取代反应,试剂X有弱酸性,写出由A到B发生反应的化学方程式 。 55、非诺洛芬的一种同分异构体满足下列条件: I.能与NaHCO3反应放出CO2,能与FeCl3溶液发生显色反应; II.分子中有6种不同化学环境的氢原子,且分子中含有两个苯环。 写出符合条件的一种同分异构体的结构简式: 。 56、根据已有知识并结合相关信息,写出以
|
|
| 24. | 详细信息 |
|
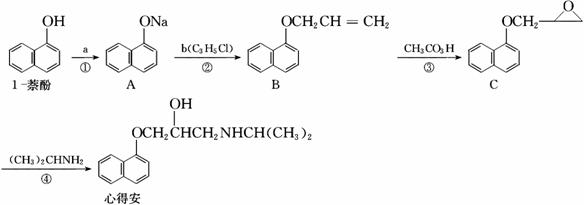
“心得安”是治疗心脏病的药物,下面是它的一种合成路线(具体反应条件和部分试剂略)。
回答下列问题: (1)试剂b的名称(系统命名法)是_________,B中官能团的名称是_________________。 (2)反应③的类型是反应_____________________。 (3)试剂b可由丙烷经三步反应合成:
反应l的试剂与条件为___________________________。X的分子中含有2种氢原子,且所含元素种类与b相同。 反应2的化学方程式为___________________________________________________。 若一次取样,检验X中所含官能团,按使用的先后顺序写出所用试剂化学式:_______________。 (4)芳香化合物D是1-萘酚的同分异构体,其分子中有两个官能团,能发生银镜反应,D分子在核磁共振氢谱图中显示4组吸收峰,则D的结构简式为_________________。 (5)以下关于心得安的说法正确的是_______________。 a.分子式为C16H20O2N b.通常状况下为固体,易溶于水 c.能使酸性高锰酸钾溶液褪色 d.能发生消去、加成、酯化、氧化反应 |
|