дәәж•ҷзүҲй«ҳдёӯеҢ–еӯҰеҗҢжӯҘз»ғд№
| 1. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—жңүе…ізЎ«зҡ„иҜҙжі•дёӯдёҚжӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) AпјҺзЎ«жҳҜдёҖз§Қж·Ўй»„иүІзҡ„дёҚжә¶дәҺж°ҙзҡ„еӣәдҪ“пјҢжңүеӨҡз§ҚеҗҢзҙ ејӮеҪўдҪ“ BпјҺзЎ«еңЁз©әж°”дёӯзҡ„зҮғзғ§дә§зү©жҳҜдәҢж°§еҢ–зЎ«пјҢеңЁзәҜж°§дёӯзҮғзғ§дә§зү©жҳҜдёүж°§еҢ–зЎ« CпјҺзЎ«еңЁз©әж°”дёӯзҮғзғ§ж—¶пјҢзҒ«з„°е‘Ҳж·Ўи“қиүІпјӣеңЁж°§ж°”дёӯзҮғзғ§ж—¶пјҢзҒ«з„°е‘Ҳи“қзҙ«иүІ DпјҺзЎ«еңЁдёҖе®ҡжқЎд»¶дёӢиғҪдёҺжҹҗдәӣйҮ‘еұһеҸҚеә”пјҢз”ҹжҲҗйҮ‘еұһзЎ«еҢ–зү© |
|
| 2. | иҜҰз»ҶдҝЎжҒҜ |
|
еҒҡе®Ңй“ңдёҺзЎ«и’ёж°”еҸҚеә”зҡ„е®һйӘҢеҗҺпјҢиҰҒйҷӨеҺ»иҜ•з®ЎеҶ…еЈҒдёҠйҷ„зқҖзҡ„зЎ«пјҢеҸҜйҮҮз”Ёзҡ„ж–№жі•жҳҜ(гҖҖгҖҖ) AпјҺз”Ёй…’зІҫжҙ—ж¶ӨгҖҖгҖҖгҖҖгҖҖВ В В В В В В В В В В В BпјҺз”Ёзӣҗй…ёжҙ—ж¶Ө CпјҺз”Ёж°ҙжҙ—ж¶Ө В В В В В В В В В В В В В В В В В В В В В DпјҺз”ЁCS2жҙ—ж¶Ө |
|
| 3. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҸҚеә”дёӯпјҢзЎ«иЎЁзҺ°иҝҳеҺҹжҖ§зҡ„жҳҜ(гҖҖгҖҖ) AпјҺзЎ«дёҺж°§ж°” В В В В В В В В В В В В В В В В В В В В В BпјҺзЎ«дёҺж°ўж°” CпјҺзЎ«дёҺй“Ғ В В В В В В В В В В В В В В В В В В В В В В В DпјҺзЎ«дёҺй“ң |
|
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
е°ҶSO2йҖҡе…ҘжҳҫзәўиүІзҡ„й…ҡй…һиҜ•еүӮдёӯпјҢеҸ‘зҺ°зәўиүІж¶ҲеӨұпјҢдё»иҰҒжҳҜеӣ дёәSO2(гҖҖгҖҖ) AпјҺжңүжјӮзҷҪжҖ§ В В В В В В В В В В В В В В В В В В В В В BпјҺжңүиҝҳеҺҹжҖ§ CпјҺжә¶дәҺж°ҙеҗҺжҳҫй…ёжҖ§ В В В В В В В В В В В В В В В DпјҺжңүж°§еҢ–жҖ§
|
|
| 5. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸдёҚжӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) AпјҺеҗ‘жҫ„жё…зҡ„зҹізҒ°ж°ҙдёӯйҖҡе…Ҙе°‘йҮҸSO2ж°”дҪ“пјҡ Ca2пјӢпјӢ2OHпјҚпјӢSO2===CaSO3вҶ“пјӢH2O BпјҺиҝҮйҮҸSO2ж°”дҪ“йҖҡе…Ҙж°ўж°§еҢ–й’ жә¶ж¶Ідёӯпјҡ SO2пјӢOHпјҚ===HSO CпјҺSO2ж°”дҪ“йҖҡе…Ҙжәҙж°ҙдёӯпјҡ SO2пјӢBr2пјӢH2O===2HпјӢпјӢ2BrпјҚпјӢSO DпјҺж°ўзЎ«й…ёдёӯйҖҡе…Ҙж°Ҝж°”пјҡH2SпјӢCl2===SвҶ“пјӢ2ClпјҚпјӢ2HпјӢ |
|
| 6. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҢ–еҗҲзү©дёҚиғҪз”Ёзӣёеә”е…ғзҙ зҡ„еҚ•иҙЁзӣҙжҺҘеҢ–еҗҲиҖҢжҲҗзҡ„жҳҜ(гҖҖгҖҖ) в‘ CuSгҖҖв‘ЎFeSгҖҖв‘ўAl2S3гҖҖв‘ЈFe2S3гҖҖв‘ӨCu2SгҖҖв‘ҘFeCl2 AпјҺв‘Ўв‘Өв‘Ҙ В В В В В В В В В В В В В В В В В В В В В В В BпјҺв‘ в‘Јв‘Ҙ CпјҺв‘ўв‘Јв‘Ө В В В В В В В В В В В В В В В В В В В В В В В DпјҺв‘ўв‘Јв‘Ҙ |
|
| 7. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) AпјҺеӣ дёәSO2е…·жңүжјӮзҷҪжҖ§пјҢжүҖд»Ҙе®ғиғҪдҪҝе“Ғзәўжә¶ж¶ІгҖҒжәҙж°ҙгҖҒKMnO4жә¶ж¶ІгҖҒзҹіи•Ҡжә¶ж¶ІиӨӘиүІ BпјҺиғҪдҪҝе“ҒзәўиӨӘиүІзҡ„дёҚдёҖе®ҡжҳҜSO2 CпјҺSO2гҖҒжјӮзҷҪзІүгҖҒжҙ»жҖ§зӮӯгҖҒNa2O2йғҪиғҪдҪҝзәўеўЁж°ҙиӨӘиүІпјҢе…¶еҺҹзҗҶзӣёеҗҢ DпјҺзӣҗй…ёиғҪдҪҝж»ҙжңүй…ҡй…һзҡ„NaOHжә¶ж¶ІиӨӘиүІпјҢиҜҙжҳҺзӣҗй…ёд№ҹжңүжјӮзҷҪжҖ§ |
|
| 8. | иҜҰз»ҶдҝЎжҒҜ |
|
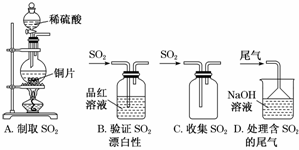
дёӢеҲ—иЈ…зҪ®дёҚиғҪе®һзҺ°зӣёеә”е®һйӘҢзӣ®зҡ„зҡ„жҳҜ(гҖҖгҖҖ)
|
|
| 9. | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||
|
з”Ё4з§Қжә¶ж¶ІиҝӣиЎҢе®һйӘҢпјҢиЎЁдёӯвҖңж“ҚдҪңеҸҠзҺ°иұЎвҖқдёҺвҖңжә¶ж¶ІвҖқдёҚз¬Ұзҡ„жҳҜ(гҖҖгҖҖ)
|
||||||||||||||||
| 10. | иҜҰз»ҶдҝЎжҒҜ |
|
е°Ҷе°‘йҮҸSO2ж°”дҪ“йҖҡе…ҘBaCl2е’ҢFeCl3зҡ„ж··еҗҲжә¶ж¶ІдёӯпјҢжә¶ж¶ІйўңиүІз”ұжЈ•й»„иүІеҸҳжҲҗжө…з»ҝиүІпјҢеҗҢж—¶жңүзҷҪиүІжІүж·Җдә§з”ҹгҖӮй’ҲеҜ№дёҠиҝ°еҸҳеҢ–пјҢдёӢеҲ—еҲҶжһҗжӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) AпјҺиҜҘе®һйӘҢиЎЁжҳҺSO2жңүжјӮзҷҪжҖ§ BпјҺзҷҪиүІжІүж·ҖдёәBaSO3 CпјҺиҜҘе®һйӘҢиЎЁжҳҺFeCl3жңүиҝҳеҺҹжҖ§ DпјҺеҸҚеә”еҗҺжә¶ж¶Ій…ёжҖ§еўһејә |
|
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
жҠҠдәҢж°§еҢ–зЎ«е’ҢеҸҰдёҖз§Қж°”дҪ“XеҗҢж—¶йҖҡе…ҘBaCl2иҜ•ж¶ІдёӯпјҢдә§з”ҹдәҶжІүж·ҖпјҢеҲҷXдёҚеҸҜиғҪжҳҜ(гҖҖгҖҖ) AпјҺCl2гҖҖгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖгҖҖВ В В В В В В В В BпјҺNH3 CпјҺO2 В В В В В В В В В В В В В В В В В В В В В В В В В В В DпјҺCO2 |
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
|
е°Ҷж ҮеҮҶзҠ¶еҶөдёӢ3 360 mL SO2ж°”дҪ“йҖҡе…Ҙ100 mL 2 molВ·LпјҚ1зҡ„NaOHжә¶ж¶Ідёӯе……еҲҶеҸҚеә”пјҢжүҖеҫ—жә¶ж¶Ізҡ„жә¶иҙЁжҳҜ(гҖҖгҖҖ) AпјҺNa2SO3 В В В В В В В В В В В В В В В В В В В В В В В В BпјҺNaHSO3 CпјҺNa2SO3е’ҢNaHSO3 В В В В В В В В В В В В В В В DпјҺNaOHе’ҢNa2SO3 |
|
| 13. | иҜҰз»ҶдҝЎжҒҜ |
|
еҸ–дёҖе®ҡйҮҸзҡ„й“ҒзІүе’ҢзЎ«зІүзҡ„ж··еҗҲзү©йҡ”з»қз©әж°”еҠ зғӯпјҢе……еҲҶеҸҚеә”еҗҺеҶ·еҚҙпјҢеҶҚеҠ е…Ҙи¶ійҮҸзҡ„зЁҖзӣҗй…ёпјҢж ҮеҮҶзҠ¶еҶөдёӢз”ҹжҲҗ2.24 Lж°”дҪ“пјҢдёӢеҲ—иҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) AпјҺеҺҹж··еҗҲзү©дёӯеҸҜиғҪеҗ«3.2 gзЎ«зІү BпјҺеҺҹж··еҗҲзү©зҡ„иҙЁйҮҸеҸҜиғҪеӨ§дәҺ8.8 g CпјҺеҺҹж··еҗҲзү©дёӯдёҖе®ҡеҗ«жңү5.6 gй“ҒзІү DпјҺ2.24 Lж°”дҪ“зҡ„иҙЁйҮҸеҸҜиғҪеӨ§дәҺ3.4 g |
|
| 14. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—дёҚиғҪз”ЁжқҘеҢәеҲ«SO2е’ҢCO2ж°”дҪ“зҡ„жҳҜ(гҖҖгҖҖ) AпјҺжҫ„жё…зҹізҒ°ж°ҙ В В В В В В В В В В В В В В В В В В В BпјҺKMnO4жә¶ж¶І CпјҺж°Ҝж°ҙ В В В В В В В В В В В В В В В В В В В В В В В В В DпјҺе“Ғзәўжә¶ж¶І
|
|
| 15. | иҜҰз»ҶдҝЎжҒҜ |
|
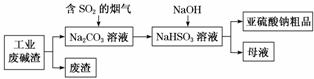
вҖңд»ҘеәҹжІ»еәҹвҖқжҳҜеҹәдәҺвҖңз»ҝиүІеҢ–еӯҰвҖқи§ӮеҝөжІ»зҗҶжұЎжҹ“зҡ„гҖӮз”Ёе·ҘдёҡеәҹзўұжёЈ(дё»иҰҒжҲҗеҲҶдёәNa2CO3)еҗёж”¶зғҹж°”дёӯзҡ„SO2пјҢеҫ—еҲ°Na2SO3зІ—е“ҒгҖӮе…¶жөҒзЁӢеҰӮеӣҫпјҡ
(1)дёәеҠ еҝ«е·ҘдёҡеәҹзўұжёЈдёӯNa2CO3зҡ„жә¶и§ЈпјҢеҸҜйҮҮеҸ–зҡ„жҺӘж–ҪжҳҜ________________(еҶҷеҮәдёҖз§ҚеҚіеҸҜ)гҖӮ (2)еҰӮеӣҫжөҒзЁӢдёӯпјҢеҠ е…ҘNaOHеҗҺпјҢеҸ‘з”ҹеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёә________________________гҖӮ (3)дәҡзЎ«й…ёй’ зІ—е“Ғдёӯеёёеҗ«жңүе°‘йҮҸNa2SO4пјҢеҺҹеӣ жҳҜ________________________________ ________________________________________________________________________гҖӮ (4)и®ҫи®Ўе®һйӘҢиҜҒжҳҺдәҡзЎ«й…ёй’ зІ—е“Ғеҗ«жңүе°‘йҮҸNa2SO4зҡ„ж–№жЎҲжҳҜпјҡеңЁдёҖж”ҜиҜ•з®ЎдёӯпјҢеҠ е…Ҙе°‘йҮҸдәҡзЎ«й…ёй’ зІ—е“ҒпјҢз”ЁйҖӮйҮҸи’ёйҰҸж°ҙжә¶и§ЈпјҢ__________________________________________________пјҢ еҮәзҺ°зҷҪиүІжІүж·ҖпјҢеҲҷиҜҒжҳҺеҗ«жңүNa2SO4гҖӮ |
|
| 16. | иҜҰз»ҶдҝЎжҒҜ |
|
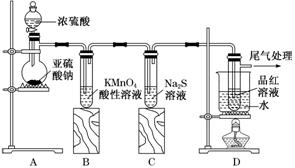
жҹҗеҢ–еӯҰе…ҙи¶Је°Ҹз»„дёәжҺўз©¶SO2зҡ„жҖ§иҙЁпјҢжҢүеҰӮеӣҫжүҖзӨәиЈ…зҪ®иҝӣиЎҢе®һйӘҢгҖӮиҜ·еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ
(1)иЈ…зҪ®Aдёӯзӣӣж”ҫдәҡзЎ«й…ёй’ зҡ„д»ӘеҷЁеҗҚз§°жҳҜ__________пјҢе…¶дёӯеҸ‘з”ҹеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёә________________________________________________________________________гҖӮ (2)е®һйӘҢиҝҮзЁӢдёӯпјҢиЈ…зҪ®BгҖҒCдёӯеҸ‘з”ҹзҡ„зҺ°иұЎеҲҶеҲ«жҳҜ__________________________гҖҒ________________________пјҢиҝҷдәӣзҺ°иұЎеҲҶеҲ«иҜҙжҳҺSO2е…·жңүзҡ„жҖ§иҙЁжҳҜ________е’Ң________пјӣиЈ…зҪ®BдёӯеҸ‘з”ҹеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸдёә______________________________________________ ________________________________________________________________________гҖӮ (3)иЈ…зҪ®Dзҡ„зӣ®зҡ„жҳҜжҺўз©¶SO2дёҺе“ҒзәўдҪңз”Ёзҡ„еҸҜйҖҶжҖ§пјҢиҜ·еҶҷеҮәе®һйӘҢж“ҚдҪңеҸҠзҺ°иұЎпјҡ________________________________________________________________________ ________________________________________________________________________гҖӮ (4)е°ҫж°”еҸҜйҮҮз”Ё________жә¶ж¶Іеҗёж”¶гҖӮ |
|
| 17. | иҜҰз»ҶдҝЎжҒҜ |
|
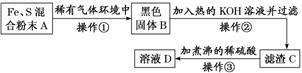
дёәдәҶйӘҢиҜҒй“Ғе’ҢзЎ«еҸҚеә”зҡ„дә§зү©дёӯй“Ғзҡ„еҢ–еҗҲд»·пјҢжҹҗеҗҢеӯҰи®ҫи®ЎдәҶдёҖдёӘе®һйӘҢпјҢеҰӮеӣҫжүҖзӨәпјҡ
иҜ·еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ (1)ж··еҗҲзІүжң«дёӯзЎ«зІүйңҖиҝҮйҮҸпјҢеҺҹеӣ жҳҜ____________________________________________ ________________________________________________________________________гҖӮ (2)еҸҚеә”еңЁвҖңзЁҖжңүж°”дҪ“зҺҜеўғдёӯвҖқиҝӣиЎҢзҡ„еҺҹеӣ жҳҜ________________________________ ________________________гҖӮ (3)з”Ёзғ§зғӯзҡ„зҺ»з’ғжЈ’зӮ№и§Ұж··еҗҲзІүжң«пјҢеҸҚеә”еҚіеҸҜжҢҒз»ӯиҝӣиЎҢпјҢиҜҙжҳҺ________________________________________________________________________гҖӮ (4)ж“ҚдҪңв‘Ўзҡ„дҪңз”ЁжҳҜ______________________пјҢд№ҹеҸҜж”№з”Ё________гҖӮ (5)ж“ҚдҪңв‘ўзЁҖзЎ«й…ёз…®жІёзҡ„зӣ®зҡ„жҳҜ_______________________________________гҖӮ (6)дёәиҜҒжҳҺдә§зү©дёӯй“Ғзҡ„д»·жҖҒпјҢеҜ№Dжә¶ж¶Ізҡ„е®һйӘҢж“ҚдҪңжңҖеҘҪжҳҜ ________________________________________________________________________гҖӮ |
|
- еұұдёң2019е№ҙй«ҳдёҖеҢ–еӯҰдёӢеҚҠжңҹжңҲиҖғжөӢйӘҢе…Қиҙ№жЈҖжөӢиҜ•еҚ·
- дёҠжө·дәӨйҖҡеӨ§еӯҰйҷ„еұһдёӯеӯҰй«ҳдәҢеҢ–еӯҰдёӢеҶҢжңҲиҖғиҜ•еҚ·еҲ·йўҳз»ғд№
- 2019-2020е№ҙй«ҳдёҖдёӢеҚҠе№ҙејҖеӯҰиҖғиҜ•еҢ–еӯҰиҜ•еҚ·еёҰеҸӮиҖғзӯ”жЎҲе’Ңи§ЈжһҗпјҲе№ҝдёңзңҒзҸ жө·еёӮ第дәҢдёӯеӯҰпјү
- 2019пҪһ2020е№ҙй«ҳдәҢдёҠеӯҰжңҹжңҹдёӯиҙЁйҮҸи°ғз ”еҢ–еӯҰйўҳејҖеҚ·жңүзӣҠпјҲжұҹиӢҸзңҒеҚ—йҖҡеёӮпјү
- 2019-2020е№ҙй«ҳдёҖдёҠеӯҰжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰйўҳе…Қиҙ№иҜ•еҚ·пјҲе№ҝдёңзңҒеҢ—еӨ§йҷ„дёӯж·ұеңіеҚ—еұұеҲҶж Ўпјү
- 2019-2020е№ҙй«ҳдёҖдёҠжңҹ第дәҢж¬ЎжңҲиҖғеҢ–еӯҰиҜ•еҚ·е®Ңж•ҙзүҲпјҲдә‘еҚ—зңҒжҳҶжҳҺеёӮеҶңдёҡеӨ§еӯҰйҷ„еұһдёӯеӯҰпјү
- еұұдёңзңҒеЁҒжө·еёӮ2020-2021е№ҙй«ҳдәҢдёҠеӯҰжңҹжңҹжң«иҖғиҜ•еҢ–еӯҰеңЁзәҝжөӢйӘҢе®Ңж•ҙзүҲ
- й«ҳдәҢдёӢжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰе…Қиҙ№иҜ•еҚ·еёҰзӯ”жЎҲе’Ңи§ЈжһҗпјҲ2019-2020е№ҙдёҠжө·еёӮдәӨйҖҡеӨ§еӯҰйҷ„еұһдёӯеӯҰпјү