2017福建高一上学期人教版高中化学月考试卷
| 1. | 详细信息 |
|
下列说法中正确的是( ) A.含有不同种元素的纯净物叫做化合物 B.水溶液中能电离出H+的化合物一定是酸 C.盐中一定含有金属元素 D.含有氧元素的化合物一定是氧化物
|
|
| 2. | 详细信息 |
|
用NA表示阿伏加德罗常数的值,下列叙述正确的是( ) A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L B.25℃,1.01×105 Pa,64g SO2中含有的原子数为3NA C.在常温常压下,11.2L Cl2含有的分子数为0.5NA D.标准状况下,11.2L H2O含有的分子数为0.5NA
|
|
| 3. | 详细信息 |
|
下列四组物质中,前者属于电解质,后者属于非电解质的是( ) A.二氧化碳 碳酸钠 B .硫酸钠 乙醇 C 氧化铝 硫 D. 盐酸 蔗糖
|
|
| 4. | 详细信息 |
|
下列说法正确的是( ) A.将BaSO4放入水中不能导电,所以硫酸钡不是电解质
|
|
| 5. | 详细信息 |
|
对下列实验过程的评价,正确的是 A. 某溶液中加入稀盐酸,产生无色气体,证明该溶液中一定有CO32- B.某溶液中先加少量氯化钡溶液,再加足量稀盐酸生成白色沉淀,证明该溶液中一定含有SO42- C.验证烧碱溶液中是否有Cl-,先加稀硝酸除去OH-,再加AgNO3溶液, 有白色沉淀产生,证明有Cl- D.某无色溶液滴入紫色石蕊试液显红色,该溶液一定显碱性
|
|
| 6. | 详细信息 |
|
等质量的①CH4、②H2、③HCl、④SO2,在标准状况下所占体积由大到小排列的顺序是( ) A、②>①>③>④ B、④>③>①>② C、③>②>④>① D、①>④>②>③
|
|
| 7. | 详细信息 |
|
下列溶液中物质的量浓度为1 mol·L-1的是 A.将40 g NaOH溶解在1 L水中 B.将200ml、2 mol·L-1HCl加水稀释配成2 L溶液 C.将10 g NaOH溶解在少量水中,再加蒸馏水直到溶液体积为250 mL D.将1 L 10 mol·L-1浓盐酸加入9 L水中
|
|
| 8. | 详细信息 |
|
下列不属于物理量的是( ) A.物质的量 B.质量 C.摩尔质量 D.摩尔
|
|
| 9. | 详细信息 |
|
下列物质既能由金属和酸反应获得,也能通过金属和氯气反应获得的是( ) A.CuCl2 B.FeCl2 C.FeCl3 D.AlCl3
|
|
| 10. | 详细信息 |
|
下列物质中,属于纯净物的是( ) A.液氯 B.氯水 C.稀盐酸 D.漂白粉
|
|
| 11. | 详细信息 |
|
下列叙述中,正确的是 ( ) A.次氯酸能杀死病菌,所以氯气可用于自来水的消毒 B.实验室制取氯气时,常用饱和石灰水来吸收多余的氯气 C.漂白粉中含有次氯酸,所以漂白粉能使染料等有机色素褪色 D.氯气不能使干燥的有色布条褪色,液氯能使干燥的有色布条褪色
|
|
| 12. | 详细信息 |
|
选择一种溶剂将碘水中的碘萃取出来,这种溶剂应该具有的性质( ) A.易溶于水,且不与碘发生反应 B.不溶于水,且比水更容易使碘溶解 C.不溶于水,且密度必须比水大 D.不溶于水,且密度必须比水小
|
|
| 13. | 详细信息 |
|
.放射性同位素铀 A.51 B.92 C.143 D.235
|
|
| 14. | 详细信息 |
|
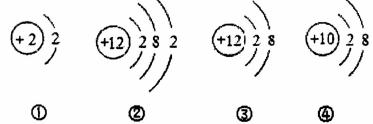
下列是几种粒子的结构示意图,有关说法正确的是
A.①和②两种粒子的化学性质相似 B.③和④均属于离子结构示意图 C.粒子②在化学反应中容易失去电子 D.①②③④共表示四种元素的粒子
|
|
| 15. | 详细信息 |
|
.下列各组物质中,互为同位素的是( ) A.
|
|
| 16. | 详细信息 |
|
能够用来鉴别BaCl2、NaCl、Na2CO3三种物质的试剂是( ) A.AgNO3 B.稀硫酸 C.稀盐酸 D.稀硝酸
|
|
| 17. | 详细信息 |
|
.下列溶液中阴离子浓度最大的是( ) A.0.5 mol.L-1HNO3溶液50mL B.0.6mol.L-1A12(SO4)3溶液35 mL C.1.8mol.L-1NaCl溶液70ml D.0.7mol.L-1 FeC13溶液60 mL
|
|
| 18. | 详细信息 |
|
下列电离方程式错误的是( ) A.KClO3 C.Mg(NO3)2
|
|
| 19. | 详细信息 |
|
.用浓硫酸配制一定物质的量浓度的硫酸溶液,下列操作会造成所配溶液浓度偏高的是( ) A.溶解后的溶液未冷却至室温就转移入容量瓶中 B.摇匀后,液面低于刻度线,再加蒸馏水至液面最低点恰好与刻度线相平 C.洗涤烧杯和玻璃棒的溶液未转移入容量瓶中 D.定容时,眼睛仰视刻度线
|
|
| 20. | 详细信息 |
|
实验室里需要480mL0.100mol/L的CuSO4溶液,以下操作正确的是( ) A.称取7.68gCuSO4,加入500mL水 B.称取12.5g胆矾,配成480mL溶液 C.称取8.0gCuSO4,加入到500mL水中配成溶液 D.称取12.5g胆矾,配成500mL溶液
|
|
| 21. | 详细信息 |
|
工业上制取氯气的化学方程式: ,又被称为______工业。 用双线桥法表示实验室制取氯气的化学方程式: 。 氧化剂:_____________ 还原剂:__________________
|
|
| 22. | 详细信息 |
|
将标准状况下22.4L HCl气体溶于水配成250mL溶液,此溶液中HCl的物质的量浓度为____________;将此10mL溶液加水稀释到100mL,稀释后溶液中HCl的物质的量浓度为_________;稀释后溶液中HCl的物质的量为___________。
|
|
| 23. | 详细信息 |
|
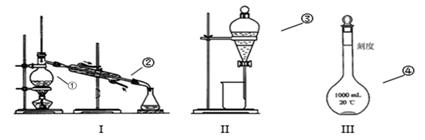
写出下图中序号①~④仪器的名称:
(1)① ;② ;③ ;④ ; (2)分离碘的四氯化碳溶液应选择装置 ,操作名称 _________ (3)分离水和汽油的混合物应选择装置 ,操作名称 __________ (4)使用仪器①时,往往要加入碎瓷片,目的是________;使用仪器②时,水流方向为:_____端进水,____端出水(填“上”或“下”)
|
|
| 24. | 详细信息 |
|
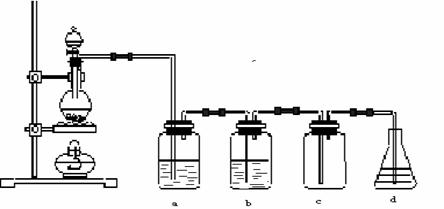
实验室制取氯气: ⑴ 装置及主要仪器:
a、b、d分别为洗气瓶②本气体发生装置为三大发生装置之一,适用于固体(或液体)与液体在加热条件下制气体的实验。 (1)净化方法:因浓HCl有挥发性,制的Cl2中常混有 和 杂质,a瓶所用试剂_________;b瓶所用试剂为________ (2)尾气吸收装置:因Cl2有毒污染空气,用_____________吸收多余的氯气,用方程式表示_______________________________ (3)已知产生的氯气的体积在标况下是2.24L,则参加反应的MnO2的质量是________g
|
|