2018山东高一上学期鲁科版高中化学月考试卷
| 1. | 详细信息 |
|
分离下列混合物,按溶解、过滤、蒸发顺序进行的是( ) A.氧化铜、木炭 B.硝酸钾、氯化钠 C.碳酸钙、氯化钠 D.乙醇、水
|
|
| 2. | 详细信息 |
|
0.5mol Na2SO4中所含的Na+离子数约为( ) A.0.5 B.6.02×1023 C.1 D.3.01×1023
|
|
| 3. | 详细信息 |
|
设NA为阿伏加德罗常数的数值,则下列说法中正确的是 A、500mL,1mol/L MgCl2溶液中含有Cl-数目为0.5NA B、标准状况下22.4 LH2O所含分子为1mol C、17gNH3含有的电子个数为10NA D、36gH2O与32gCH4所含的氢原子数相等
|
|
| 4. | 详细信息 |
|
含相同分子数的H2O和NH3一定具有相同的( ) A. 物质的量 B. 原子个数 C. 质量 D. 体积
|
|
| 5. | 详细信息 |
|
对下列物质进行的分类正确的是( )。 A.纯碱、烧碱均属于碱 B.CuSO4·5H2O属于纯净物 C.凡能电离出H+的化合物均属于酸 D.盐类物质一定含有金属阳离子
|
|
| 6. | 详细信息 |
|
下列物质中属于电解质的是( ) A.铁 B.熔融的氯化钠 C.盐酸 D.SO2
|
|
| 7. | 详细信息 |
|
在无色透明的溶液中可以大量共存的离子组是( ) A.Ca2+ Na+ CO32- Cl- B.Na+ K+ CO32- H+ C.Ba2+ Cu2+ SO42- Cl- D.Mg2+ Al3+ Cl- NO3-
|
|
| 8. | 详细信息 |
|
下列离子方程式书写正确的是( ) A. 铁和稀硫酸反应: 2Fe+6H+=2Fe3++3H2↑ B. 实验室用大理石与盐酸反应制取二氧化碳: CO32-+2H+= CO2↑+H2O C.碳酸银溶于稀硝酸: Ag2CO3+2H+=2Ag++CO2↑+H2O D.铜片插入硝酸银溶液中: Cu+Ag+=== Cu2++Ag
|
|
| 9. | 详细信息 |
|
下列反应不属于氧化还原反应的是( )。 A.3Fe + 4H2O(g) C.Ca(OH)2+SO2 = CaSO3 + H2O D.Cu+2H2SO4 (浓)
|
|
| 10. | 详细信息 |
|
下列微粒既具有氧化性又具有还原性的是( ) A.Al3+ B.Cl- C.Fe2+ D.H+
|
|
| 11. | 详细信息 |
|
在下列反应中,氧化产物和还原产物是同一种物质的是( ) A.Cl2+2NaOH=NaCl+NaClO+H2O B.Fe2O3+3CO=2Fe+3CO2 C.Zn+CuSO4=ZnSO4+Cu D.2H2S+SO2=3S+2H2O
|
|
| 12. | 详细信息 |
|
下列变化过程中,需要加入氧化剂的是( ) A.CO2 → CO B.FeCl3 →FeCl2 C.HCl → AgCl D. KI → I2
|
|
| 13. | 详细信息 |
|
人体血红蛋白中含有Fe2+,如果误食亚硝酸盐,会使人中毒。因为亚硝酸盐会使Fe2+转变成Fe3+,生成高铁血红蛋白而丧失与O2结合的能力。服用维生素C可缓解亚硝酸盐的中毒,这说明维生素C具有( ) A.酸性 B.碱性 C.氧化性 D.还原性
|
|
| 14. | 详细信息 |
|
下列有关钠的物理性质的叙述中正确的是( ) ①银白色金属 ②质软,可以用小刀切割 ③熔点低 ④密度比水小 ⑤热和电的良导体 A.①②④ B.①②③④ C.①③④ D.①②③④⑤
|
|
| 15. | 详细信息 |
|
少量的金属钠长期暴露在空气中,它的最终产物是( ) A.NaOH B. Na2CO3•10H2O C.Na2CO3 D.NaHCO3
|
|
| 16. | 详细信息 |
|
镁、铝、铜三种金属粉末混合物, 加入过量盐酸充分反应,过滤后向滤液中加入过量烧碱溶液,再过滤, 滤液中存在的离子有 ( ) A.AlO2— B.Cu2+ C.Al3+ D.Mg2+
|
|
| 17. | 详细信息 |
|
每做一次焰色反应实验,都要用一种试剂洗净铂丝,这种试剂是( )。A.Na2CO3溶液 B.NaOH溶液 C.硫酸 D.盐酸
|
|
| 18. | 详细信息 |
|
关于碳酸钠和碳酸氢钠的性质,下列说法正确的是( ) A.碳酸氢钠受热分解为碳酸钠,可以说明碳酸钠的稳定性强于碳酸氢钠 B.可加入少量稀盐酸除去碳酸氢钠溶液中混有的少量碳酸钠 C.可用氢氧化钡溶液鉴别碳酸钠和碳酸氢钠溶液 D.等质量的碳酸钠和碳酸氢钠与足量稀盐酸反应,产生等质量的气体
|
|
| 19. | 详细信息 |
|
把一定量的铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+与 Fe3+的物质的量浓度之比为3∶2。则已反应的Fe3+与未反应的Fe3+的物质的量之比是( ) A.1∶1 B.1∶2 C.2∶1 D.2∶3
|
|
| 20. | 详细信息 |
|
向某晶体的水溶液中加入Fe2+的溶液后,无明显变化,当滴加几滴氯水后混合液出现红色,那么由此得出的下列结论,错误的是( ) A、该晶体中一定含有SCN- B、Fe3+的氧化性比氯气的氧化性强 C、Fe2+被Cl2氧化为Fe3+ D、Fe3+与SCN-能形成红色的物质
|
|
| 21. | 详细信息 |
|
1)22克CO2的物质的量为 mol,其中含有O原子的个数为 ,含质子的物质的量为 mol,该气体在标准状况下的体积为 L。 (2)写出下列反应的离子方程式。 Fe2O3与稀盐酸反应 (3)写出下列离子方程式对应的任意一个化学方程式。 2H++CO32-
|
|
| 22. | 详细信息 |
|
实验室用固体烧碱配制100 mL 1.0 mol·L-1的NaOH溶液。 A、100 mL烧杯 B、500 mL容量瓶 C、玻璃棒 D、100 mL容量瓶 E、漏斗 F、胶头滴管 G、试管 H、托盘天平 I、 药匙 J、200 mL试剂瓶 (1)需称量_________ g 烧碱,应放在___________中(填写代号)称量、溶解。 (2)完成此配制实验,不需要用的仪器(填写代号)___________________ (3)在定容过程中,最后是用__________(填写代号)加入少量水,至凹液面的最低处与刻度线水平时停止加水。
|
|
| 23. | 详细信息 |
|
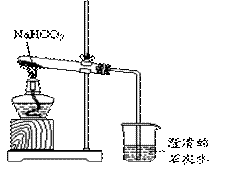
实验室利用右图所示装置进行NaHCO3的受热分解实验。请回答:
(2)实验结束时的正确操作是 (填字母); A.先从液体中移出导管,再熄灭酒精灯 B.先熄灭酒精灯,再从液体中移出导管。 否则会引起 。 (3)NaHCO3受热分解的化学方程式
|
|
| 24. | 详细信息 |
|
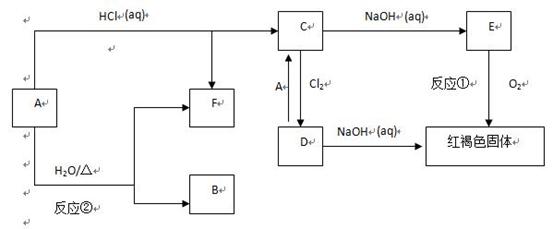
已知A为金属单质,它们之间能发生如下反应(部分产物未标出)
请根据以上信息回答下列问题: (1)写出物质B的化学式: (2)写出下列反应的化学方程式: 反应① 反应② (3)写出下列反应的离子方程式:
(4) 检验D中阳离子的方法:________________________________________________________________________________________________________________________
|
|